3D細胞培養市場規模と展望、2025年~2033年

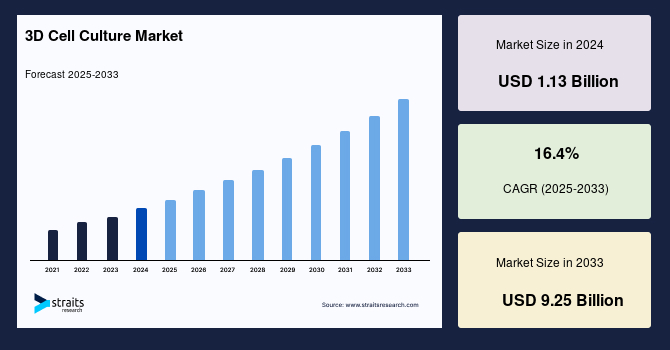
| 世界の3D細胞培養市場は、2024年に23億6000万米ドルと評価され、2025年には27億4000万米ドルに成長し、2033年には92億5000万米ドルに達すると予測されています。この期間中、年平均成長率は16.4%と見込まれています。市場の成長を促進する要因には、2D培養よりも3D培養技術の利点や研究開発の支出増加が含まれます。 3D細胞培養は、生体内の環境に類似した条件下での細胞配置を特徴としており、従来の培養法、臓器オンチップモデル、組織バイオエンジニアリングの3つに分類されます。3D培養は、細胞外マトリックス成分の発現を促進し、培養環境との相互作用を向上させるため、創薬や毒性試験、組織工学、基礎研究において重要な役割を果たしています。 市場の成長要因としては、3D細胞培養技術が生体内環境を正確に模擬できることが挙げられます。これにより、臨床試験への適用が進む一方で、研究開発への投資も増加しています。特に、創薬やがん治療、幹細胞研究においては、3D細胞培養が生物学的研究を推進しています。 一方で、3D細胞培養の導入には高いコストが伴い、特に専用の顕微鏡や高価な材料が必要なため、実験全体のコストが増加することが市場の成長を妨げる要因となっています。 技術の進歩が市場における新たな機会を生み出しており、特に3D細胞培養技術は医薬品開発において注目されています。イメージング技術の進展により、研究者は重要な結論を導き出すことができ、がん研究や再生医療においても3D細胞培養が広く受け入れられるようになっています。 地域別の市場動向では、北米が最も大きな市場であり、予測期間中の年平均成長率は14.3%と見込まれています。ヨーロッパも成長が期待され、年平均成長率は17.6%とされています。アジア太平洋地域は急成長が予測されており、日本や中国の研究機関が3D細胞培養製品を使用した研究を進めています。 市場は製品別、用途別、エンドユーザー別にセグメント化されており、特にスキャフォールドベースのプラットフォームが市場で高い貢献度を持っています。用途としては、がん研究や幹細胞研究、創薬、再生医療が重要な分野となっています。 主要企業には3D BiotekやCorning、Thermo Fisher Scientificなどがあり、今後も市場の成長が期待されています。最近では、企業間の提携や買収が進んでおり、技術革新が進展しています。3D細胞培養市場は、医療研究や新たな治療法の開発において重要な役割を果たすことが期待されています。 |
*** 本調査レポートに関するお問い合わせ ***
世界的な3D細胞培養市場は、2024年に11.3億米ドルの規模に達し、2025年には13.6億米ドル、そして2033年までには92.5億米ドルに成長すると予測されています。この予測期間(2025年から2033年)における年平均成長率(CAGR)は16.4%と見込まれています。市場成長の主な要因は、従来の2D培養技術と比較した3D細胞培養技術の優位性と、研究開発(R&D)活動への投資増加にあります。
**市場概要**
3D細胞培養とは、生物学的細胞をin vitro(生体外)で、生体内の状況、特に人体内の生理学的環境をより忠実に再現する形で配置・培養する技術を指します。この技術は、大きく分けて伝統的な培養法、オルガンオンチップモデル、そして組織バイオエンジニアリングの3つの主要なカテゴリーに分類されます。3D細胞培養技術は、その優れた利点から、創薬、毒性試験、組織工学、基礎研究といった分野において不可欠なツールとして認識されています。
従来の2D(単層)細胞培養は、細胞培養技術の発明以来、実験器具の基質に付着させて行われてきました。しかし、この人工的な環境は生体内の生理的条件を正確に模倣していないため、in vitro実験の結果を臨床試験に変換する際に課題が生じます。加えて、体内の細胞は常に細胞外マトリックス(ECM)やその他の様々な生物学的プロセスに曝され、相互作用しています。しかし、2D表面でのin vitro細胞培養では、特に特殊な細胞において、細胞の機能性、表現型、形態が頻繁に失われることが観察されます。これは、in vivo(生体内)の状況を適切に再現しているとは言えません。
これに対し、3D細胞培養はin vivo環境を正確にシミュレートすることでこれらの課題を克服し、より優れたモデルとして機能します。細胞を3次元(3D)で培養することで、細胞外マトリックス(ECM)成分の発現が促進され、培養環境との相互作用が向上します。このような2D細胞培養に対する明確な優位性により、3D細胞培養は急速に普及しており、調査期間中の市場拡大を強力に後押ししています。3D細胞培養は、分子レベルから全身レベルに至るまで、身体のプロセスや機能を再現する能力を持つため、創薬・開発、幹細胞研究、がん治療など、多様な医療応用における生物学研究を推進しています。
**市場促進要因**
市場の成長を牽引する主要な要因は、以下の点に集約されます。
1. **2D培養に対する3D細胞培養技術の優位性:** 3D細胞培養は、2D培養が抱える多くの課題を解決し、生体内の生理的環境をより正確に再現します。これにより、細胞の機能性、表現型、形態が維持されやすくなり、より信頼性の高い研究結果が得られます。特に、医薬品の有効性や毒性を評価する上で、in vivoでの反応を予測する能力が高いことは、創薬プロセスにおいて極めて重要です。この優れたモデルとしての特性が、研究者や製薬企業の間で3D細胞培養の採用を促し、市場拡大の最も強力な原動力となっています。
2. **研究開発(R&D)活動への投資増加:** 製薬およびバイオテクノロジー企業は、創薬、治療法、治療薬の開発にかかる全体的なコストと時間を削減するために、研究ベースの活動への投資を積極的に行っています。過去数十年にわたり、ヘルスケア分野では、公的機関および民間組織からの投資が増加しています。政府機関や確立された大手企業が、小規模なスタートアップ企業に投資するケースも多く見られます。このような製薬およびバイオテクノロジー企業や組織からの資金提供と投資の全体的な増加は、世界の3D細胞培養市場の成長を加速させる主要な要因となるでしょう。多額のR&D投資は、新しい3D細胞培養技術の開発、既存技術の改良、そしてその幅広い応用を可能にします。
3. **医療応用における需要の拡大:** 3D細胞培養は、その生体模倣能力により、創薬・開発、幹細胞研究、がん治療といった多様な医療応用で不可欠なツールとなっています。身体のプロセスや機能を分子レベルから全身レベルまで再現できる能力は、これらの分野における生物学研究を大きく推進しています。例えば、がん研究では、腫瘍微小環境をより正確に再現できる3Dモデルが、新しい治療法の開発や既存薬のスクリーニングに役立っています。また、再生医療分野では、複雑な組織や臓器の構築に向けた研究が活発化しており、3D細胞培養はその基盤技術として期待されています。
**市場抑制要因**
3D細胞培養市場の成長を抑制する可能性のある主な要因は以下の通りです。
1. **高コスト:** 3D細胞培養は、従来の単層培養よりもはるかに洗練されており、最先端の細胞培養用消耗品を必要とします。このため、実験全体の直接的なコストが上昇します。3D細胞培養には多くの利点があるものの、3D足場(スキャフォールド)や関連材料は、2D細胞培養用の実験器具よりも高価です。創薬における3D細胞培養の使用は、膨大な数の実験が必要となるため、医薬品開発コストを法外なものにしてしまう可能性があります。さらに、3D細胞培養におけるタンパク質や遺伝子発現の分析には、特殊な顕微鏡が必要です。合成ハイドロゲルや細胞外マトリックス(ECM)タンパク質の使用もコストを押し上げます。これらの要因は、実験プロセス全体の総コストを増加させるため、研究における3D細胞培養の魅力を低下させる可能性があります。
2. **技術的な複雑さと専門知識の必要性:** 3D細胞培養技術は、その高度な性質から、特定の技術的知識と熟練した操作を必要とします。2D培養と比較して、プロトコルの確立、細胞の生存率の維持、均一な培養条件の確保などがより複雑になる場合があります。この技術的なハードルは、特にリソースが限られている小規模な研究機関や新興企業にとって、導入の障壁となる可能性があります。
3. **標準化の課題:** 3D細胞培養モデルは多様であり、様々な足場材料、培養方法、細胞の種類が使用されます。この多様性は、異なる研究室間での結果の比較や、医薬品開発における規制当局への提出のための標準化を困難にします。標準化されたプロトコルや評価基準が十分に確立されていないことは、技術の広範な採用と商業化を遅らせる可能性があります。
**市場機会**
医療分野における数々の進歩の結果、技術は全体的なプロセスにおいて大きな役割を果たしています。3D細胞培養はそのような革新の一つであり、その人気は劇的に高まっています。市場における主要な機会は以下の通りです。
1. **技術革新と製品開発:** 過去数年間で、医薬品開発において細胞ベースのアプローチがより普及し、生化学的アッセイを徐々に置き換える傾向にあります。3D細胞培養技術は、より高品質なin vitro結果を生み出す可能性を秘めており、医薬品開発業界で大きな評価を得ています。さらに、3Dマイクロ組織の開発により、研究者はイメージング技術を活用して重要な結論を導き出すことができるようになりました。いくつかの企業は、3D画像をキャプチャし、分析し、さらに研究して新規治療法を開発するためのイメージング製品を開発しています。これらのヘルスケア関連製品の進歩の結果として、3D細胞培養は様々な産業分野の研究での使用において、より広く受け入れられるようになっています。
2. **幅広い応用分野での需要拡大:** がん研究、再生医療、幹細胞研究といった分野での3D細胞培養製品の利用が市場を成長させています。3Dスキャフォールドを使用して組織を作成する3Dマルチマテリアルプリンティング技術は、組織工学における3Dアクチュエーターの使用に対してカスタマイズされた機能を提供できます。これにより、個別の患者ニーズに対応した治療法の開発や、複雑な組織モデルの構築が可能になります。
3. **個別化医療の進展:** 3D細胞培養は、患者固有の細胞をin vitroで成長させることを可能にするため、病気の精密な個別化医療を開発する上で有利な機会を提供する可能性があります。これにより、患者ごとに最適化された薬剤スクリーニングや治療法の選択が可能となり、治療効果の向上と副作用の低減が期待されます。
4. **創薬プロセスの効率化:** 3Dモデルにおける薬剤感受性は、2D細胞培養モデルとは著しく異なるため、3D細胞培養は創薬および開発において非常に重要です。スクリーニング方法の改善は、早期の薬剤毒性評価と生理学的に価値のあるデータ収集を支援し、創薬プロセスを加速させると期待されています。これにより、開発期間の短縮とコスト削減が実現し、新たな医薬品の市場投入を促進します。
**セグメント分析**
3D細胞培養市場は、プラットフォーム、用途、エンドユーザーの観点から詳細に分析されています。
**1. プラットフォーム別**
市場は、足場ベースプラットフォーム、足場なしプラットフォーム、ゲル、バイオリアクター、マイクロチップ、およびサービスに二分されます。
* **足場ベースプラットフォーム:** このセグメントは市場への最大の貢献者であり、予測期間中に17%のCAGRで成長すると予想されています。足場ベースプラットフォームでは、細胞は細胞外マトリックス(ECM)または合成材料の内部で培養されます。足場の特性と材料の性質は、細胞の接着、増殖、および活性化に影響を与えます。必要な機械的機能と新しい組織形成の速度を達成するためには、使用される材料、新しい組織が形成される速度、および足場の特性を含む様々な特徴をアプリケーションに合わせて変更する必要があります。足場の孔分布、多孔性、および露出表面積は、細胞がECMにどの程度浸透し、どのくらいの速さで浸透するかに影響を与えることで、再生プロセスの最終的な成功度合いに影響を与える可能性があります。このアプローチは、特定の組織構造や生体力学的特性を模倣するのに特に有用です。
* **足場なしプラットフォーム:** 足場なしプラットフォームには、細胞外マトリックスやその他の生体材料は含まれません。これらのプラットフォームでは、表面がないため、細胞が自ら3Dの細胞外マトリックスを作成し、配置することが求められ、in vivo組織に非常に近い状態を再現します。自己組織化するこれらの球状の細胞コロニーの塊は「スフェロイド」と呼ばれます。これらの技術は、栄養素、酸素、二酸化炭素、廃棄物など、細胞が自然に生成する代謝および増殖勾配を正確に模倣するため、優れた生理学的モデルとなります。このモデルは、特に薬剤スクリーニングや基礎研究において、より生体に近い細胞応答を観察するのに適しています。
**2. 用途別**
市場は、がん研究、幹細胞研究、創薬、および再生医療に二分されます。
* **がん研究:** このセグメントは市場への最大の貢献者であり、予測期間中に15.5%のCAGRで成長すると予想されています。in vitro環境で典型的な細胞形態と機能を持つ腫瘍を再現するには、細胞外マトリックス(ECM)、間質細胞、がん幹細胞、および増殖する腫瘍細胞がすべて必要です。これらの要素は相互に影響し合い、最終的に腫瘍細胞培養モデルを形成します。これらの腫瘍細胞は、人体から取り出され2D環境で培養されると、これらの相互作用を失い、がん治療に対する反応が変化します。しかし、3D細胞培養モデルは、腫瘍微小環境を密接に模倣できるため、がん研究に利用できます。これにより、より正確な薬剤スクリーニング、治療標的の特定、および個別化されたがん治療法の開発が可能になります。近年、がんの罹患率が増加しているため、がんの診断と治療に関する研究が増加しており、がん患者向けの個別化された薬剤療法の開発に3D細胞培養がますます利用されています。
* **創薬:** 集中的なR&Dにより、3D培養技術は今や前臨床創薬における効果的なツールとして利用されており、研究コミュニティに限定されなくなっています。細胞生物学と組織工学手法の最近の進歩により、足場、多細胞スフェロイド、ハイドロゲル、3Dバイオプリンティング、オルガノイドなど、多種多様な3D細胞培養技術が開発されてきました。その結果、3D細胞培養モデルは、創薬プロセスの様々な段階でより頻繁に使用されるようになっています。3D細胞培養は、リード特定、前臨床最適化、およびターゲット検証の段階で最も一般的に使用されます。さらに、これらの培養は患者固有の細胞をin vitroで成長させることを可能にするため、病態生理学における3D細胞培養の導入は、疾患の精密な個別化医療を開発するための有利な機会を提供する可能性があります。また、3Dモデルにおける薬剤感受性は2D細胞培養モデルとは著しく異なるため、3D細胞培養は創薬および開発にとって極めて重要です。
* **幹細胞研究および再生医療:** これらの分野でも3D細胞培養の需要が高まっています。幹細胞の分化、増殖、および組織形成をより生体に近い環境で研究できるため、再生医療における細胞治療や組織工学の進展に不可欠な技術となっています。特に、臓器移植の需要増加と技術的に高度なソリューションを目指すR&D活動は、3D細胞培養製品の需要を牽引しています。
**3. エンドユーザー別**
市場は、バイオテクノロジー・製薬企業、受託研究機関(CRO)、および学術機関に二分されます。
* **学術機関:** このセグメントは市場への最大の貢献者であり、予測期間中に16.5%のCAGRで成長すると予想されています。進行中の創薬、開発、およびスクリーニングの実践を考慮すると、世界中の多くの機関や大学が、研究プロジェクトにおける3D細胞培養の使用による潜在的な成果を調査しています。様々なヘルスケアアプリケーションにおける3D細胞培養の需要増加に伴い、いくつかの企業が研究組織や臨床検査機関と提携しています。さらに、多くの学術機関は、様々な病状を治療するための新しい方法を開発するために、3D培養モデルにR&Dの取り組みを集中させています。例えば、ヘルムホルツ協会のある研究大学では、3D培養ベースのマイクロバイオリアクターシステムの最近の進歩、それに対応するin vitroモデル、および潜在的な応用について研究しています。3D細胞培養モデルは、細胞により自然な環境を提供するため、新しい治療法や治療法の開発を加速させると期待されています。
* **バイオテクノロジー・製薬企業:** 予測期間中、一部の製薬およびバイオテクノロジー企業からの需要が増加すると予想されます。これは、3D細胞培養が2D培養細胞よりも薬剤応答や毒性をより正確に予測できるためです。3D細胞のこれらの特性により、関連性のない薬剤候補を予備的に排除し、関連する薬剤化合物を検証することが可能になります。3D細胞培養を利用して薬剤応答を研究することで、早期の信頼性検証が可能となり、リソース、時間、コストの節約につながります。グローバルな3D細胞培養市場における製薬およびバイオテクノロジー企業セグメントの成長は、様々な技術的進歩、R&D活動への多額の投資、生物医学応用における3D細胞培養需要の増加、および3D細胞培養医療製品に対するFDA承認によっても主に推進されています。
**地域分析**
世界の3D細胞培養市場は、北米、欧州、アジア太平洋、ラテンアメリカ、中東、アフリカ(LAMEA)の5つの主要地域に区分されています。
* **北米:** 北米は最も大きな収益貢献地域であり、予測期間中に14.3%のCAGRで成長すると予想されています。米国、カナダ、メキシコが北米の3D細胞培養市場の大部分を占めると予測されています。再生医療および創薬・開発のために、研究機関や臨床検査機関と協力して3D培養技術を使用する多数の製薬およびバイオテクノロジー企業が存在するため、予測期間中もその優位性を維持すると予想されます。米国3D細胞培養市場は、北米市場全体の最大のシェアを占めると予想されています。3D培養製品の需要増加は、主に臓器移植の需要増加と、技術的に高度なソリューションを目指すR&D活動によって説明されます。
* **欧州:** 欧州は予測期間中に17.6%のCAGRで成長すると予想されており、これは全地域の中で最も高い成長率です。ドイツ、フランス、英国、およびその他の欧州諸国が欧州地域として研究されています。世界の3D細胞培養市場において、この地域は第2位に位置すると予測されています。主要なバイオ医薬品企業がこの地域に存在し、民間組織による資金提供活動の増加がこれに寄与しています。さらに、過去数年間、欧州ではオルガノイドに関する重要なバイオテクノロジーR&Dと、学術界および産業界の最前線での製品開発が見られます。加えて、がんの罹患率の増加により、がん診断と治療に関する研究が増加しており、3D細胞培養は、がん患者向けの個別化された薬剤療法を作成するためにますます使用されています。
* **アジア太平洋:** この地域は予測期間中により速く成長すると予想されています。日本、中国、インド、オーストラリア、およびその他のアジア太平洋地域が地域分析に含まれます。がん、幹細胞、再生医療に関する研究で3D細胞培養製品が使用される可能性が高いため、この地域での需要が増加しています。これにより、研究者は線維症の異なるレベルを標的とする治療法を調整できるようになります。さらに、中国は、創薬におけるR&Dを進めようとしている製薬およびバイオテクノロジー企業にとって、巨大な新しい機会を提供する新興市場であると考えられています。
* **ラテンアメリカ、中東、アフリカ(LAMEA):** ブラジルは、ヘルスケア分野における研究需要の高まりの結果として、LAMEA市場拡大において重要な役割を果たしています。3D細胞培養の利点はこれらの疾患の治療に利用でき、市場の拡大を助けるでしょう。さらに、南アフリカに拠点を置くノースウェスト大学(NWU)の医薬品科学センターオブエクセレンス(PharmacenTM)では、研究目的の高度な細胞培養イニシアチブに関する研究プロジェクトが進行中です。同センターは現在、デンマークのバイオテクノロジー企業CelVivo IVSと協力し、3D細胞培養技術を用いてがん研究を標的としています。多くの製薬会社も、今後数年間で地理的拡大と経済的利益のための収益性の高い機会を提供すると予想されるため、この地域での事業を拡大しています。
Report Coverage & Structure
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制限と前提
- 市場範囲とセグメンテーション
- 考慮される通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場トレンド
- 推進要因
- 市場警報要因
- 最新のマクロ経済指標
- 地政学的な影響
- 技術的要因
- 市場評価
- ポーターの5つの力分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- ヨーロッパ
- アジア太平洋
- 中東およびアフリカ
- ラテンアメリカ
- ESGトレンド
- 世界の3D細胞培養市場規模分析
- 世界の3D細胞培養市場の概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- 北米市場分析
- 概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- 米国
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- カナダ
- ヨーロッパ市場分析
- 概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- 英国
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他のヨーロッパ
- アジア太平洋市場分析
- 概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- 中国
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- 韓国
- 日本
- インド
- オーストラリア
- 台湾
- 東南アジア
- その他のアジア太平洋
- 中東およびアフリカ市場分析
- 概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- アラブ首長国連邦
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他のMEA
- ラテンアメリカ市場分析
- 概要
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- ブラジル
- 製品別
- 概要
- 製品別金額
- スキャフォールドフリープラットフォーム
- 金額別
- ゲル
- ゲル別金額
- バイオリアクター
- バイオリアクター別金額
- マイクロチップ
- マイクロチップ別金額
- サービス
- サービス別金額
- スキャフォールドベースプラットフォーム
- 金額別
- マクロスケール
- マクロスケール別金額
- マイクロスケール
- マイクロスケール別金額
- ナノスケール
- ナノスケール別金額
- ソリッドスキャフォールド
- ソリッドスキャフォールド別金額
- アプリケーション別
- 概要
- アプリケーション別金額
- がん研究
- 金額別
- 幹細胞研究
- 金額別
- 創薬
- 金額別
- 再生医療
- 金額別
- 最終用途別
- 概要
- 最終用途別金額
- 製薬およびバイオテクノロジー企業
- 金額別
- 学術および研究機関
- 金額別
- 病院および診断ラボ
- 金額別
- その他
- 金額別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のラテンアメリカ
- 競合状況
- 3D細胞培養市場のプレーヤー別シェア
- M&A契約とコラボレーション分析
- 市場プレーヤー評価
- 3DバイオテックLLC
- 概要
- 事業情報
- 収益
- ASP
- SWOT分析
- 最近の動向
- アドバンストバイオマトリックスInc.
- アバンターInc.
- ベクトン
- ディキンソン・アンド・カンパニー
- コーニング・インコーポレイテッド
- インスフェロAg
- ロンザ・グループLtd.
- メルク・アンド・カンパニーInc.
- シンセコン
- インコーポレイテッド
- サーモフィッシャーサイエンティフィックInc.
- 調査方法
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次情報の内訳
- 二次および一次調査
- 主要な業界インサイト
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査の前提
- 前提
- 制限事項
- リスク評価
- 付録
- ディスカッションガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
*** 本調査レポートに関するお問い合わせ ***

3D細胞培養は、細胞を生体内の三次元的な環境により近づけて培養する技術でございます。従来の2D培養が細胞を平坦な表面で増殖させるのに対し、3D培養では細胞が互いに、また細胞外マトリックス(ECM)と立体的に相互作用できる環境を提供いたします。これにより、細胞の形態、増殖、分化、遺伝子発現、機能などが生体内により近い状態で再現され、より生理学的に関連性の高い研究が可能となります。この技術は、細胞間コミュニケーションや組織構造の形成といった複雑な生物学的プロセスを研究する上で極めて重要でございます。
3D細胞培養には、そのアプローチによっていくつかの種類がございます。一つは「スキャフォールド(足場)を用いる方法」で、コラーゲン、マトリゲル、アルギネートなどのハイドロゲルや、ポリ乳酸などの多孔質ポリマー製の足場が細胞の物理的な支持体となり、生体組織に近い環境を提供いたします。これにより、細胞の接着、増殖、分化を促進します。一方、「スキャフォールドを用いない方法」も広く用いられており、これは細胞が自己集合する能力を利用して、球状の細胞塊(スフェロイドやオルガノイド)を形成させるものです。具体的には、ハンギングドロップ法、低接着性プレートでの培養、あるいは回転培養器やバイオリアクターを用いて細胞を浮遊させながら培養する方法などがございます。これらの方法では、細胞が自ら細胞外マトリックス(ECM)を分泌し、細胞間接着を介して三次元構造を構築いたします。
3D細胞培養の応用範囲は非常に広範でございます。最も顕著な用途の一つは「創薬研究と開発」で、より生体に近い環境で薬物の有効性や毒性を評価できるため、従来の2D培養よりも高精度なスクリーニングが可能となります。これにより、臨床試験での失敗率を低減し、開発期間の短縮に貢献いたします。また、「疾患モデルの構築」においても重要な役割を果たしており、がん、神経変性疾患、感染症などの複雑な病態をin vitroで再現し、病気のメカニズム解明や新しい治療法の探索に役立てられております。さらに、「再生医療」の分野では、機能的な組織や臓器をin vitroで構築するための基盤技術として期待されており、将来的には移植可能な組織の作製や、損傷した組織の修復に応用される可能性がございます。基礎研究においても、細胞生物学、発生生物学、組織工学といった様々な分野で、生体内の複雑な現象をより忠実に再現し、深く理解するための強力なツールとして活用されております。
3D細胞培養の発展は、様々な関連技術の進化によって加速されております。特に注目されるのは「オルガノイド」技術で、多能性幹細胞や体性幹細胞から自己組織化によって形成されるミニ臓器のような三次元構造体を指します。これは、実際の臓器の細胞組成、構造、機能の一部を再現できるため、疾患モデル、創薬、再生医療の分野で革新的なツールとして期待されております。また、「マイクロ流体デバイス(Lab-on-a-chip)」は、微細な流路内で細胞を培養し、培養環境を精密に制御する技術であり、複数の異なる組織を連結して生体内の臓器間相互作用を再現する「臓器チップ(Organ-on-a-chip)」へと発展しております。これにより、より複雑な生理学的応答の評価が可能となります。さらに、「3Dバイオプリンティング」は、細胞や生体材料を一層ずつ積み重ねて三次元構造を直接作製する技術で、複雑な組織や人工臓器の構築を目指す最先端のアプローチでございます。これらの技術は、それぞれが独立して進化するだけでなく、互いに連携することで、3D細胞培養の可能性を大きく広げております。