デュシェンヌ型筋ジストロフィー治療市場:規模・シェア分析、成長動向・予測 (2025年~2030年)
デュシェンヌ型筋ジストロフィー治療市場レポートは、治療アプローチ(分子ベース、ステロイド療法、NSAIDs、その他)、投与経路(静脈内、皮下、経口)、流通チャネル(病院薬局、小売薬局、オンライン薬局)、および地域(北米、欧州、アジア太平洋など)別に区分されます。市場予測は金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
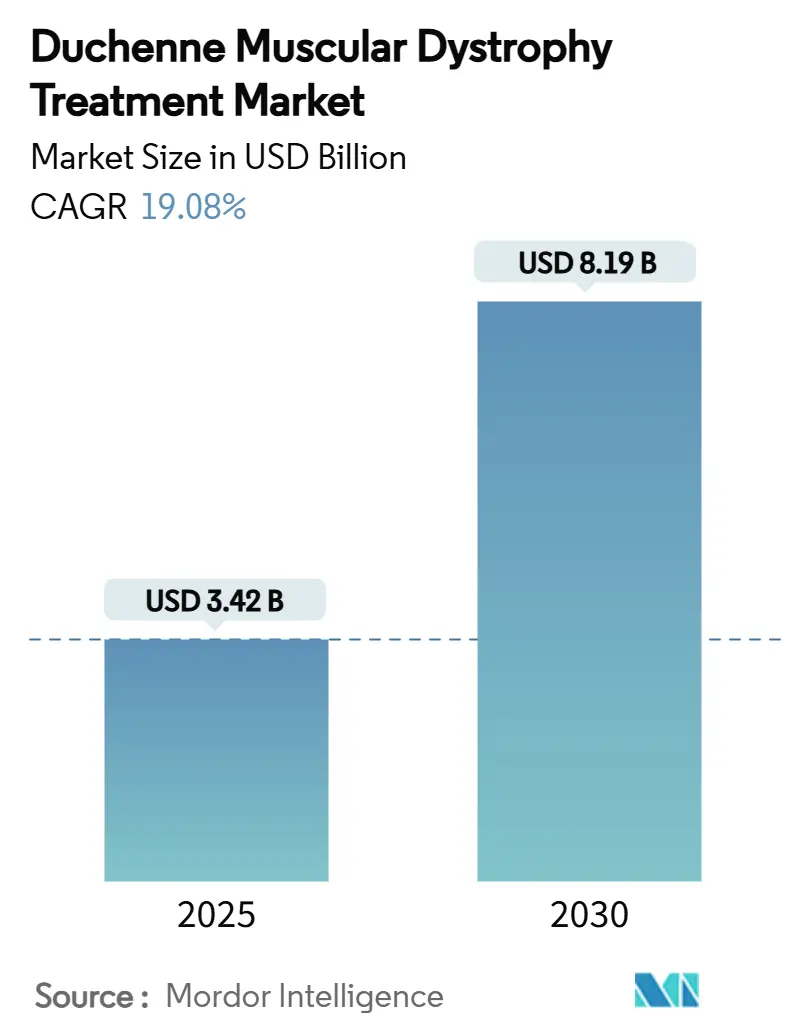
デュシェンヌ型筋ジストロフィー(DMD)治療市場は、2025年に34.2億米ドル、2030年には81.9億米ドルに達し、予測期間中の年平均成長率(CAGR)は19.08%と見込まれています。画期的な遺伝子治療、規制当局による承認の加速、継続的なベンチャー投資が治療基準を再定義し、緩和ケアから持続的な疾患修飾介入へとケアの焦点が移行しています。米国食品医薬品局(FDA)によるデランジストロゲン・モクセパルボベックの承認拡大、初の非ステロイド性薬剤であるギビノスタット、およびコルチコステロイド代替薬であるバモロロンの承認は、分子標的アプローチが優勢な多角的エコシステムを形成しています。投資家の関心は高く、オリゴヌクレオチドおよびCRISPR技術のイノベーターへの記録的な資金調達が見られます。大手企業におけるプログラム中止による競争環境の再編は、新興企業に機会をもたらし、スケーラブルなベクター製造への注目を高めています。地理的にはアジア太平洋地域が成長の中心であり、日本と中国の規制当局が審査を加速させています。
主要なレポートのポイント
* 治療アプローチ別: 分子標的治療製品が2024年にDMD治療市場シェアの61.34%を占めると予測されています。
* 薬剤タイプ別: 遺伝子治療薬が最も急速に成長するセグメントであり、予測期間中にCAGR 25%以上で成長すると見込まれています。
* 投与経路別: 経口投与薬が依然として主要なシェアを占めていますが、静脈内投与薬の採用が増加しています。
* 地域別: 北米が最大の市場シェアを保持していますが、アジア太平洋地域が最も高い成長率を示すと予測されています。
* 主要企業: 主要な市場プレーヤーは、新製品開発、戦略的提携、およびM&Aに注力しており、市場競争は激化しています。
市場の動向と推進要因
デュシェンヌ型筋ジストロフィー(DMD)治療市場は、画期的な治療法の進歩、特に遺伝子治療と分子標的治療の開発によって大きく推進されています。これらの治療法は、疾患の根本原因に対処し、患者の生活の質を大幅に改善する可能性を秘めています。また、規制当局による承認プロセスの加速も市場成長の重要な要因です。FDAや欧州医薬品庁(EMA)などの機関は、希少疾患に対する治療法の迅速な承認を促進しており、これにより新薬がより早く患者に届けられるようになっています。
さらに、DMDに関する意識の高まりと診断率の向上も市場拡大に寄与しています。早期診断は、治療介入のタイミングを早め、疾患の進行を遅らせる上で極めて重要です。政府や非営利団体によるDMD研究への資金提供の増加も、新しい治療法の発見と開発を後押ししています。
課題と制約
DMD治療市場は成長を続けていますが、いくつかの課題に直面しています。最も顕著なのは、新しい遺伝子治療や分子標的治療の高額な費用です。これらの治療法は、開発コストが高く、製造プロセスも複雑であるため、患者や医療システムにとって大きな経済的負担となる可能性があります。これにより、治療へのアクセスが制限される可能性があります。
また、DMDの複雑な病態生理学と、患者間の遺伝的変異の多様性も、効果的な治療法を開発する上での課題となっています。すべての患者に効果的な単一の治療法を見つけることは困難であり、個別化医療アプローチの必要性が高まっています。さらに、長期的な安全性と有効性に関するデータが不足していることも、一部の新しい治療法に対する懸念材料となっています。特に、遺伝子治療においては、免疫反応やオフターゲット効果のリスクが慎重に監視される必要があります。
市場の機会
DMD治療市場には、いくつかの大きな機会が存在します。未だ満たされていない医療ニーズが高いことから、新規治療法の開発と商業化の余地は依然として大きいです。特に、疾患の進行を完全に停止させる、あるいは逆転させる可能性のある治療法に対する需要は非常に高いです。
バイオテクノロジー企業と製薬企業間の戦略的提携や共同研究は、研究開発の加速と市場投入までの期間短縮に貢献しています。また、AIや機械学習などの先進技術を創薬プロセスに統合することで、新しい治療標的の特定や薬剤候補のスクリーニングが効率化される可能性があります。
アジア太平洋地域などの新興市場は、DMD治療市場にとって大きな成長機会を提供しています。これらの地域では、医療インフラの改善、診断能力の向上、およびDMDに対する意識の高まりが見られます。日本や中国などの国々では、規制当局が希少疾患治療薬の審査を加速させており、これにより市場へのアクセスが容易になっています。
結論
DMD治療市場は、画期的な科学的進歩と投資家の強い関心に支えられ、今後も力強い成長が予測されます。遺伝子治療や分子標的治療の進化は、患者の予後を改善し、疾患管理のパラダイムを変化させる可能性を秘めています。しかし、高額な治療費や長期的な安全性データなどの課題に対処することが、市場の持続的な成長と広範なアクセスを確保するために不可欠です。
このレポートは、デュシェンヌ型筋ジストロフィー(DMD)治療市場に関する詳細な分析を提供しています。DMDは、X連鎖劣性遺伝パターンによって引き起こされる、筋肉の進行性の消耗と衰弱を特徴とする希少な遺伝性疾患です。本レポートでは、治療アプローチと地域別に市場をセグメント化し、各セグメントの市場規模と予測を米ドル(USD)で示しています。
市場は2030年までに81.9億米ドルに達すると予測されており、予測期間中の年平均成長率(CAGR)は19.08%と非常に高い成長が見込まれています。治療アプローチ別では、分子ベースの治療法が市場の61.34%を占め、遺伝子置換やエクソンスキッピングの進歩により、今後も主導的なカテゴリーであり続けると予想されています。
市場の成長を牽引する主な要因としては、DMDの疾病負担の増加、新規治療法への投資の拡大、アンチセンスエクソンスキッピング薬の承認の勢い、オーファンドラッグのインセンティブと優先審査バウチャーの存在が挙げられます。さらに、CRISPRプラットフォーム取引による遺伝子編集パイプラインの加速や、患者募集を改善する分散型臨床試験も市場拡大に寄与しています。
一方で、市場にはいくつかの課題も存在します。標準化された臨床的有効性評価指標の不足、高額な治療費と償還に関するハードル、高用量AAVベクターの製造におけるボトルネック、オフターゲット遺伝子編集に関する規制の不確実性が主な抑制要因となっています。
地域別では、アジア太平洋地域が最も急速に成長する市場であり、2030年までのCAGRは19.98%と予測されています。これは、日本における迅速承認や中国における優先審査制度、そして臨床インフラの拡大が主な要因です。
償還に関する課題に対しては、支払者が価値ベースの契約、分割払い、リアルワールドエビデンスの収集を試行し、高額な初期費用と長期的な治療成果のバランスを取ろうとしています。また、皮下投与経路は、自己投与による通院回数の削減、服薬遵守の向上、およびデポ型またはオートインジェクタープラットフォーム向けに設計されたパイプライン薬剤の存在により、19.83%のCAGRで成長すると見込まれています。
競争環境においては、Sarepta Therapeutics、PTC Therapeutics、Nippon Shinyaku(NS Pharma)、Pfizerなどの主要企業が名を連ねています。Dyne Therapeutics、Edgewise Therapeutics、Capricorといった新興企業は、最適化されたオリゴヌクレオチド、筋肉保護小分子、心臓標的エクソソームなどの新規メカニズムを活用し、既存の遺伝子治療企業との差別化を図り、市場の挑戦者として台頭しています。
本レポートでは、治療アプローチ(分子ベース、ステロイド療法、NSAIDsなど)、投与経路(静脈内、皮下、経口)、流通チャネル(病院薬局、小売薬局、オンライン薬局)、および地理(北米、欧州、アジア太平洋、中東・アフリカ、南米)といった多角的なセグメンテーションに基づいて市場を分析しています。
DMD治療市場は、未充足のニーズと将来の展望において大きな機会を秘めており、継続的なイノベーションと戦略的な取り組みがその成長をさらに加速させるでしょう。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
- 4.2 市場の推進要因
- 4.2.1 DMDの疾病負荷の増加
- 4.2.2 新規治療法への投資の増加
- 4.2.3 アンチセンスエクソンスキッピング薬の承認の勢い
- 4.2.4 希少疾病用医薬品のインセンティブと優先審査バウチャー
- 4.2.5 CRISPRプラットフォーム取引による遺伝子編集パイプラインの加速
- 4.2.6 分散型試験による患者募集の改善
- 4.3 市場の阻害要因
- 4.3.1 標準化された臨床有効性評価項目の不足
- 4.3.2 高額な治療費と償還の障壁
- 4.3.3 高用量AAVベクターの製造上のボトルネック
- 4.3.4 オフターゲット遺伝子編集に関する規制の不確実性
- 4.4 規制環境
- 4.5 ポーターの5つの力分析
- 4.5.1 買い手の交渉力
- 4.5.2 供給者の交渉力
- 4.5.3 新規参入の脅威
- 4.5.4 代替品の脅威
- 4.5.5 競争上の対抗関係
5. 市場規模と成長予測(金額、米ドル)
- 5.1 治療アプローチ別
- 5.1.1 分子ベース
- 5.1.1.1 変異抑制
- 5.1.1.2 エクソンスキッピング
- 5.1.2 ステロイド療法
- 5.1.3 NSAIDs
- 5.1.4 その他
- 5.2 投与経路別
- 5.2.1 静脈内
- 5.2.2 皮下
- 5.2.3 経口
- 5.3 流通チャネル別
- 5.3.1 病院薬局
- 5.3.2 小売薬局
- 5.3.3 オンライン薬局
- 5.4 地域別
- 5.4.1 北米
- 5.4.1.1 米国
- 5.4.1.2 カナダ
- 5.4.1.3 メキシコ
- 5.4.2 欧州
- 5.4.2.1 ドイツ
- 5.4.2.2 英国
- 5.4.2.3 フランス
- 5.4.2.4 イタリア
- 5.4.2.5 スペイン
- 5.4.2.6 その他の欧州
- 5.4.3 アジア太平洋
- 5.4.3.1 中国
- 5.4.3.2 日本
- 5.4.3.3 インド
- 5.4.3.4 オーストラリア
- 5.4.3.5 韓国
- 5.4.3.6 その他のアジア太平洋
- 5.4.4 中東およびアフリカ
- 5.4.4.1 GCC
- 5.4.4.2 南アフリカ
- 5.4.4.3 その他の中東およびアフリカ
- 5.4.5 南米
- 5.4.5.1 ブラジル
- 5.4.5.2 アルゼンチン
- 5.4.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
- 6.3 企業プロファイル(グローバル概要、市場概要、主要セグメント、利用可能な財務情報、戦略情報、主要企業の市場ランキング/シェア、製品およびサービス、最近の動向を含む)
- 6.3.1 Sarepta Therapeutics
- 6.3.2 PTC Therapeutics
- 6.3.3 Nippon Shinyaku (NS Pharma)
- 6.3.4 Pfizer
- 6.3.5 Italfarmaco
- 6.3.6 Santhera Pharmaceuticals
- 6.3.7 FibroGen
- 6.3.8 BioMarin
- 6.3.9 Roche / Genentech
- 6.3.10 Wave Life Sciences
- 6.3.11 Solid Biosciences
- 6.3.12 Dyne Therapeutics
- 6.3.13 Edgewise Therapeutics
- 6.3.14 Regenxbio
- 6.3.15 Alexion (AstraZeneca Rare Disease)
- 6.3.16 Genethon
- 6.3.17 Eli Lilly
- 6.3.18 Dystrogen Therapeutics
- 6.3.19 Entrada Therapeutics
7. 市場機会と将来展望
*** 本調査レポートに関するお問い合わせ ***

デュシェンヌ型筋ジストロフィー治療に関する包括的な概要を以下に示します。
デュシェンヌ型筋ジストロフィー(DMD)は、主に男児に発症する重篤な遺伝性疾患であり、その治療法は医学の進歩とともに大きく変化してきました。この疾患は、筋肉の細胞膜を安定させる役割を持つジストロフィンというタンパク質の遺伝子(DMD遺伝子)に変異が生じることで、ジストロフィンが欠損または機能不全となるために発症します。その結果、筋肉細胞が脆弱になり、進行性の筋力低下と筋組織の変性が引き起こされます。幼少期に発症し、歩行能力の喪失、呼吸筋や心筋の障害へと進行し、最終的には呼吸不全や心不全により若年で命を落とすことが多い難病です。
治療の種類は大きく分けて、根本的な原因にアプローチする「根本治療」と、症状の進行を遅らせたり、合併症を管理したりする「対症療法・支持療法」があります。根本治療としては、ジストロフィン遺伝子の変異を直接修正したり、機能的なジストロフィンを補充したりするアプローチが研究・開発されています。具体的には、エクソンスキッピング療法、遺伝子治療、そして遺伝子編集技術が挙げられます。エクソンスキッピング療法は、DMD遺伝子のmRNAスプライシングを操作することで、一部の変異をスキップし、短縮型ではあるものの機能的なジストロフィンを産生させることを目指します。これは特定の遺伝子変異を持つ患者さんにのみ適用可能です。遺伝子治療は、アデノ随伴ウイルス(AAV)などのベクターを用いて、機能的なジストロフィン遺伝子(通常は小型化したマイクロジストロフィン遺伝子)を患者さんの筋肉細胞に導入するものです。遺伝子編集技術は、CRISPR/Cas9システムなどを用いて、DMD遺伝子上の変異を直接修正し、正常なジストロフィン産生を回復させることを目指す、より根本的なアプローチとして期待されていますが、まだ臨床応用には多くの課題が残されています。
対症療法・支持療法は、患者さんの生活の質(QOL)を維持し、合併症を管理するために不可欠です。ステロイド療法は、プレドニゾロンやデフラザコートといった薬剤が用いられ、筋力低下の進行を遅らせ、歩行期間を延長し、呼吸機能や心機能の低下を抑制する効果が認められています。しかし、長期使用による副作用(骨粗鬆症、体重増加、成長障害など)も考慮する必要があります。リハビリテーションは、理学療法や作業療法を通じて、関節の拘縮予防、筋力維持、呼吸機能の改善、日常生活動作の支援を行います。呼吸管理は、病気の進行に伴う呼吸筋の弱化に対して、非侵襲的陽圧換気(NIPPV)や、必要に応じて気管切開による人工呼吸器管理が行われます。心臓管理は、心筋症の進行を遅らせるために、ACE阻害薬やβ遮断薬などが用いられます。その他、骨粗鬆症対策、栄養管理、整形外科的介入(脊柱側弯症の手術など)も重要な治療の一部です。
関連技術としては、エクソンスキッピング療法に用いられるアンチセンスオリゴヌクレオチド(ASO)技術、遺伝子治療の基盤となるAAVベクター技術、そして次世代の根本治療として期待されるCRISPR/Cas9などの遺伝子編集技術が挙げられます。また、疾患メカニズムの解明や薬剤スクリーニングに貢献するiPS細胞技術、治療効果の評価や疾患進行のモニタリングに不可欠なバイオマーカー開発、さらには個別化医療の実現に向けたAIやビッグデータ解析も重要な役割を担っています。これらの技術は、DMD治療の選択肢を広げ、より効果的な治療法の開発を加速させています。
市場背景としては、デュシェンヌ型筋ジストロフィーが希少疾患であるため、多くの治療薬がオーファンドラッグ(希少疾病用医薬品)として指定されています。これにより、開発企業は研究開発費の助成や市場独占期間の延長といったインセンティブを受け、新薬開発が促進されています。現在、複数のエクソンスキッピング薬が承認され、特定の遺伝子変異を持つ患者さんへの治療選択肢となっています。また、遺伝子治療薬も米国で加速承認されるなど、新たな治療モダリティが市場に登場し始めています。しかし、これらの先進的な治療薬は非常に高額であり、医療経済性や患者さんへのアクセス確保が大きな課題となっています。世界中で多くの製薬企業やバイオベンチャーがDMD治療薬の開発競争を繰り広げており、患者団体も研究資金の調達や政策提言を通じて、治療開発を強力に支援しています。
今後の展望としては、個別化医療のさらなる進展が期待されます。患者さん一人ひとりの遺伝子変異や病態に合わせた最適な治療法を選択する時代が到来するでしょう。エクソンスキッピング療法は、より多くの遺伝子変異に対応できるよう、新たな薬剤の開発が進められています。遺伝子治療は、より安全で効果的なベクターの開発、全身への効率的な送達、免疫反応の抑制などが今後の課題となりますが、その可能性は非常に大きいと考えられています。遺伝子編集技術の実用化も、長期的な目標として研究が進められており、オフターゲット効果の抑制やデリバリー方法の確立が鍵となります。また、複数の治療法を組み合わせる併用療法や、疾患の進行をより早期に診断し、介入する新生児スクリーニングの導入も、患者さんの予後を大きく改善する可能性を秘めています。治療費の高騰という課題に対しては、持続可能な医療提供体制の構築や、費用対効果を考慮した薬剤評価の仕組みが求められます。国際的な研究協力や情報共有も、希少疾患であるDMDの治療開発を加速させる上で不可欠であり、患者さんのQOL向上と生命予後の改善に向けた努力が続けられています。