治療薬物モニタリング市場 規模・シェア分析 ― 成長動向と予測 (2026年~2031年)
治療薬物モニタリング市場は、テクノロジー(イムノアッセイ、プロテオミクスなど)、薬剤クラス(抗不整脈薬、免疫抑制剤など)、エンドユーザー(病院検査室、独立/リファレンス検査室など)、および地域によってセグメント化されています。市場規模と予測は、金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
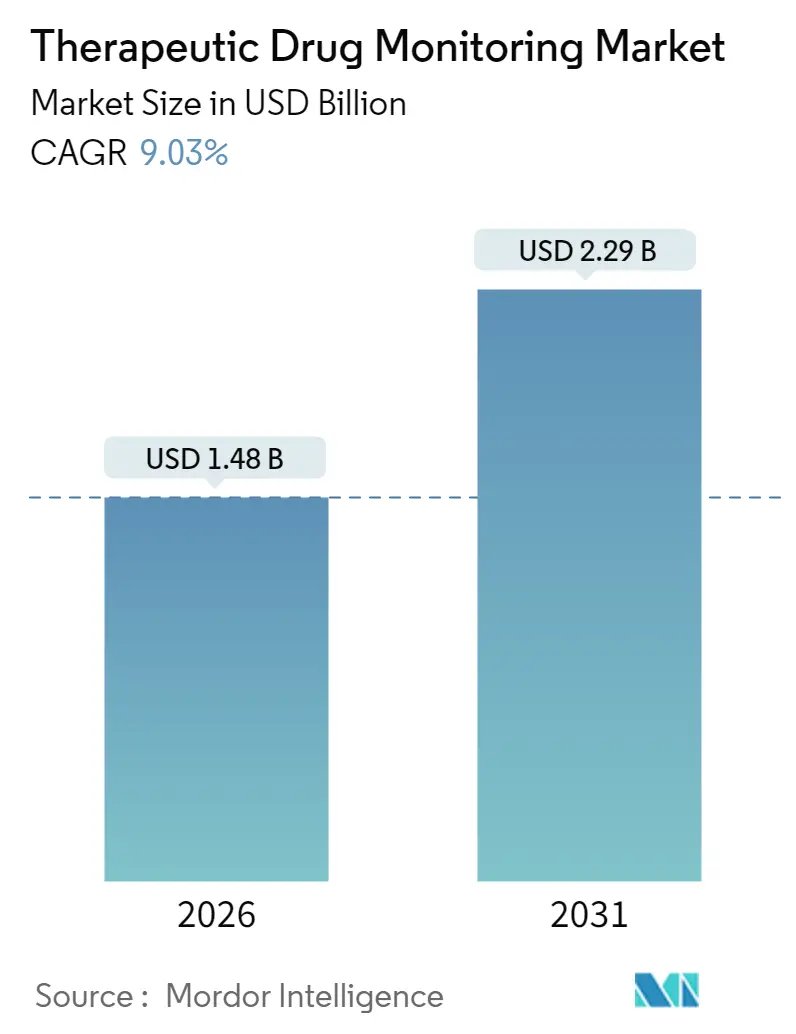
治療薬物モニタリング(TDM)市場は、2025年に13.6億米ドルと評価され、2026年には14.8億米ドルに成長し、予測期間(2026-2031年)中に年平均成長率(CAGR)9.03%で拡大し、2031年までに22.9億米ドルに達すると予測されています。この市場は、技術(免疫測定法、プロテオミクスなど)、薬物クラス(抗不整脈薬、免疫抑制剤など)、エンドユーザー(病院検査室、独立/リファレンス検査室など)、および地域によってセグメント化されています。最も急速に成長する市場はアジア太平洋地域であり、最大の市場は北米です。市場の集中度は中程度とされています。
市場の主要トレンドと洞察
成長を促進する要因:
* がん、HIV、自己免疫疾患、心臓病の有病率上昇(CAGRへの影響: +2.1%): がん治療における小分子キナーゼ阻害剤とモノクローナル抗体の併用療法は、精密な血清レベル管理を必要とします。HIV治療における長時間作用型薬剤は、持続的なトラフ濃度確認が不可欠です。自己免疫疾患では、生物学的疾患修飾薬のクリアランス率が変動するため、TDMは効果喪失の原因特定に役立ちます。高齢化に伴う心血管疾患の増加も、ジゴキシンや抗不整脈薬のモニタリング需要を押し上げています。これらの疾患負担は、市場における検査量の着実な増加を支えています。
* 臨床試験の拡大とコンパニオン診断の義務化(CAGRへの影響: +1.8%): 規制当局は、臨床試験において用量最適化のエビデンスを要求しており、TDMは研究プロトコルに不可欠な要素となっています。LC-MS/MS分析と薬理ゲノムアルゴリズムを統合したワークフローは、適応的用量設定を可能にし、後期段階での脱落を減少させます。分散型臨床試験モデルは、乾燥血液スポットキットの採用を加速させ、データ忠実度を維持しつつ、サイト訪問を最小限に抑えます。
* コアラボにおける自動化とハイスループット免疫測定法の採用(CAGRへの影響: +1.5%): 第4世代のベンチトップアナライザーは、前分析ロボット、マイクロ流体試薬パック、および検査情報システム(LIS)への自動結果転送を統合しています。AIを活用した予測保守により、稼働時間は97%を超え、高容量の施設では1日あたり10,000件以上の検査処理能力を実現しています。これにより、試薬コストの削減と手作業時間の最小化が実現し、利益率が向上しています。
* 遠隔TDMを可能にする低コストの乾燥血液スポットサンプリング(CAGRへの影響: +1.3%): マイクロキャピラリー採血カードは、全血を室温で最大3週間保存でき、冷蔵物流の必要性を排除し、地方への普及を促進します。自己採血は患者の負担を軽減し、モニタリングスケジュールへの遵守を向上させます。東南アジア、ラテンアメリカ、サハラ以南アフリカの公衆衛生プログラムでは、郵送TDMキットが試験的に導入され、ターンアラウンドタイムを短縮しています。
* 薬理ゲノムデータとTDMアルゴリズムの統合(CAGRへの影響: +1.2%): 個別化医療の進展に伴い、薬理ゲノムデータとTDMアルゴリズムの統合は、より精密な薬物投与を可能にします。
* リアルタイム薬物レベル追跡のためのウェアラブル微小流体バイオセンサー(CAGRへの影響: +0.9%): ウェアラブルバイオセンサーは、リアルタイムでの薬物レベル追跡を可能にし、エピソード的な採血から動的な薬物動態プロファイリングへとTDMのパラダイムを再定義する可能性を秘めています。
市場の成長を抑制する要因:
* LC-MS/MSプラットフォームの設備投資とサービス契約費用(CAGRへの影響: -1.4%): エントリーレベルのLC-MS/MSシステムは高価であり、年間保守契約も高額なため、特に低・中所得経済圏の病院や民間ラボの予算を圧迫します。これにより、外部委託検査が継続され、ターンアラウンドタイムが延長され、ルーチン検査の採用が遅れる傾向にあります。
* 新興国における熟練した臨床毒物学者の不足(CAGRへの影響: -0.9%): 自動化が進む一方で、メソッドバリデーション、トラブルシューティング、臨床解釈には専門家の監督が不可欠です。トレーニングパイプラインが技術的複雑さに追いついておらず、高給の製薬業界への人材流出も相まって、新興国では熟練した臨床毒物学者が不足しています。
* TDMパネルの償還コードの断片化(CAGRへの影響: -0.8%): 特に北米やヨーロッパの一部地域では、TDMパネルの償還コードが断片化しており、医療提供者や患者にとって費用負担の予測が困難になることがあります。
* LISと意思決定支援ソフトウェア間のデータ交換のギャップ(CAGRへの影響: -0.6%): 検査情報システム(LIS)と意思決定支援ソフトウェア間のデータ交換のギャップは、TDMデータの効率的な利用を妨げ、臨床意思決定の遅延やエラーにつながる可能性があります。
セグメント別分析
* 技術別: 免疫測定法は2025年に58.74%の収益シェアを占め、最大のセグメントでした。これは、既存の化学分析ラインへの統合、一貫した償還コーディング、および技術者の慣れによって支えられています。しかし、バイオセンサーベースプラットフォームは2031年までに9.74%のCAGRで拡大すると予測されており、電気化学的トランスダクションの進歩に支えられています。質量分析法(LC-MS/MS)は、タンパク質結合干渉や交差反応性の制限がある複雑なレジメンにおいて、三次医療センターで採用が進んでいます。
* 薬物クラス別: 抗てんかん薬は2025年の収益の31.88%を占めました。一方、腫瘍治療薬は2031年までに9.55%のCAGRで急増すると予測されており、市場で最も急速に成長するセグメントです。精密腫瘍学は、最適な腫瘍曝露と全身毒性軽減のために、個別に滴定されたキナーゼ阻害剤の用量を義務付けており、LC-MS/MSマルチプレックスパネルの広範な展開を促進しています。免疫抑制剤、バンコマイシン、アミノグリコシド、精神科薬なども重要な薬物クラスです。
* エンドユーザー別: 病院検査室は2025年にTDM市場シェアの55.05%を占めました。しかし、ポイントオブケア(POC)サイト(外来診療所、透析ユニット、在宅デバイスなど)は、小型アナライザーの普及により10.03%のCAGRで拡大しています。リファレンスラボラトリーは特殊なアッセイ需要を保護し、学術センターは新規バイオマーカーやウェアラブル統合を試験的に導入しています。CRO(医薬品開発業務受託機関)も、サービスポートフォリオを強化しています。
地域別分析
* 北米: 2025年のTDM市場規模の41.80%を占め、確立された償還制度、広範な移植プログラム、および薬理ゲノムのリーダーシップに起因しています。
* ヨーロッパ: 北米と同様の成熟度を示しますが、コスト抑制圧力の下にあります。
* アジア太平洋: 2031年までに10.27%のCAGRを示しており、病院建設ブーム、臨床試験の流入、および国家的な精密医療イニシアチブを反映しています。特に中国は、公共部門のインフラ資金と規制改革により、地域の量的な増加を牽引しています。日本は超高齢化社会の人口動態により高い一人当たりの検査比率を維持し、インドは医療保険制度の拡大により患者アクセスが広がっています。
* 中東および南米: 検査自動化ベンダーが政府機関と提携して診断能力を近代化するにつれて、初期段階ながら加速する採用曲線を示しています。
競合状況
治療薬物モニタリング市場は中程度の集中度を示しています。Abbott、Thermo Fisher、Roche、Siemens Healthineers、Danaherといった主要プレーヤーは、フルラインの診断ポートフォリオと確立されたサービス拠点を活用し、エンドツーエンドのソリューションを提供することで市場での地位を保護しています。中堅企業はニッチなイノベーションに焦点を当てており、Bio-Radはマルチプレックス免疫測定パネルを活用し、スタートアップ企業はクラウドネイティブダッシュボードを展開しています。
過去2年間は戦略的買収が特徴的で、Siemens Healthineersはウェアラブルセンサー開発企業を買収し、Thermo FisherはAIアルゴリズムベンダーを統合しました。デバイスメーカーと製薬会社間のコラボレーションも強化されており、腫瘍薬のスポンサーは独自の分析法を臨床試験プロトコルに組み込んでいます。試薬レンタル契約や成果ベースの価格モデルが普及しつつあり、サイバーセキュリティ層と標準化されたデータ相互運用性に投資するベンダーが、デジタルヘルスエコシステムが成熟するにつれて有利な立場を築くと考えられます。
主要リーダー: Thermo Fisher Scientific、Bio-Rad Laboratories、F. Hoffmann-La Roche Ltd、Danaher Corporation (Beckman Coulter, Inc.)、Siemens Healthcare GmbHなどが挙げられます。
最近の業界動向: 2024年4月にはFerring B.V.が米国でRebyotaとAdstiladrinを発売し、長期的な用量モニタリングの機会を創出しました。2022年1月にはSeerが次世代プロテオミクス研究プラットフォームを発売し、人体内のタンパク質分類に貢献しています。
治療薬物モニタリング(TDM)市場に関する本レポートは、特定の薬剤(治療域が狭いもの)およびその代謝物の血中濃度を定期的に測定し、個々の投与計画の評価を支援する臨床実践に焦点を当てています。この市場は、2026年には14.8億米ドルに達し、2031年には9.03%の年平均成長率(CAGR)で22.9億米ドルに成長すると予測されています。
市場の成長を牽引する主な要因としては、腫瘍学、HIV、自己免疫疾患、心臓病の症例増加、臨床試験の拡大とコンパニオン診断の義務化が挙げられます。また、コアラボにおける自動化およびハイスループット免疫測定法の採用、遠隔TDMを可能にする低コストの乾燥血液スポットサンプリング、薬理ゲノムデータとTDMアルゴリズムの統合、リアルタイムの薬物レベル追跡を可能にするウェアラブルマイクロ流体バイオセンサーの登場も重要な推進力となっています。
一方で、市場の成長を阻害する要因も存在します。LC-MS/MSプラットフォームの高額な設備投資およびサービス契約費用、特に新興国における熟練した臨床毒物学者の不足が挙げられます。さらに、TDMパネルに対する償還コードの断片化や、LIS(検査情報システム)と意思決定支援ソフトウェア間のデータ交換のギャップも課題となっています。
技術別では、免疫測定法が2025年に58.74%の収益シェアを占め、市場を支配しています。これにはELISA、化学発光免疫測定法(CLIA)、蛍光免疫測定法などが含まれます。しかし、バイオセンサーベースおよびウェアラブル技術は9.74%のCAGRで最も急速に成長しているセグメントです。その他、プロテオミクス/LC-MS/MS、クロマトグラフィー(GC、HPLC)なども重要な技術として挙げられます。
薬物クラス別では、抗不整脈薬、抗てんかん薬、免疫抑制剤、抗生物質(例:バンコマイシン、アミノグリコシド)、抗精神病薬および気分安定薬、腫瘍学および標的療法などが主要なセグメントとして分析されています。エンドユーザー別では、病院検査室、独立/リファレンス検査室、学術・研究機関、ポイントオブケア/患者自己検査、受託研究機関(CROラボ)などが含まれます。
地域別では、2025年に北米が最大の市場シェアを占めています。一方、アジア太平洋地域は、政府主導の病院拡張、臨床試験活動の急増、ヘルスケア技術への投資により、2031年までに10.27%のCAGRで最も急速に成長する地域と予測されています。
競争環境においては、Thermo Fisher Scientific、Bio-Rad Laboratories、F. Hoffmann-La Roche Ltd(Roche Diagnostics)、Danaher Corporation(Beckman Coulter)、Siemens Healthineersなどが主要な市場プレイヤーとして挙げられます。これらの企業は、グローバルおよび市場レベルでの概要、主要セグメント、財務情報、戦略的情報、市場ランク/シェア、製品・サービス、最近の動向などに基づいてプロファイルされています。
本レポートは、市場の機会と将来の展望、特に未開拓の領域や満たされていないニーズについても評価しています。TDM市場は、医療技術の進歩と疾患の増加に伴い、今後も着実な成長が見込まれる重要な分野であると言えます。

1. はじめに
- 1.1 調査の前提条件と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
- 4.2 市場の推進要因
- 4.2.1 腫瘍、HIV、自己免疫疾患、心臓病の症例の増加
- 4.2.2 臨床試験とコンパニオン診断の義務化の拡大
- 4.2.3 コアラボにおける自動化とハイスループット免疫測定法の採用
- 4.2.4 低コストの乾燥血液スポットサンプリングによる遠隔TDMの実現
- 4.2.5 薬理ゲノムデータとTDMアルゴリズムの統合
- 4.2.6 リアルタイムの薬物レベル追跡のためのウェアラブルマイクロ流体バイオセンサー
- 4.3 市場の阻害要因
- 4.3.1 LC-MS/MSプラットフォームの設備投資およびサービス契約費用
- 4.3.2 新興国における熟練した臨床毒物学者の不足
- 4.3.3 TDMパネルの償還コードの断片化
- 4.3.4 LISと意思決定支援ソフトウェア間のデータ交換のギャップ
- 4.4 バリュー/サプライチェーン分析
- 4.5 規制環境
- 4.6 技術的展望
- 4.7 ポーターの5つの力分析
- 4.7.1 新規参入の脅威
- 4.7.2 買い手の交渉力
- 4.7.3 供給者の交渉力
- 4.7.4 代替品の脅威
- 4.7.5 競争の激しさ
5. 市場規模と成長予測(金額 – USD百万)
- 5.1 テクノロジー別
- 5.1.1 免疫測定法
- 5.1.1.1 ELISA
- 5.1.1.2 化学発光免疫測定法 (CLIA)
- 5.1.1.3 蛍光およびその他のIAフォーマット
- 5.1.2 プロテオミクス / LC-MS/MS
- 5.1.3 クロマトグラフィー (GC、HPLC)
- 5.1.4 バイオセンサーベースおよびウェアラブル
- 5.1.5 その他のテクノロジー
- 5.2 薬剤クラス別
- 5.2.1 抗不整脈薬
- 5.2.2 抗てんかん薬
- 5.2.3 免疫抑制剤
- 5.2.4 抗生物質 (例: バンコマイシン、アミノグリコシド)
- 5.2.5 抗精神病薬および気分安定薬
- 5.2.6 腫瘍学および標的療法
- 5.2.7 その他の薬剤クラス
- 5.3 エンドユーザー別
- 5.3.1 病院検査室
- 5.3.2 独立系 / 参照検査室
- 5.3.3 学術・研究機関
- 5.3.4 臨床現場 / 患者自己検査
- 5.3.5 受託研究・CROラボ
- 5.4 地域別
- 5.4.1 北米
- 5.4.1.1 米国
- 5.4.1.2 カナダ
- 5.4.1.3 メキシコ
- 5.4.2 ヨーロッパ
- 5.4.2.1 ドイツ
- 5.4.2.2 イギリス
- 5.4.2.3 フランス
- 5.4.2.4 イタリア
- 5.4.2.5 スペイン
- 5.4.2.6 その他のヨーロッパ
- 5.4.3 アジア太平洋
- 5.4.3.1 中国
- 5.4.3.2 日本
- 5.4.3.3 インド
- 5.4.3.4 韓国
- 5.4.3.5 オーストラリア
- 5.4.3.6 その他のアジア太平洋
- 5.4.4 中東
- 5.4.4.1 GCC
- 5.4.4.2 南アフリカ
- 5.4.4.3 その他の中東
- 5.4.5 南米
- 5.4.5.1 ブラジル
- 5.4.5.2 アルゼンチン
- 5.4.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
- 6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要セグメント、財務、戦略情報、市場ランク/シェア、製品・サービス、最近の動向を含む)
- 6.3.1 Abbott Laboratories
- 6.3.2 Thermo Fisher Scientific
- 6.3.3 F. Hoffmann-La Roche Ltd (Roche Diagnostics)
- 6.3.4 Siemens Healthineers
- 6.3.5 Danaher Corp (Beckman Coulter)
- 6.3.6 Bio-Rad Laboratories
- 6.3.7 Chromsystems Instruments & Chemicals
- 6.3.8 Randox Laboratories
- 6.3.9 Alpco Diagnostics
- 6.3.10 ARK Diagnostics
- 6.3.11 DiaSorin S.p.A.
- 6.3.12 bioMérieux SA
- 6.3.13 Tecan Group
- 6.3.14 Waters Corporation
- 6.3.15 Agilent Technologies
- 6.3.16 Hitachi High-Tech Corp.
- 6.3.17 Bruker Corp.
- 6.3.18 JEOL Ltd.
- 6.3.19 Quotient Ltd.
- 6.3.20 LabCorp (Covance Labs)
7. 市場機会と将来展望
*** 本調査レポートに関するお問い合わせ ***

治療薬物モニタリング(Therapeutic Drug Monitoring, TDM)は、患者さんの血液やその他の体液中の薬物濃度を測定し、その結果に基づいて個々の患者さんに最適な薬物投与計画を立案・調整する医療行為でございます。これは、薬物の有効性を最大限に引き出し、副作用のリスクを最小限に抑えることを目的とした、個別化医療の重要な柱の一つです。特に、治療域が狭い薬物においてその重要性が高く、患者さんの年齢、肝機能、腎機能、遺伝的要因などによる薬物動態の個体差を考慮し、科学的根拠に基づいた最適な薬物療法を実現するために不可欠な手法でございます。
TDMには様々なアプローチがございます。測定対象は主に血液(血漿、血清)ですが、唾液や尿も用いられます。検体採取タイミングは、薬物濃度が最も低くなるトラフ値が有効性維持や中毒回避の評価に重要視されますが、ピーク値やランダムな時点での測定も薬物や目的に応じて使い分けられます。分析方法としては、迅速性、自動化、低コストが特徴の免疫測定法(酵素免疫測定法 EIA、蛍光偏光免疫測定法 FPIA、化学発光免疫測定法 CLIAなど)が広く利用されています。一方、高い特異性と感度を持ち、複数の薬物やその代謝物を同時に測定できる液体クロマトグラフィー・タンデム質量分析法(LC-MS/MS)やガスクロマトグラフィー・質量分析法(GC-MS)は、より精密な分析や薬物相互作用の評価に用いられます。近年は、迅速な結果が得られるポイントオブケアテスティング(POCT)デバイスの開発も進み、救急医療や集中治療室などでの活用が期待されております。
TDMの主な用途は多岐にわたります。第一に、抗てんかん薬、免疫抑制剤、抗不整脈薬など治療域が狭い薬物の投与量最適化により、治療効果の最大化と副作用の最小化を図ります。第二に、患者さんの代謝・排泄能力低下による薬物中毒のリスクを早期に検知し、予防と管理を行います。第三に、標準投与量で効果が得られない場合に薬物濃度を確認し、服薬遵守の確認や増量検討に役立て、治療効果を確保します。第四に、患者さんの服薬遵守を確認する手段としても重要です。第五に、複数の薬物併用時の相互作用による薬物濃度変動を評価し、適切な対処を可能にします。小児、高齢者、腎機能・肝機能障害患者、妊婦など、薬物動態が大きく変動しやすい特殊な集団においても、TDMは特に重要な役割を果たします。
TDMを支える関連技術も進化を続けております。LC-MS/MSや自動免疫測定装置といった高性能分析機器は、TDMの精度と効率を向上させました。近年注目されるのは、ファーマコゲノミクス(PGx)との連携です。PGxは遺伝子情報に基づき薬物応答性を予測する学問分野であり、TDMと組み合わせることで、初回投与量の予測から実際の薬物濃度確認まで、より個別化された薬物療法を可能にします。ポピュレーション薬物動態学(PopPK)モデルは、患者集団の薬物動態データを統計的に解析し、個々の患者さんの薬物濃度を予測します。人工知能(AI)や機械学習(ML)も、TDMの分野で活用が進んでおり、大量の患者データから最適な投与量予測アルゴリズムの開発、薬物相互作用の検出、副作用リスクの評価などに貢献が期待されます。デジタルヘルス技術や遠隔医療の進展も、TDMデータの効率的な管理や共有、遠隔モニタリングを可能にし、医療アクセス向上に寄与しています。
TDMの市場背景には重要な動向が見られます。慢性疾患の罹患率増加、高齢化社会の進展、個別化医療への需要の高まりが市場を牽引しています。特に、免疫抑制剤や抗がん剤など、治療域が狭く高価な新薬開発が進むにつれてTDMの必要性は高まり、医療費抑制の観点からもその経済的価値が再評価されています。主要な市場プレイヤーとしては、ロシュ、アボット、シーメンスヘルスケア、サーモフィッシャーサイエンティフィックといった大手診断薬・機器メーカーが挙げられます。一方で、課題も存在します。検査コスト、検査結果が得られるまでの時間(ターンアラウンドタイム)、一部の医療従事者におけるTDMの重要性や適切な実施方法に関する知識不足、そして検査の標準化や保険償還の問題などが挙げられます。特に、迅速な結果が求められる状況では中央検査室での分析では間に合わないことがあり、POCTの普及が待たれます。
将来展望として、TDMはさらなる進化を遂げると予想されます。ファーマコゲノミクスとの統合による真の個別化医療の実現が最も期待され、遺伝子情報と薬物濃度データを組み合わせることで、より精密な投与量設計と治療最適化が図られるでしょう。POCTデバイスのさらなる発展も重要なトレンドであり、より多くの薬物に対応し、精度と利便性を向上させることで、救急医療や外来診療、さらには在宅医療でのTDM普及が期待されます。分析技術の面では、より高感度で多項目同時測定が可能な小型化された分析装置の開発が進むと考えられます。AIや機械学習は、TDMデータの解析、投与量アルゴリズムの最適化、薬物動態モデルの構築において、その役割を拡大していくでしょう。また、非侵襲的なモニタリング技術、例えばウェアラブルセンサーを用いた連続的な薬物濃度測定や、呼気分析など、採血を伴わないTDM手法の研究開発も進められております。適用範囲も従来の低分子化合物だけでなく、バイオ医薬品(抗体医薬など)の治療薬物モニタリング(Therapeutic Protein Monitoring, TPM)への応用も注目されております。最終的には、TDMデータが電子カルテシステムや他の患者データとシームレスに統合され、医療従事者が患者さんの状態を包括的に把握し、より質の高い医療を提供できる未来が期待されます。