小児臨床試験市場規模と展望, 2025-2033

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
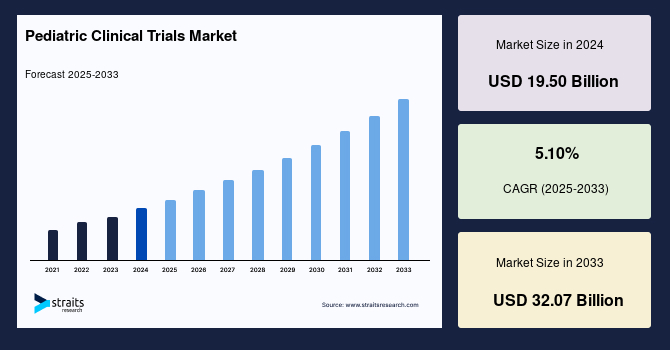
グローバルな小児臨床試験市場は、2024年に195億ドルと評価され、2025年には215.4億ドルから2033年までに320.7億ドルに達すると予測され、予測期間中(2025-2033年)の年平均成長率(CAGR)は5.10%です。小児臨床試験は、子供に影響するさまざまな適応症に対する新薬を市場に投入する唯一の基準であるため、製薬およびバイオテクノロジー業界は社内での臨床研究から契約研究機関(CRO)との契約へとシフトしています。小児集団における未充足の医療ニーズにより、開発の臨床段階に大規模な製品パイプラインが存在します。今後、新薬の強力なパイプラインは製薬業界に大きな利益をもたらすと予想されます。
小児薬に対する意識の高まり、社内での臨床試験からCROへのシフト、小児糖尿病などの小児疾患の増加が、小児臨床試験市場の拡大を促進する主要な要因です。小児薬の重要性が増すにつれ、今後数年間で小児臨床試験市場は安定した成長を示すと予測されています。市場の成長は、はしかやおたふく風邪、結核、風疹などの感染症を治療する新しいワクチンや他の生物学的製品への需要の増加によって推進される可能性があります。世界保健機関(WHO)によると、新生児の約86%が26の病気に対して予防接種を受けている一方で、1,950万人の子供が未接種であり、年間200万から400万人の子供が死亡しています。
米国疾病管理予防センター(CDC)のデータシートによると、米国では0~17歳の子供の約0.6%が現在のてんかんを持っていると推定されています。国際糖尿病連合(IDF)による「Diabetes Atlas 2017」によれば、2019年までに全世界で4億6300万人が糖尿病を患っており、20歳未満(子供と青年)の100万人が1型糖尿病を持っています。世界中の医療機関や研究機関は、小児がんの治療薬の開発に焦点を当てており、それにより小児臨床試験が増加しています。
アメリカ臨床腫瘍学会(ASCO)の2022年2月の報告によれば、2022年末までに米国で15歳未満の子供が推定10,470人がんを診断されると予想されています。世界保健機関によると、1か月から9歳の子供の死因の主な原因は下痢、マラリア、肺炎、敗血症です。これらの疾患の有病率の増加は、新たな治療オプションの探求を促進しています。その結果、市場の成長が促進されると予測されています。
小児臨床試験市場の拡大を阻む要因として、さまざまな理由で終了される小児臨床試験の高い割合が挙げられます。患者不足を含むさまざまな理由で多くの小児臨床試験が失敗に終わっています。他の課題には、行動問題や臨床試験中の試験実施問題が含まれます。これらの問題には、誤った投薬、製剤の困難、情報提供の終了が含まれます。規制問題や薬物毒性も臨床試験中に生じる問題です。
米国食品医薬品局(FDA)のデータによると、小児試験の25%から40%が、小児にとって安全で効果的であることを証明できないために終了され、小児での使用のためのラベル表示された適応症を生み出さないとされています。市場の投資家は、研究開発のために現在開発中の革新的な化合物を用いた小児試験に注力しています。小児患者には重要な未充足の医療ニーズがあり、市場の主要企業はこれらのニーズを満たすために新しい改善された製品の開発に焦点を当てています。さらに、健全な医薬品開発パイプラインが市場の拡大を促進しました。
2018年には、感染症、神経学的問題、遺伝的異常、およびさまざまな形態のがんなど、大きな未充足のニーズを持つ疾患を含む広範な治療分野で1,300以上の産業スポンサーによる小児臨床試験が行われていました。主要市場プレーヤーはまた、有望な分野での製品提供を拡大するために新しいアイテムへのアクセスを得るための買収戦略に焦点を当てています。これらは予測期間中に有利な機会をもたらすでしょう。
グローバルな小児臨床試験市場は、地域によって北アメリカ、ヨーロッパ、アジア太平洋、ラテンアメリカ、中東およびアフリカに分けられます。2021年には北アメリカの市場が最も有利であり、全世界で生成された収入の45%を占める最高のシェアを持っていました。これは、地域内に多くの製薬企業とCROが存在し、積極的に小児試験を実施しているためです。
Report Coverage & Structure
小児臨床試験市場レポートの構造
このレポートは、小児臨床試験市場に関する詳細な分析を提供し、様々なセグメントに分かれて構成されています。それぞれのセクションは市場の異なる側面を掘り下げており、読者が包括的に理解できるように構成されています。
序論
- セグメンテーション: 市場のセグメント化の基礎を説明します。
- 調査方法論: 調査の進め方やデータの収集方法について詳述します。
- 無料サンプル取得: サンプル提供の案内があります。
エグゼクティブサマリー
市場の全体像と主要な発見についての要約が含まれています。
調査の範囲とセグメンテーション
- 調査目的: 調査の目標と意図について記述しています。
- 制約と仮定: 調査における前提条件や制約事項。
- 市場の範囲とセグメンテーション: 分析対象の範囲と具体的なセグメント。
- 考慮した通貨と価格: 分析で使用する通貨とその価格設定の基準。
市場機会の評価
- 新興地域/国: 今後の成長が見込まれる地域や国。
- 新興企業: 注目の新興企業についての情報。
- 新興用途/エンドユース: 新たな適用領域や用途。
市場動向
- ドライバー: 市場を牽引する要因。
- 市場警告要因: 市場に影響を与えるリスク要因。
- 最新のマクロ経済指標: 経済動向の指標。
- 地政学的影響: 地政学的な変化が市場に与える影響。
- 技術要因: 技術の進化が市場に与える影響。
市場評価
- ポーターの5つの力分析: 競争環境の分析。
- バリューチェーン分析: 価値の流れの分析。
規制の枠組み
各地域(北米、ヨーロッパ、APAC、中東とアフリカ、LATAM)の規制環境についての説明があります。
ESGトレンド
環境、社会、ガバナンスに関連するトレンドの分析を含んでいます。
グローバル小児臨床試験市場規模分析
- 市場の導入: 市場の背景と全体像を説明。
- フェーズ別分析: 各フェーズ(フェーズI, II, III, IV)ごとの市場価値分析。
- 研究デザイン別分析: 治療研究や観察研究の市場価値分析。
- 治療領域別分析: 感染症、腫瘍学、免疫疾患、呼吸器疾患、精神疾患などの治療領域ごとの分析。
地域別市場分析
各地域(北米、ヨーロッパ、APAC、中東とアフリカ)の市場概要、フェーズ別、研究デザイン別、治療領域別の詳細な分析が含まれます。特に、北米市場では米国とカナダ、ヨーロッパ市場ではイギリス、ドイツ、フランス、スペイン、イタリア、ロシア、北欧、ベネルクス、およびヨーロッパのその他の地域について詳細に触れています。
*** 本調査レポートに関するお問い合わせ ***

小児臨床試験とは、子供を対象とした医薬品や治療法の有効性と安全性を評価するための臨床試験のことを指します。小児科領域では、成人とは異なる生理学的特性や病態があり、特に成長発達段階における影響を考慮する必要があります。そのため、子供に対する治療法や薬剤の適切な使用を確立するためには、小児特有の臨床試験が不可欠です。
小児臨床試験にはいくつかのタイプがあります。まず、第一相試験では安全性と適正投与量の評価が行われます。第二相試験では、治療法や薬剤の有効性を確認するための初期的な評価が行われます。第三相試験では、より大規模な被験者を対象にして、有効性と安全性の確定的な評価が行われます。さらに、第四相試験は市販後の監視として、新たな副作用の発見や長期使用における影響を評価することを目的としています。
これらの臨床試験の目的は、子供に対して最適な治療を提供するための科学的根拠を確立することです。成人向けのデータをそのまま子供に適用することはできませんので、小児特有のデータが必要です。例えば、用量の調整や投与経路の選択、治療効果の測定方法などが大人と異なる場合があります。
小児臨床試験には、特に倫理的な配慮が求められます。子供は自分で試験への参加を決めることができないため、保護者の同意が不可欠です。また、試験が子供にとって過度な負担とならないように、試験デザインの段階で慎重な検討がなされます。
技術の進展により、小児臨床試験の効率性と安全性も向上しています。例えば、臨床試験のデザインやデータ解析においてAIや機械学習が活用されることがあります。これにより、試験の迅速化や精度の向上が期待されています。また、バイオマーカーの使用やゲノム解析技術の発展により、個々の子供に最適化された治療法の開発が進んでいます。
小児臨床試験は、単に新しい治療法を探るだけでなく、現行の治療法の再評価や、適応の拡大にも貢献します。例えば、新たな適応症の確認や投与方法の改良などが挙げられます。これにより、より多くの子供たちが安全で効果的な治療を受けられることが期待されています。
以上のように、小児臨床試験は医療の質を向上させるための重要な手段であり、子供たちの健康と福祉を支える基盤となっています。倫理的配慮と技術革新を組み合わせることで、今後ますます重要性を増す分野です。