肺がんゲノム検査市場規模と展望、2025-2033年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
## 肺がんゲノム検査市場に関する詳細な市場調査レポート概要
### はじめに:肺がんゲノム検査市場の概観
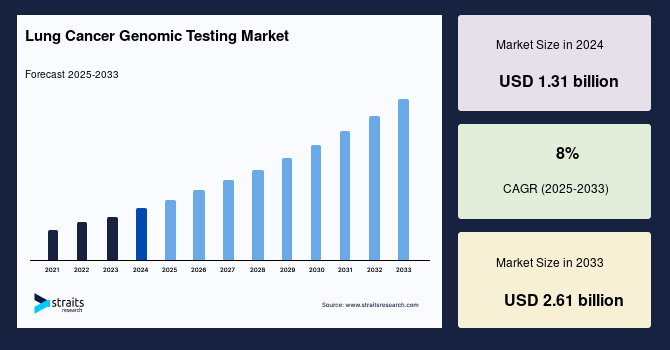
世界の**肺がんゲノム検査**市場は、2024年に13億1,000万米ドルの規模に達しました。この市場は、2025年には14億1,000万米ドルに成長し、予測期間である2025年から2033年にかけて年平均成長率(CAGR)8%で拡大し、2033年には26億1,000万米ドルに達すると予測されています。近年、喫煙の増加や大気汚染の深刻化など、複数の要因により肺がんの罹患率が飛躍的に上昇しており、これが世界の**肺がんゲノム検査**市場を牽引する主要な要因となっています。さらに、検査効率を高めるためのゲノム検査技術の進歩は、世界市場の拡大に新たな機会をもたらすと期待されています。
**肺がんゲノム検査**は、肺がんの遺伝子構成を詳細に分析し、特定の遺伝子変異や異常を検出する技術です。これらの変異は、個別化された治療法の標的となり得るため、治療戦略の策定において極めて重要です。特に非小細胞肺がん(NSCLC)の患者にとって、この検査は、特定の薬剤で標的治療が可能な遺伝子変異を特定する上で不可欠なツールとなります。これにより、より効果的な治療と副作用の軽減が期待できます。
**肺がんゲノム検査**は、通常、肺腫瘍の生検から得られた組織サンプルを用いて実施されます。検査には、EGFR、KRAS、ALKなどの遺伝子を対象とした様々な種類があります。一部の状況では、血液検査(リキッドバイオプシー)によって血流中の腫瘍DNAを検出することも可能です。これらの検査結果は、治療方針の決定、がんの再発予測、そして患者の予後評価に役立ちます。重要なのは、**肺がんゲノム検査**がすべての肺がん患者の診断における標準的な側面ではないという点ですが、NSCLC患者にとっては、標的治療オプションを発見し、患者の転帰を改善するための非常に有用なツールとなり得ます。
### 市場促進要因:肺がん罹患率の急増と精密医療の進展
**肺がんゲノム検査**市場の最も重要な促進要因は、肺がんの罹患率が世界的に急増していることです。世界保健機関(WHO)によると、肺がんは依然として世界中でがん関連死の主要な原因であり、毎年約180万人が肺がんによって命を落としています。この憂慮すべき有病率は、喫煙、環境汚染物質への曝露、職業上のハザード、そして遺伝的素因といった複数の要因に起因しています。
早期発見の重要性に対する意識が高まるにつれて、**肺がんゲノム検査**は肺がんの診断と管理においてますます不可欠なものとなっています。ゲノム検査は、肺がん患者における特定の遺伝子変異や異常を特定することを可能にし、それによって患者の転帰と生存率を改善する標的治療法の開発を促進します。
精密医療の登場は、個々の遺伝子プロファイルに合わせて治療計画を調整するアプローチであり、包括的な**肺がんゲノム検査**の必要性をさらに増幅させています。精密医療は、患者一人ひとりの遺伝的特性に基づいて最適な治療法を選択することで、従来の画一的な治療法では得られなかった高い治療効果と個別化されたケアを提供します。例えば、特定の遺伝子変異を持つ患者には、その変異を標的とする分子標的薬が選択され、これにより不必要な副作用を避けつつ、最大の効果を引き出すことが可能になります。このように、肺がんの世界的な負担が増加し続ける中、高度なゲノム検査技術に対する需要は拡大し、市場の成長を強力に推進しています。
### 市場抑制要因:高コストと限定されたアクセス
**肺がんゲノム検査**の診断および治療における進歩と利点にもかかわらず、これらの技術の高コストと限定されたアクセスは、市場の成長に対する重大な抑制要因となっています。包括的なゲノムプロファイリングや次世代シーケンシング(NGS)技術は、高度な設備と熟練した人材に多大な財政投資を必要とします。
個々のゲノム検査の費用は数百ドルから数千ドルに及ぶことがあり、特に低・中所得国における多くの患者にとっては手の届かないものとなっています。これらの地域では、高度なゲノム検査の広範な実施を支援するために必要な医療インフラが不足していることがしばしば見られます。例えば、専門の検査機器の導入コスト、試薬や消耗品の継続的な費用、そしてバイオインフォマティクス解析を行うための専門家の育成と維持にかかる費用は、医療機関にとって大きな負担となります。さらに、これらの検査に対する保険適用が限定的であるか、あるいは全く存在しないことが多く、患者の自己負担額が高額になる原因となっています。
これらの財政的および物流上の障壁は、**肺がんゲノム検査**の普及を妨げ、より広範な患者集団への利用可能性を制限しています。その結果、多くの地域で肺がんの診断と治療の転帰を改善する上でのゲノム検査の潜在能力が十分に活用されていない状況にあります。医療費の増大は世界的な課題であり、ゲノム検査のような革新的な技術の導入は、その費用対効果と公平なアクセスをどのように両立させるかという点で、政策立案者や医療提供者にとって重要な課題となっています。
### 市場機会:技術革新とAIの活用
技術の進歩、特に次世代シーケンシング(NGS)の登場は、**肺がんゲノム検査**に革命をもたらしました。NGSは、DNAとRNAの包括的な分析を可能にし、変異、遺伝子発現、エピジェネティックな変化を同時に検出することができます。この能力は、EGFR、ALK、KRAS、ROS1、BRAF、NTRK1/2/3、MET、RET、PD-L1など、肺がんにおける複数の遺伝子変異を特定する上で極めて重要であり、標的治療の決定と患者の転帰改善に不可欠な情報を提供します。
2023年の『Journal of Thoracic Oncology』誌の研究では、多様な変異を特定し、個別化された治療を導くNGSの能力により、過去10年間でNGSの採用が著しく増加したことが指摘されています。NGSは、従来の単一遺伝子検査では見落とされがちだった稀な変異や複雑な遺伝子再編成も効率的に検出できるため、治療選択肢を大幅に広げることが可能です。
さらに、メモリアル・スローン・ケタリングがんセンターの研究者たちは、**肺がんゲノム検査**データ分析のためのAI(人工知能)を活用したプラットフォームを導入しました。この革新は、複雑な検査結果の解釈の速度と精度を向上させ、より効率的な治療計画の策定を促進する可能性を秘めています。AIは、膨大なゲノムデータを迅速に処理し、臨床的意義のあるパターンを特定することで、医師の診断支援や治療法の最適化に貢献します。
これらの進歩は、高度なゲノム技術に裏打ちされた精密で個別化された治療法に対する需要の増加によって、世界の**肺がんゲノム検査**市場における成長機会を明確に示しています。医療提供者がこれらの技術を統合し、肺がん治療における診断精度と治療転帰を改善するにつれて、市場はさらなる成長を遂げる態勢が整っています。
### セグメント分析
**1. 製品・サービス別**
* **製品セグメント:** 肺がんの検出と治療におけるゲノム検査の需要増加により、最も大きく成長すると予測されています。これは、肺がんサンプルを検査するために、キットや試薬といった遺伝子検査製品が不可欠であるためです。次世代シーケンシング(NGS)やポリメラーゼ連鎖反応(PCR)などの新しい改良されたゲノム検査技術の登場は、これらの製品への需要をさらに高めています。肺がんの罹患率の急増と個別化された治療オプションへの需要が、遺伝子検査製品市場の拡大を牽引しています。ゲノム検査市場は、NGSキット、PCRキット、そして肺がんサンプル分析に使用される化学薬品など、幅広い製品を包含しています。これらの製品は、遺伝子変異やバイオマーカーの検出に使用され、オーダーメイドの治療計画を策定するために不可欠です。
**2. 技術別**
* **ポリメラーゼ連鎖反応(PCR):** **肺がんゲノム検査**市場において、PCR技術は依然として優位な地位を占めています。PCRが選好される理由は、その低コストと高感度であり、これらは肺がんの原因となる変異を発見する上で極めて重要です。少量のDNAを増幅するPCRの能力は、DNAが少量であるか、あるいは劣化しているサンプルにおいても、肺がんに関連する特定の遺伝子変異を検出するための効果的な方法となっています。PCRは他のゲノム検査方法と比較して、より迅速な結果を提供できます。また、非常に感度が高く、微量の遺伝物質でも特定することが可能です。PCR検査は、通常、他のゲノム検査技術よりも費用が安価であり、より手頃な価格で利用できる利点があります。これらの利点が市場におけるPCRの優位な地位と、**肺がんゲノム検査**における広範な利用につながっています。
* **次世代シーケンシング(NGS):** ゲノム全体や特定の遺伝子パネルを網羅的に解析できるNGSは、多様な遺伝子変異を同時に検出する能力が高く、特に治療標的が多岐にわたるNSCLCにおいて、その重要性が増しています。
* **蛍光in situハイブリダイゼーション(FISH):** 染色体異常や遺伝子再編成の検出に用いられる技術で、特定の遺伝子融合(例:ALK融合遺伝子)の確認に利用されます。
**3. 検体タイプ別**
* **組織生検:** 伝統的に**肺がんゲノム検査**に利用されてきた主要な検体タイプであり、腫瘍細胞を直接的かつ包括的に調査することを可能にします。これにより、腫瘍の正確な病理学的特徴と遺伝子プロファイルを把握することができます。しかし、組織生検は侵襲的な手技であり、患者への負担や合併症のリスクを伴う場合があります。また、腫瘍の部位によっては生検が困難な場合や、腫瘍内の遺伝的異質性を完全に捉えきれない可能性もあります。
* **リキッドバイオプシー:** 近年の技術的進歩により、リキッドバイオプシーが有力な選択肢として浮上しています。リキッドバイオプシーとは、血液中に検出される循環腫瘍細胞(CTC)や循環腫瘍DNA(ctDNA)を検査する非侵襲的なアプローチです。この方法は、アクセスが容易であること、合併症のリスクが低いこと、そしてリアルタイムで疾患の進行を追跡できる機会があることなど、組織生検に比べていくつかの利点があります。例えば、治療効果のモニタリング、薬剤耐性変異の早期検出、手術後の微小残存病変の評価などに活用されています。その結果、リキッドバイオプシーは**肺がんゲノム検査**市場の成長を牽引し、予測期間中に主要な市場シェアを獲得すると予想されています。
**4. パネルタイプ別**
* **マルチ遺伝子パネル:** 複数の遺伝子変異や再編成を同時に検出できる能力から、市場を支配すると予測されています。これは、複数の遺伝子変異が発生する可能性があり、それらを特定することが標的治療オプションの選択に役立つ肺がんにおいて特に不可欠です。例えば、メイヨークリニックの「MayoComplete Lung Cancer-Targeted Gene Panel with Rearrangement, Tumor」のようなマルチ遺伝子パネルは、12の変異と7つの再編成を検出できます。この包括的なアプローチは、患者に予後および治療上のソリューションを提供することができ、個別化医療における重要なツールとなっています。さらに、これらのパネルは、入手が困難な検体に対してより少量の組織を使用することができ、免疫療法に関する推奨のためにマイクロサテライト不安定性(MSI)の状態を提供することも可能です。MSIの検出は、特定の免疫チェックポイント阻害剤に対する反応性を予測する上で重要なバイオマーカーとなります。
* **シングル遺伝子パネル:** 特定の単一遺伝子変異のみを検査するもので、既知の変異が強く疑われる場合や、コストを抑えたい場合に用いられます。
**5. エンドユーザー別**
* **病院・クリニック:** 世界の**肺がんゲノム検査**市場において、病院・クリニックセグメントが優位な地位を占めると予想されています。この優位性は、個別化医療に対する需要の高まりと、病院・クリニックで治療を求める患者数の増加によって推進されています。病院・クリニックは、遺伝子検査を実施するために不可欠な高度なツールとインフラを備えており、患者にとって便利な選択肢を提供します。さらに、肺がんの罹患率の増加と、早期かつ正確な診断の必要性が、これらの施設におけるゲノム検査の需要をさらに高めています。病院・クリニックがゲノム検査を包括的ながんケア計画に統合する能力は、患者の転帰を向上させ、市場におけるそのリーダーシップを強化しています。
* **研究機関:** 新しいバイオマーカーの発見や検査技術の開発を主導し、市場の革新を支えています。
* **診断検査機関:** 専門的なゲノム検査サービスを提供し、病院やクリニックからの検体を受け入れて大規模な分析を行います。
### 地域別分析
**1. 北米**
北米は世界の**肺がんゲノム検査**市場において最大のシェアを占めており、予測期間中に著しい成長を遂げると予測されています。このリーダーシップは、この地域における肺がんの高い罹患率によって推進されており、疾患の原因となる遺伝子異常を特定するためのゲノム検査の需要を大幅に増加させています。北米の高度な医療システムは、最先端の医療施設と新しい技術の迅速な採用を特徴としており、市場の拡大をさらに促進しています。
米国政府や民間団体は、研究開発に多額の投資を行っており、高度なゲノム検査ツールの開発を育成しています。この投資環境は、Thermo Fisher Scientific、Illumina、Qiagenなどの主要な業界プレイヤーの存在によってさらに強化されており、これらすべてが市場の成長に大きく貢献しています。さらに、この地域が個別化医療に強い重点を置いていることと、その利点に対する高い国民意識が、肺がんの診断と治療における**肺がんゲノム検査**の利用増加を推進しています。加えて、国立がん研究所によるがん研究強化の取り組みや、精密医療プログラムの実施などのイニシアティブは、ゲノム検査を通じて肺がん治療を進歩させるというこの地域のコミットメントを明確に示しています。
**2. アジア太平洋**
アジア太平洋地域は、いくつかの主要な要因によって**肺がんゲノム検査**市場において著しい成長を遂げると予測されています。第一に、この地域は、喫煙の増加、環境汚染、人口構造の変化といった要因により、肺がんの負担が増大しています。中国、インド、日本などの国々では、肺がんの症例が顕著に増加しており、ゲノム検査を含む高度な診断および治療ソリューションへの需要が高まっています。
さらに、アジア太平洋地域の各国における医療インフラの改善と医療費の増加は、ゲノム検査を含む高度な医療技術へのアクセスを促進しています。また、がんケアの向上と早期発見の促進を目的とした政府のイニシアティブや医療改革が、市場の成長をさらに推進しています。例えば、中国やインドなどの国々では、がんスクリーニングおよび治療施設の拡大に焦点を当てたプログラムが実施されており、これによりゲノム検査技術の採用が促進されています。
さらに、医療提供者と患者の間で個別化医療の利点に対する意識が高まっていることも、ゲノム検査の採用を促進しています。また、アジア太平洋地域は、大規模で多様な患者集団を抱えており、市場拡大と研究協力のための豊富な機会を提供しています。規制枠組みが進化し、研究開発への投資が継続的に増加するにつれて、アジア太平洋の**肺がんゲノム検査**市場は繁栄し、イノベーションと患者転帰の改善のための新たな道筋を提供すると期待されています。
### 結論
世界の**肺がんゲノム検査**市場は、肺がんの罹患率上昇、精密医療への需要、そしてNGSやAIなどの技術革新によって、今後も力強い成長を続けると予測されます。高コストとアクセス制限という課題は残るものの、リキッドバイオプシーやマルチ遺伝子パネルのような新しいアプローチが市場の機会を拡大しています。特に北米が市場を牽引し、アジア太平洋地域が急速な成長を遂げる中で、病院・クリニックがこの分野における主要な役割を担い続けるでしょう。**肺がんゲノム検査**は、肺がん治療の個別化と患者転帰の改善に不可欠なツールとして、その重要性を増していくと考えられます。
Report Coverage & Structure
“`html
- セグメンテーション
- 調査方法論
- 無料サンプルを入手
- 目次
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制限事項と仮定
- 市場範囲とセグメンテーション
- 考慮された通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場トレンド
- 推進要因
- 市場警告要因
- 最新のマクロ経済指標
- 地政学的な影響
- 技術的要因
- 市場評価
- ポーターの5つの力分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- 欧州
- アジア太平洋
- 中東およびアフリカ
- ラテンアメリカ
- ESGトレンド
- 世界の肺がんゲノム検査市場規模分析
- 世界の肺がんゲノム検査市場の概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- 世界の肺がんゲノム検査市場の概要
- 北米市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- 米国
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- カナダ
- 欧州市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- 英国
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他の欧州
- アジア太平洋市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- 中国
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- 韓国
- 日本
- インド
- オーストラリア
- シンガポール
- 台湾
- 東南アジア
- その他のアジア太平洋
- 中東およびアフリカ市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- アラブ首長国連邦
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他の中東およびアフリカ
- ラテンアメリカ市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- ブラジル
- タイプ別
- 概要
- タイプ別金額
- 製品
- 金額別
- サービス
- 金額別
- 技術別
- 概要
- 技術別金額
- ポリメラーゼ連鎖反応 (PCR)
- 金額別
- 次世代シーケンシング (NGS)
- 金額別
- 蛍光in situハイブリダイゼーション
- 金額別
- サンプルタイプ別
- 概要
- サンプルタイプ別金額
- 組織生検
- 金額別
- 液体生検
- 金額別
- パネルタイプ別
- 概要
- パネルタイプ別金額
- マルチ遺伝子パネル
- 金額別
- シングル遺伝子パネル
- 金額別
- エンドユーザー別
- 概要
- エンドユーザー別金額
- 研究機関
- 金額別
- 病院/クリニック
- 金額別
- 診断ラボ
- 金額別
- タイプ別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のラテンアメリカ
- 競合情勢
- 肺がんゲノム検査市場のプレーヤー別シェア
- M&A契約と提携分析
- 市場プレーヤー評価
- QIAGEN N.V.
- 概要
- 企業情報
- 収益
- 平均販売価格 (ASP)
- SWOT分析
- 最近の動向
- Agilent Technologies, Inc.
- Thermo Fisher Scientific, Inc.
- Quest Diagnostics Incorporated
- Laboratory Corporation of America Holdings
- CENTOGENE N.V.
- BGI
- CeGaT GmbH
- Illumina, Inc.
- Hoffmann-La Roche Ltd.
- Abbott Laboratories
- CD Genomics
- NeoGenomics Laboratories
- Admera Health
- OncoDNA
- OPKO Health, Inc.
- Invitae Corporation
- Veracyte, Inc.
- QIAGEN N.V.
- 調査方法
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次情報の内訳
- 二次および一次調査
- 主要な業界インサイト
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査仮定
- 仮定
- 制限事項
- リスク評価
- 調査データ
- 付録
- 議論ガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
“`
*** 本調査レポートに関するお問い合わせ ***

肺がんゲノム検査とは、肺がん患者様の腫瘍組織や血液などの検体から、がん細胞の遺伝子(ゲノム)変異を網羅的に解析し、その情報に基づいて最適な治療法を選択するための検査です。がんの発生や進行に関わる特定の遺伝子変異を特定することで、患者様一人ひとりの病態に合わせた個別化医療(プレシジョン・メディシン)の実現を目指します。従来の検査では限られた遺伝子のみを調べていましたが、ゲノム検査はより広範囲な遺伝子情報を一度に得られる点が特徴です。
この検査は、特に進行期肺がんの患者様において、分子標的薬や免疫チェックポイント阻害薬といった新しい治療薬の効果を予測し、適切な薬剤選択を行う上で不可欠な情報を提供します。がん細胞が持つ遺伝子変異は、がんの「顔」とも言えるものであり、その変異の種類に応じて効果が期待できる薬剤が異なるため、精密な解析が求められるのです。
ゲノム検査にはいくつかの種類がありますが、代表的なものとして、特定の遺伝子群に焦点を当てた「パネル検査」と、より広範な遺伝子を対象とする「包括的ゲノムプロファイリング(CGP)」が挙げられます。パネル検査は、肺がんにおいて治療標的となりやすいEGFR、ALK、ROS1、BRAF、MET、RET、KRASといった既知のドライバー遺伝子変異を効率的に検出するために開発されました。これらの遺伝子変異は、それぞれに対応する分子標的薬が存在し、その有無が治療方針を大きく左右します。
一方、包括的ゲノムプロファイリング(CGP)は、数百に及ぶ遺伝子のDNAおよびRNAの異常を同時に解析することで、より多くの治療標的候補や、免疫療法の効果予測に役立つ腫瘍遺伝子変異負荷(TMB)やマイクロサテライト不安定性(MSI)といったバイオマーカーの情報を得ることができます。これにより、稀な遺伝子変異を持つ患者様や、既存の治療法が奏効しない患者様に対しても、新たな治療選択肢や臨床試験への参加機会を探る可能性が広がります。
この検査の主な用途は、前述の通り、患者様のゲノム情報に基づいた分子標的薬の選択です。例えば、EGFR遺伝子に変異が見つかればEGFR阻害薬が、ALK融合遺伝子があればALK阻害薬が有効である可能性が高まります。また、TMBが高い場合やMSIが陽性の場合には、免疫チェックポイント阻害薬が奏効しやすいことが知られており、これらの情報も治療戦略を立てる上で極めて重要です。さらに、特定の遺伝子変異が予後と関連していることもあり、治療方針の決定だけでなく、病状の予測にも貢献することがあります。
既存の治療薬では対応できないような、まだ承認されていない稀な遺伝子変異が見つかった場合でも、その変異を標的とする治験薬の臨床試験への参加を検討するきっかけとなることがあります。将来的には、治療効果のモニタリングや再発の早期発見のために、定期的にゲノム検査を実施する可能性も考えられており、その応用範囲は広がりつつあります。
肺がんゲノム検査を支える主要な技術は、次世代シーケンサー(NGS)です。NGSは、一度に大量のDNAやRNA配列を高速かつ低コストで読み取ることができるため、数百もの遺伝子を同時に解析する包括的ゲノムプロファイリングを可能にしました。検体としては、主に腫瘍組織が用いられ、これは手術で切除された組織や、気管支鏡検査、針生検などで採取された組織が病理学的検査を経て提供されます。
近年では、血液中にごく微量に存在するがん由来のDNA断片(循環腫瘍DNA、ctDNA)を解析する「リキッドバイオプシー(液体生検)」も実用化が進んでいます。これは、組織採取が困難な場合や、患者様への負担を軽減したい場合に有効な手段であり、繰り返し検査を行うことで治療効果のモニタリングにも応用が期待されています。得られた膨大なゲノムデータは、バイオインフォマティクスと呼ばれる情報科学技術を用いて解析され、臨床的に意味のある情報へと変換されます。
最終的に、解析されたゲノム情報は、腫瘍内科医、呼吸器内科医、病理医、ゲノム医療専門医、薬剤師、臨床検査技師などの多職種で構成される「エキスパートパネル」または「分子腫瘍ボード(MTB)」と呼ばれる会議で慎重に検討されます。この会議では、患者様の病状、ゲノム解析結果、既存の治療選択肢、治験情報などを総合的に評価し、個々の患者様にとって最も適切と考えられる治療方針が決定されます。このように、肺がんゲノム検査は、先端技術と多分野の専門知識が結集して行われる、高度な医療実践の一部なのです。