臨床試験市場規模と展望、2025年~2033年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
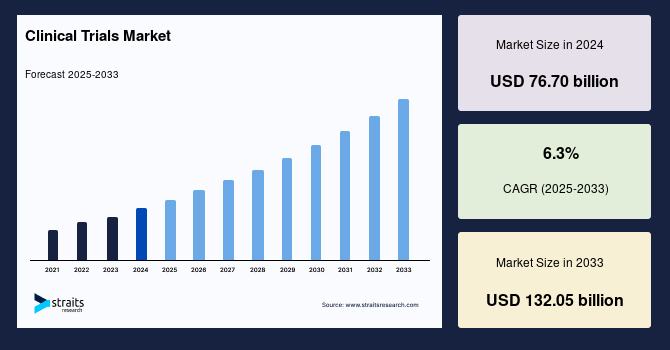
世界の**臨床試験**市場は、2024年に767億米ドルと評価され、2025年には807.1億米ドルに成長し、2033年までに1,320.5億米ドルに達すると予測されています。予測期間(2025年~2033年)における年平均成長率(CAGR)は6.3%と見込まれており、その成長は堅調です。
**市場概要**
**臨床試験**とは、新しい医薬品、治療法、医療機器などの医療介入がヒトに対してどの程度有効であるか、そして安全であるかを評価するために綿密に設計された研究です。これらは、治療法が広く利用される前に、その安全性と有効性を確立するために不可欠なプロセスです。**臨床試験**は、それぞれが独自の目的を持つ複数の段階(フェーズ)に分かれて実施されます。
* **第I相試験**: 主に安全性に焦点を当て、少数の健康なボランティアまたは特定の疾患を持つ患者に対して新しい治療法を試験し、副作用の評価と適切な投与量の決定を目指します。この段階は、治療法がヒトに対して安全であるかどうかの初期評価を行う上で極めて重要です。
* **第II相試験**: 治療法の有効性を評価するとともに、引き続き安全性を監視します。より多くの患者集団を対象とし、疾患に対する治療効果の予備的な兆候を探り、最適な投与量や投与スケジュールをさらに検討します。
* **第III相試験**: 新しい治療法を既存の標準治療と比較し、大規模な患者集団を対象とします。この段階で得られるデータは、規制当局による承認取得のために不可欠であり、治療法の有効性と安全性に関する包括的な情報を提供します。
* **第IV相試験**: 治療法が承認され、市販された後に実施されます。長期的な効果や稀な副作用の監視、特定の患者集団における有効性の評価など、実臨床での治療法の性能を継続的に評価することを目的とします。
**臨床試験**は、参加者の安全と科学的正確性を確保するために、厳格なプロトコルに従って実施され、規制当局によって厳重に監督されます。これらの研究は、特定の適格基準を満たす個人の自発的な参加に依存しており、多くの場合、参加者は最先端の治療法にアクセスする機会を得ることができます。
**臨床試験**市場の拡大を推進する主要な要因は、慢性疾患や複雑な疾患に対する世界的なヘルスケアニーズの急増、そして個別化医療および精密医療への注力です。さらに、分散型**臨床試験**(DCT)の導入や患者中心の試験デザインへの移行も、市場の成長を加速させています。新興市場におけるヘルスケアインフラの拡大、合理化された試験プロセスを目的とした規制改革、そしてAIやビッグデータ分析などの先進技術の採用も、市場の効率性とスケーラビリティを向上させ、成長に貢献しています。
**成長要因(ドライバー)**
1. **世界的なヘルスケアニーズの急増**: 世界中で慢性疾患(糖尿病、心血管疾患、自己免疫疾患など)や複雑な疾患(癌、神経変性疾患など)の罹患率が増加しています。これには、高齢化社会の進展、生活習慣病の蔓延、そして診断技術の進歩が寄与しています。これらの疾患に対する未充足の医療ニーズは非常に高く、新たな治療法や診断法の開発を加速させる必要性が高まっています。その結果、製薬・バイオテクノロジー企業は、研究開発パイプラインを拡大し、これらのニーズに応えるための**臨床試験**を積極的に推進しています。この根本的な需要が、**臨床試験**市場全体の成長を強力に後押ししています。
2. **個別化医療および精密医療への注力**: ゲノム研究の進展とバイオマーカーの発見により、患者個人の遺伝的特徴や病態に合わせて最適化された治療法を提供する個別化医療および精密医療への関心が高まっています。このアプローチは、治療効果の最大化と副作用の最小化を目指します。個別化医療の開発は、特定の遺伝子変異やバイオマーカーを持つ患者集団を対象とした、よりターゲットを絞った**臨床試験**の実施を必要とします。これにより、従来の「ワンサイズ・フィット・オール」型のアプローチとは異なる、高度に専門化された**臨床試験**の需要が生まれており、市場の多様化と成長を促進しています。
3. **分散型**臨床試験**(DCT)の台頭**: DCTは、従来の施設ベースの**臨床試験**の枠を超え、遠隔医療、ウェアラブルデバイス、モバイルアプリ、電子同意(eConsent)などのデジタル技術を活用して、患者が自宅や地域社会で試験に参加できるようにする革新的なアプローチです。このモデルは、**臨床試験**へのアクセスを劇的に改善し、地理的な障壁を取り除きます。
* **利点**: 患者の負担軽減、被験者募集の加速、試験参加者の多様性の確保、脱落率の低減、試験期間の短縮、データ収集の効率化といった多大なメリットをもたらします。例えば、ファイザー社がアトピー性皮膚炎のために実施した完全バーチャル**臨床試験**では、モバイル技術を活用して遠隔での患者モニタリングとバーチャル診察を可能にし、DCTアプローチを通じてアクセシビリティと効率性を大幅に向上させました。このように、DCTは**臨床試験**のプロセスを合理化し、患者の維持率を高めることで、**臨床研究**をより効率的かつ包括的なものに変革しています。
4. **患者中心の試験デザイン**: 患者中心の**臨床試験**デザインは、試験プロセス全体を通じて参加者のニーズ、好み、幸福を最優先するアプローチです。この設計思想は、患者の視点を試験計画の初期段階から取り入れることで、参加者の負担を軽減し、エンゲージメントを高めることを目指します。
* **具体的なアプローチ**: 柔軟なプロトコル、個別化されたケアプラン、コミュニケーションを強化するための技術の活用などが含まれます。例えば、ヤンセン社の「**臨床試験**における患者の声」プログラムは、患者を試験デザインプロセスに積極的に巻き込み、彼らの意見を取り入れることで、プロトコルを改善し、患者エンゲージメントを高め、試験が彼らのニーズにより良く合致するようにしています。これにより、参加者の経験が向上し、より良いエンゲージメントが促進され、最終的に**臨床試験**の結果の質が高まることが期待されます。
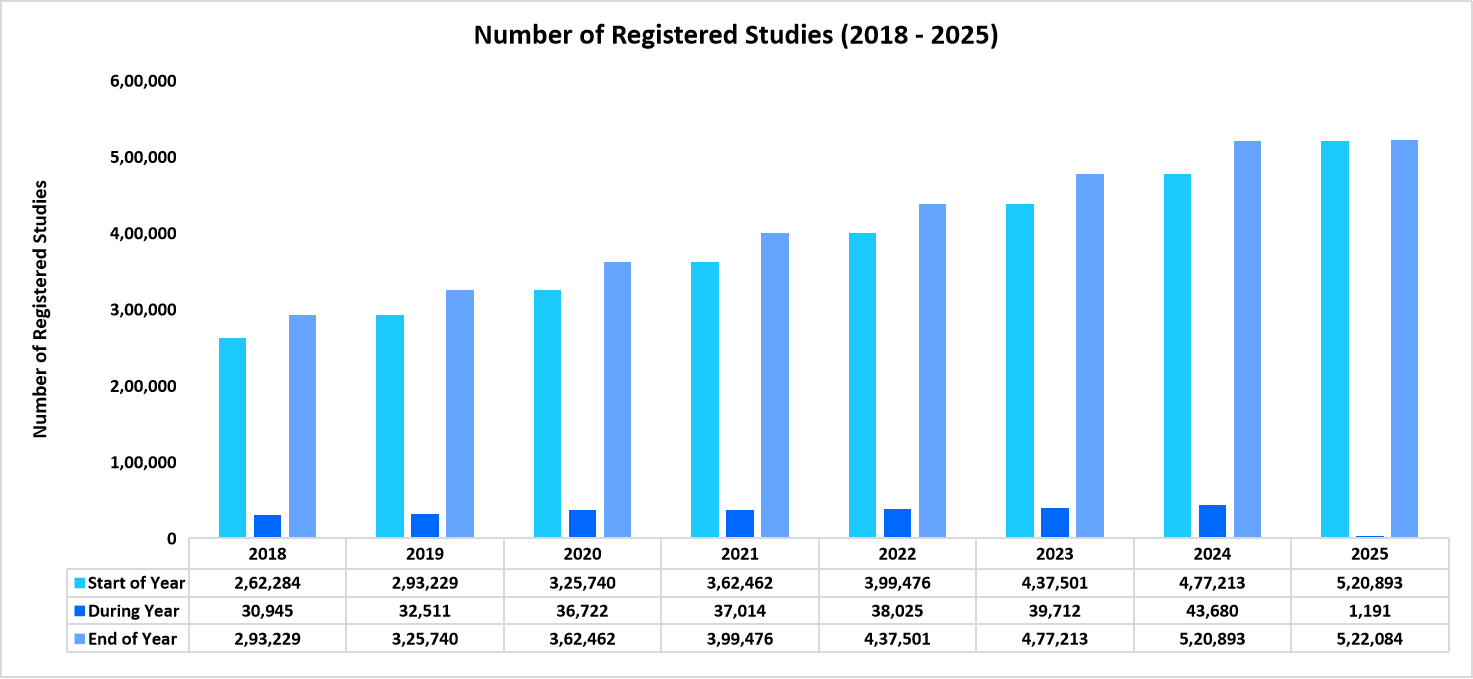
5. **臨床試験数の増加**: 新規治療法や治療薬に対する世界的な需要の高まりを背景に、**臨床試験**の実施数は一貫して増加傾向にあります。製薬およびバイオテクノロジー企業は、未充足の医療ニーズに対応するため、広範な治療領域で研究開発パイプラインを拡大しており、これが**臨床試験**活動の急増につながっています。ClinicalTrials.govのデータによると、2018年から2025年(現在まで)にかけて登録された**臨床試験**数は8.18%の成長を示しています。この上向きのトレンドは、革新的な治療法への需要、技術の進歩、および様々な治療領域における研究イニシアチブの拡大によって推進されており、結果として**臨床試験**市場の成長に大きく貢献しています。
6. **臨床試験のグローバル化**: **臨床試験**のグローバル化は、多様な患者集団へのアクセスを可能にし、被験者募集の課題を軽減し、コストを削減することで市場拡大を推進しています。国際的な共同研究は、試験期間を短縮し、多国籍企業間の協力を促進することで、規制当局による承認を加速させ、新しい治療法の市場アクセスを広げます。
* **WHOのデータ**: 2024年6月にWHOが発表したデータによると、西太平洋地域で登録された**臨床試験**数(23,250件)は、アフリカ地域(845件)の約14倍でした。この格差は、中国における試験登録数の大幅な増加に大きく起因しており、中国の学術雑誌、政府系資金提供機関、大学、病院が試験登録を義務付けていることが背景にあります。このように、**臨床試験**のグローバル化は、患者アクセスの拡大、コスト削減、国際協力の促進を通じて、医薬品開発の加速に寄与し、市場の成長を推進しています。
**阻害要因(リストレイント)**
1. **被験者募集と維持の課題**: **臨床試験**業界において、被験者の募集と維持は依然として極めて重要な課題であり、医薬品開発の速度と成功を著しく妨げています。参加者の不足や高い脱落率は、試験期間を混乱させ、データの完全性を損ない、コストを増加させます。
* **データ**: Emmes Company, LLCのホワイトペーパー(2023年9月)によると、85%以上の**臨床試験**が、試験完了まで十分な参加者を維持できていません。同様に、Md Groupの記事(2020年10月)では、患者の約30%が、経済的負担、時間的制約、試験内容の理解不足やエンゲージメントの欠如、長距離移動、ストレス、不安、家族の都合といった理由により、試験を完了する前に脱落していると報告されています。
* **影響**: これらの脱落は、試験の遅延、重要なデータの損失、そして代替被験者を募集するための財政的負担につながります。MJH Life Sciencesが指摘するように(2023年4月)、失われた参加者1人を補充するための平均コストは19,533ドルにも上り、募集プロセスにさらなる負担をかけています。これらの課題に対処することは、**臨床試験**の効率性、費用対効果、成功率を高める上で不可欠です。改善された患者エンゲージメント戦略、経済的支援、柔軟なスケジュール設定などが、これらの問題を緩和するのに役立つでしょう。
2. **地域間の規制の違い**: 世界中で**臨床試験**がグローバル化するにつれて、各国・地域の規制当局が定める異なる要件、承認プロセス、倫理基準は、企業にとって複雑なコンプライアンス上の課題となっています。これらの規制の違いは、試験のデザイン、実施、データ提出、そして最終的な承認取得において、多大な時間とリソースを要する可能性があります。企業は、各国の特定の規制環境を詳細に理解し、それに対応するための専門知識と戦略を必要とします。この複雑な規制環境のナビゲートは、**臨床試験**の遅延を引き起こし、開発コストを増加させる主要な阻害要因となっています。
**機会(オポチュニティ)**
1. **医薬品開発業務受託機関(CRO)の存在感の高まり**: CROは、**臨床試験**業界に変革をもたらす機会を提供し、業務の合理化、コスト削減、医薬品開発期間の短縮に貢献しています。CROは、規制遵守、被験者募集、データ管理、試験実施などにおいて専門的な知識と経験を有しており、これにより製薬企業は研究とイノベーションに専念することができます。
* **CROの貢献**: CROのグローバルなネットワークと専門性を活用することで、製薬企業は患者アクセスを向上させ、試験効率を高め、イノベーションを促進することができます。この協力関係は、新しい治療法の市場投入を加速させ、すべてのステークホルダーにとってWin-Winのシナリオを生み出しています。CROは、特に複雑化する**臨床試験**において、その専門性と効率性で不可欠なパートナーとしての地位を確立しており、市場の成長をさらに後押しする強力な機会となっています。
2. **新興市場におけるヘルスケアインフラの拡大**: アジア太平洋地域やラテンアメリカなどの新興市場では、ヘルスケアインフラへの投資が活発化しており、医療機関の近代化と医療アクセスの改善が進んでいます。これにより、これらの地域は新たな**臨床試験**の実施拠点として魅力的な選択肢となっています。広範で多様な患者プールへのアクセス、比較的低い運用コスト、政府による研究開発支援策などが、グローバルな**臨床試験**の誘致を促進し、市場全体の成長機会を創出しています。
3. **試験プロセスを合理化するための規制改革**: 各国の規制当局は、医薬品開発の迅速化と効率化を目指し、**臨床試験**の承認プロセスや実施要件を合理化するための改革を進めています。例えば、ファストトラック承認制度の導入や、デジタル技術を活用したデータ提出の簡素化などが挙げられます。これらの規制改革は、企業が新薬をより迅速に市場に投入することを可能にし、開発にかかる時間とコストを削減することで、**臨床試験**市場全体の成長を促進する重要な機会となります。
4. **AIおよびビッグデータ分析などの先進技術の採用**: 人工知能(AI)とビッグデータ分析の技術は、**臨床試験**業界に革命的な変化をもたらしています。これらの技術は、被験者選択の最適化、試験デザインの改善、データ分析の高速化、安全性監視の強化など、多岐にわたる分野で活用されています。
* **具体的な応用**: AIは、大量の医療データから潜在的な被験者を特定し、試験の適合性を予測することで、募集プロセスを効率化します。また、ビッグデータ分析は、複雑な**臨床試験**データから新たな洞察を抽出し、迅速な意思決定を支援します。これらの技術の導入は、**臨床試験**の効率性を大幅に向上させ、コストを削減し、グローバルな規模でのスケーラビリティを高めることで、市場のさらなる発展に貢献する大きな機会を提供します。
**セグメント分析**
**1. 地域別分析**
* **北米**: 世界の**臨床試験**市場において最大の収益シェア(37.60%)を占めています。この支配的な地位は、先進的なヘルスケアインフラ、研究開発への多額の投資、主要な製薬およびバイオテクノロジー企業の存在によって推進されています。さらに、支援的な規制枠組み、多様な患者プール、および試験管理のための最先端技術の広範な採用が、この地域をグローバルな革新的**臨床研究**および加速された医薬品開発のハブとして確立しています。高度な医療技術と豊富な資金が、複雑で大規模な**臨床試験**の実施を可能にしています。
* **アジア太平洋**: 予測期間中に最も速いCAGRを示すと予想されています。この成長は、急速に発展するヘルスケアセクター、**臨床研究**への投資増加、そして増大する患者人口によって牽引されています。中国、日本、インドなどの国々は、規制環境の改善と費用対効果の高い運営において極めて重要な役割を果たしており、世界中の**臨床試験**を惹きつけています。インフラの強化と革新的な治療法への需要の高まりが、アジア太平洋地域を**臨床試験**業界における主要な成長ドライバーとして位置づけています。特に、大規模な患者プールとコスト優位性が、グローバル企業にとって魅力的な要素となっています。
**2. フェーズ別分析**
* **第III相試験**: グローバル市場をリードしています。これは、大規模な患者参加と、新しい治療法の安全性および有効性を最終的に確認する上での極めて重要な役割に起因しています。この段階で生成される包括的なデータは、規制当局による承認取得のために必須であり、医薬品開発の成功にとって決定的な重要性を持ちます。第III相試験に関連する高額なコストと多大なリソースは、治療の信頼性を確保し、公衆衛生のニーズに効果的に対応する上でのその重要性をさらに強調しています。
**3. 治療領域別分析**
* **腫瘍学**: 世界の**臨床試験**市場を支配しています。癌の罹患率の増加と、革新的な治療法への緊急ニーズがその主要な要因です。癌研究と医薬品開発への多額の投資、そして標的療法や免疫腫瘍学における進歩が、この分野での**臨床試験**を加速させています。効果的な癌治療ソリューションに対する高い需要が、このセグメントの優位性を強化しており、差し迫った世界的な健康課題に対処する上でのその重要な役割を浮き彫りにしています。
**4. 試験デザイン別分析**
* **介入試験**: 市場をリードしています。これは、管理された条件下で治療の有効性と安全性を評価するための広範な採用によるものです。これらの試験は、規制当局の承認に必要な堅牢なデータを生成するために不可欠です。介入研究の構造化されたアプローチは一貫性を確保し、研究者が治療効果をより正確に評価することを可能にします。医薬品開発の基盤として、このセグメントはイノベーションを推進し、新しい医療介入の信頼性を高めています。
**5. サービスタイプ別分析**
* **臨床試験データ管理サービス**: 市場を支配しています。これは、**臨床データ**の正確性、完全性、およびセキュリティを確保する上でのその重要な役割に起因しています。**臨床試験**がますます複雑になるにつれて、効果的なデータ管理は業務を合理化し、規制基準への準拠を確保し、リアルタイムの洞察を提供します。膨大なデータセットの効率的な処理を可能にすることで、これらのサービスは迅速な意思決定を支援し、試験結果を向上させるため、現代の**臨床研究**において不可欠なものとなっています。
**競合状況**
市場の主要プレイヤーは、サービス提供の強化、地理的プレゼンスの拡大、競争力の強化を目的として、戦略的な協業、買収、パートナーシップを積極的に追求しています。企業は、CRO(医薬品開発業務受託機関)、学術機関、バイオテクノロジー企業との提携を活用し、業務を合理化し、医薬品開発期間を加速させています。
その中でも、Clinipaceは、現在はCaidyaとしてリブランドされていますが、次世代治療法の進歩に対する革新的なアプローチで認識されている**臨床試験**業界の新興リーダーです。同社は特に、癌に対する免疫応答を高めるための新しいチェックポイント経路を標的とする、最先端のLAG-3免疫療法で知られています。この画期的なアプローチは、Caidyaを腫瘍学研究、特に急速に進化する免疫腫瘍学分野における重要な貢献者として位置づけています。
**アナリストの見解**
アナリストによると、世界の**臨床試験**市場は、慢性疾患の罹患率の増加、バイオテクノロジーの進歩、個別化医療および革新的な治療法への需要の高まりによって力強い成長を遂げています。新興市場におけるヘルスケアインフラの拡大と、試験プロセスを合理化するように設計された規制改革も、市場の発展をさらに加速させています。
さらに、AIやビッグデータ分析などの先進技術の採用は、業界を変革し、試験効率を高め、コストを削減し、**臨床試験**を世界中でよりスケーラブルなものにしています。
しかしながら、課題も依然として残っています。特に被験者の募集と維持においては、高い脱落率や多様な患者集団へのアクセスの制限が、試験期間に影響を与え、コストを増加させています。地域間の規制の違いも、企業が複雑なコンプライアンス環境をナビゲートすることを要求し、大きな障害となっています。市場の成長と成功を維持するためには、これらの課題を克服することが不可欠であると結論付けられています。
Report Coverage & Structure
“`html
- セグメンテーション
- 調査方法
- 無料サンプルを入手
-
目次
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制限事項と前提条件
- 市場範囲とセグメンテーション
- 考慮される通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場トレンド
- 推進要因
- 市場警戒要因
- 最新のマクロ経済指標
- 地政学的影響
- 技術的要因
- 市場評価
- ポーターの5つの力分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- 欧州
- アジア太平洋
- 中東およびアフリカ
- ラテンアメリカ
- ESGトレンド
- 世界の臨床試験市場規模分析
- 世界の臨床試験市場概要
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- 北米市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- 米国
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- カナダ
- 欧州市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- 英国
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他の欧州
- アジア太平洋市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- 中国
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- 韓国
- 日本
- インド
- オーストラリア
- シンガポール
- 台湾
- 東南アジア
- その他のアジア太平洋
- 中東およびアフリカ市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- アラブ首長国連邦
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他のMEA
- ラテンアメリカ市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- ブラジル
- フェーズ別
- はじめに
- フェーズ別(金額)
- フェーズ I
- 金額別
- フェーズ II
- 金額別
- フェーズ III
- 金額別
- フェーズ IV
- 金額別
- 治療領域別
- はじめに
- 治療領域別(金額)
- 感染症
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 代謝性疾患
- 金額別
- 心血管疾患
- 金額別
- その他
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別(金額)
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス
- 金額別
- サービスタイプ別
- はじめに
- サービスタイプ別(金額)
- プロトコル設計
- 金額別
- 施設特定
- 金額別
- 被験者募集
- 金額別
- 検査サービス
- 金額別
- 臨床試験データ管理サービス
- 金額別
- その他
- 金額別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のラテンアメリカ
- 競合状況
- 臨床試験市場のプレイヤー別シェア
- M&A契約と提携分析
- 市場プレイヤー評価
- Pharmaceutical Product Development, INC. (Thermo Fisher Scientific, Inc.)
- 概要
- 事業情報
- 収益
- 平均販売価格
- SWOT分析
- 最近の動向
- ICON plc
- Charles River Laboratories International, Inc.
- IQVIA
- SYNEOS HEALTH
- SGS SA
- PAREXEL International Corporation
- Wuxi AppTec, Inc
- Chiltern International Ltd (Laboratory Corporation of America)
- Eli Lilly and Company
- Novo Nordisk A/S
- Pfizer
- Clinipace (Caidya)
- Medpace
- Frontage Labs
- 調査方法
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次情報の内訳
- 二次および一次調査
- 主要な業界インサイト
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査の前提条件
- 前提条件
- 制限事項
- リスク評価
- 付録
- 議論ガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
“`
*** 本調査レポートに関するお問い合わせ ***

臨床試験は、新しい医薬品、医療機器、治療法、診断法などがヒトに対して安全かつ有効であるかを科学的に評価する研究です。その利益がリスクを上回ることを確認するため、厳格な倫理的・科学的基準に基づき実施されます。被験者の人権と安全を最優先し、安全で効果的な医療を提供し、人々の健康と福祉を向上させることを目的としております。
臨床試験は複数のフェーズに分かれて進行します。フェーズI試験では、少数の健康な成人を対象に、医薬品の安全性や体内動態を評価し、用量を探索します。次にフェーズII試験では、対象疾患を持つ患者さんに対し有効性の兆候と安全性評価を行い、最適な用量や投与方法を検討します。そして最終段階のフェーズIII試験は、大規模な患者集団を対象に、既存の標準治療と比較しながら有効性と安全性を最終的に確認する重要な試験です。ここで良好な結果が得られれば、製造販売承認申請へと進みます。
承認後のフェーズIV試験は市販後調査とも呼ばれ、より多くの患者さんにおける長期的な安全性や稀な副作用、新たな適応症の可能性などを評価します。これら主要フェーズの他に、早期段階で特定の仮説を検証する探索的臨床試験や、医師や研究者が自ら計画・実施する医師主導治験も存在します。医師主導治験は、未承認薬の適応拡大や希少疾患治療の開発など、多様なニーズに応える役割を担っております。
臨床試験の用途は、新薬や医療機器の承認取得に留まらず、既存治療法の改善、病気の予防法や診断法の開発、さらには公衆衛生政策の策定にも貢献します。例えば、ワクチンの有効性や安全性を評価する臨床試験は感染症対策に極めて重要です。また、手術手技やリハビリテーションプログラムなど、非薬物的な介入の効果検証にも用いられ、患者さんの生活の質の向上に貢献しております。
臨床試験を支える技術も進化しています。膨大なデータを正確かつ効率的に収集・管理するためには電子データ収集システム(EDC)が不可欠であり、データ入力の自動化やリアルタイムモニタリングを可能にします。収集データの信頼性を統計学的に評価する高度な統計解析ソフトウェアも欠かせません。さらに、バイオマーカー技術の進展は疾患の早期診断や治療効果予測、個別化医療の実現に寄与し、ゲノム解析技術は患者さんの遺伝子情報に基づいた治療法の開発を後押ししております。
近年では、人工知能(AI)や機械学習が臨床試験の様々な側面に導入されています。AIは適切な被験者の特定、データ解析、創薬プロセスにおける候補物質選定を加速させることが期待されます。ウェアラブルデバイスやセンサー技術は、被験者の活動量、心拍数、睡眠パターンなどのリアルタイムデータを非侵襲的に収集し、より包括的な評価を可能としました。また、分散型臨床試験(DCT)という概念も注目され、遠隔医療技術や電子同意(eConsent)を活用し、被験者の負担軽減と試験参加の促進を図るものです。これらの技術革新は、臨床試験の効率性、アクセシビリティ、そして質を飛躍的に向上させる可能性を秘めております。