バイオ医薬品発酵システム市場規模と展望、2024-2032年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
## バイオ医薬品発酵システム市場に関する詳細な概要
### 1. 市場概要と規模
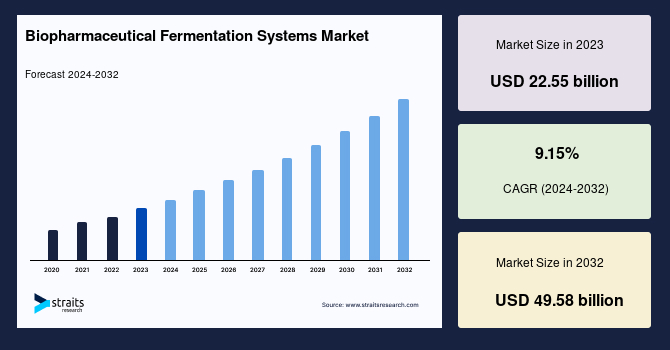
世界の**バイオ医薬品発酵システム**市場は、2023年に225.5億米ドルと評価されました。この市場は、2032年までに495.8億米ドルに達すると予測されており、予測期間(2024年~2032年)中に年平均成長率(CAGR)9.15%という堅調な成長が見込まれています。近年、癌、糖尿病、自己免疫疾患といった慢性疾患の発生率が増加しており、これらの疾患の治療に用いられるバイオ医薬品、特に生物学的製剤に対する需要が高まっています。この傾向が、世界の**バイオ医薬品発酵システム**市場を強力に牽引しています。さらに、シングルユースバイオリアクター、灌流システム、自動制御システムといった発酵技術の継続的な進歩は、バイオ医薬品生産の効率性、拡張性、柔軟性を大幅に向上させており、市場成長のための新たな機会を創出しています。
**バイオ医薬品発酵システム**とは、微生物または細胞ベースのプロセスを通じて治療用タンパク質、酵素、抗体、その他のバイオ医薬品を生産するための、高度なバイオテクノロジー設備を指します。これらのシステムは通常、遺伝子組換えされた微生物や哺乳類細胞を、厳密に制御された条件下でバイオリアクター内で培養します。このプロセスでは、生きた細胞が栄養豊富な環境で代謝プロセスを経て、望ましい治療用化合物を合成する発酵が行われます。発酵プロセスは、接種、成長、誘導、収穫といった複数の段階で構成されます。細胞の成長と製品収量を最適化するためには、温度、pH、酸素レベル、栄養供給といった要因を精密に制御することが不可欠です。**バイオ医薬品発酵システム**は、高純度かつ一貫性のある複雑な生物学的製剤の拡張可能な生産を可能にすることで、製薬業界において極めて重要な役割を果たしており、様々な疾患に対する医療治療の進歩と新たな治療法の開発に大きく貢献しています。
### 2. 市場促進要因 (Drivers)
**バイオ医薬品に対する需要の高まり**が、**バイオ医薬品発酵システム**市場における最も重要な促進要因の一つです。モノクローナル抗体、組換えタンパク質、ワクチンといった生物学的製剤は、多種多様な疾患に対して、標的型かつ個別化された治療選択肢を提供します。この需要は、慢性疾患の有病率の増加と、医療分野における精密医療への移行によってさらに加速されています。世界保健機関(WHO)の報告によると、慢性疾患は年間4100万人の死因となっており、これは全世界の死亡者数の約74%を占めています。特に、心血管疾患は年間1790万人という驚異的な犠牲者数で慢性疾患による死亡の大部分を占め、次いで癌が年間930万人の命を奪っています。このような背景から、バイオ医薬品は今後もヘルスケア分野でその重要性を増し続けると予想されており、増加する生産要件に対応し、これらの救命治療薬のタイムリーな供給を確保するために、効率的な**バイオ医薬品発酵システム**への必要性がさらに高まっています。慢性疾患の複雑な病態や、従来の小分子医薬品では治療が困難であった疾患領域において、バイオ医薬品はその高い特異性と有効性から、患者の予後改善に大きく貢献しています。高齢化社会の進展もまた、慢性疾患の患者数を増加させ、結果としてバイオ医薬品の需要を押し上げる要因となっています。
### 3. 市場抑制要因 (Restraints)
**バイオ医薬品発酵システム**市場における主要な抑制要因は、**限られた生産能力と拡張性の課題**です。技術的な進歩にもかかわらず、発酵プロセスの拡張性は、バイオ医薬品メーカーにとって依然として重大な課題として立ちはだかっています。研究室規模から商業規模への生産を拡大するには、設備、インフラ、プロセス最適化に多大な投資が必要となります。さらに、一貫した製品品質の維持、厳格な規制要件への準拠の確保、そして生産過程におけるボトルネックの管理に関連する複雑さが、追加的な課題を生み出しています。生産能力の制限は、生物学的製剤の供給不足、新規バイオ医薬品の市場投入の遅延、そして最終的には生産コストの増加につながる可能性があります。また、拡張可能な発酵ソリューションの不足は、バイオ医薬品企業が市場の需要増に対応し、新たな市場機会を十分に活用する能力を妨げる要因となることも指摘されています。大規模な生産施設を建設・維持するための財政的負担は大きく、特に小規模なバイオテクノロジー企業や新規参入企業にとっては参入障壁となり得ます。また、生物学的製剤特有の複雑な分子構造は、スケールアップの過程で品質特性や安定性が変動するリスクを伴うため、より厳格なプロセス管理とバリデーションが求められ、これがコストと時間をさらに増加させています。
### 4. 市場機会 (Opportunities)
**発酵プロセスの技術的進歩**は、**バイオ医薬品発酵システム**市場に革命をもたらし、生産の効率性、拡張性、柔軟性を大幅に向上させる機会を創出しています。注目すべき進歩の一つは、**シングルユースバイオリアクターの採用**です。これは、従来のステンレス製バイオリアクターに伴う高価な洗浄および滅菌プロセスを不要にします。これらの使い捨てシステムは、迅速なターンアラウンドタイム、交差汚染のリスク低減、そして低い設備投資という利点を提供し、小規模かつ柔軟なバイオ製造作業に理想的なソリューションとなっています。
さらに、**灌流ベースのバイオリアクターシステム**は、連続細胞培養においてその優位性から注目を集めています。これらのシステムは、従来のバッチまたはフェッドバッチプロセスと比較して、より高い細胞密度、培養期間の延長、そして生産性の向上を可能にします。これにより、より少ない施設面積でより多くの製品を生産できるようになり、全体的な生産コスト削減に貢献します。
また、人工知能(AI)および機械学習(ML)アルゴリズムを組み込んだ**自動制御システム**は、発酵パラメーターをリアルタイムで最適化し、プロセスの堅牢性と製品の一貫性を向上させています。これらのインテリジェントシステムは、人間の介入を最小限に抑えながら、予測分析に基づいて培養条件を微調整することで、エラーを減らし、収量を最大化します。
これらの技術的進歩は、バイオプロセシングにおける革新を推進し、**バイオ医薬品発酵システム**メーカーが、増加する需要に対応し、開発期間を短縮し、生産における費用対効果を向上させることを可能にします。これらの技術は、生産プロセスのデジタル化を促進し、データ駆動型の意思決定を可能にすることで、バイオ医薬品製造をより効率的で持続可能なものに変革する潜在力を秘めています。
### 5. セグメント分析
世界の**バイオ医薬品発酵システム**市場は、製品タイプ、用途、最終用途に基づいて細分化されています。
#### 5.1. 製品タイプ別
製品タイプに基づいて、市場はアップストリーム処理装置とダウンストリーム処理装置に分けられます。
* **アップストリーム処理装置:** このセグメントには、細胞培養、発酵、培地調製、細胞増殖のための装置が含まれます。具体的には、バイオリアクター、インキュベーター、培地調製システム、細胞分離装置などが挙げられます。これらは、バイオ医薬品生産プロセスの初期段階において、目的の生物学的製剤を生産する細胞の増殖と維持に不可欠な環境を提供します。
* **ダウンストリーム処理装置:** このセグメントは、発酵ブロスからバイオ医薬品を精製および分離するための多様な技術を包含します。これには、細胞やデブリを除去するためのろ過システム(例:デプスフィルター、膜ろ過システム)、タンパク質精製のためのクロマトグラフィーカラム(例:イオン交換、アフィニティー、サイズ排除クロマトグラフィー)、細胞分離のための遠心分離機、その他様々な精製技術が含まれます。ダウンストリーム処理装置は、不純物、凝集体、宿主細胞タンパク質を効果的に除去することで、バイオ医薬品の品質、純度、収率を確保する上で極めて重要な役割を果たします。さらに、これらの技術は、生物学的製剤の濃縮、分画、製剤化を可能にし、安全性と有効性に関する厳格な規制要件を満たすために不可欠です。シングルユースシステム、自動クロマトグラフィープラットフォーム、連続精製技術といったダウンストリーム処理装置の進歩は、バイオ医薬品製造における効率性、拡張性、費用対効果を高め、市場の成長と革新を推進しています。複雑な生物学的製剤の構造は、より高度で特異的な精製技術を必要とし、このセグメントの技術革新を加速させています。
#### 5.2. 用途別
用途に基づいて、市場はワクチン、モノクローナル抗体、組換えタンパク質、プロバイオティクス、その他に細分化されます。
* **組換えタンパク質:** **バイオ医薬品発酵システム**市場における組換えタンパク質セグメントは、遺伝子工学技術を通じて治療用タンパク質を生産することを包含します。インスリン、成長因子、サイトカイン、そしてモノクローナル抗体など、組換えタンパク質は様々な疾患に対して計り知れない治療の可能性を秘めています。**バイオ医薬品発酵システム**は、微生物または哺乳類細胞培養に由来するかどうかにかかわらず、これらのタンパク質の効率的かつ拡張可能な生産において極めて重要な役割を果たします。これらのシステムは、細胞の成長とタンパク質発現に最適化された制御された環境を提供し、高い収量と製品品質を保証します。シングルユースバイオリアクターや灌流システムなどの発酵技術の進歩は、組換えタンパク質生産における生産性と柔軟性を大幅に向上させました。標的療法や個別化医療への需要が高まるにつれて、組換えタンパク質セグメントは、継続的な研究、新規生物学的製剤の開発、そして疾患管理における応用拡大によって、今後も大幅な成長を遂げる態勢にあります。特に、希少疾患や難病に対する治療薬としての組換えタンパク質の開発が活発化しており、この分野の成長を牽引しています。
#### 5.3. 最終用途別
最終用途に基づいて、市場はバイオ医薬品企業、医薬品受託開発製造機関(CDMO)、学術・研究機関、その他に分けられます。
* **バイオ医薬品企業:** バイオ医薬品企業は、**バイオ医薬品発酵システム**市場において最も重要な最終用途セグメントを構成します。これらの企業は、モノクローナル抗体、組換えタンパク質、ワクチン、その他のバイオ医薬品を含む生物学的製剤の研究、開発、製造、そして商業化に従事しています。彼らは、これらの生物学的製剤の大量生産のために**バイオ医薬品発酵システム**に大きく依存しており、高度なバイオプロセシング技術を活用して収量、品質、効率を最適化しています。バイオ医薬品企業は、製造業務をサポートするために、バイオリアクターやダウンストリーム処理システムなどの最先端の**バイオ医薬品発酵システム**に多大な投資を行っています。さらに、これらの企業は、規制要件への準拠を確保し、製品の一貫性を維持するために、プロセス自動化、リアルタイムモニタリング、品質管理システムを統合することが多いです。バイオ医薬品の需要が引き続き増加するにつれて、バイオ医薬品企業は、生産能力を強化し、コストを削減し、新しい治療法の市場投入までの時間を短縮するために、革新的な**バイオ医薬品発酵システム**ソリューションを積極的に模索しています。大手製薬企業から新興バイオテクノロジー企業まで、バイオ医薬品のパイプラインの拡大は、**バイオ医薬品発酵システム**への継続的な投資を促しています。
### 6. 地域分析
世界の**バイオ医薬品発酵システム**市場は、北米、欧州、アジア太平洋、ラテンアメリカ、中東およびアフリカに区分されます。
* **北米:** 北米は、世界の**バイオ医薬品発酵システム**市場において最も重要なシェアを占めており、予測期間中に大幅に拡大すると予想されています。この地域は、確立されたバイオ医薬品企業の存在、堅牢な研究開発インフラ、そして有利な規制枠組みによって特徴づけられる、支配的で成熟した市場です。研究開発への強い重点と、癌や自己免疫疾患などの一般的な慢性疾患に対処するための生物学的製剤への高い需要が、市場の成長を引き続き牽引しています。RANDが実施した最近の調査によると、米国成人の60%が少なくとも1つの慢性疾患を抱え、そのうち42%が複数の慢性疾患に罹患しており、年間数千億ドルもの医療費に貢献しています。この状況が、北米地域における生物学的製剤の需要を促進し、ひいては地域の市場拡大を後押しすると推定されます。さらに、バイオ医薬品企業、CDMO、学術機関間の活発な協力関係が、技術移転と知識交換を促進し、地域における革新と市場拡大を推進しています。例えば、2021年9月には、バイオ医薬品製造向けの統合ソリューションおよびサービスを提供する世界的プロバイダーであるABECと、高品質の規制された生物学的製剤、原薬、中間体を臨床から商業規模で生産するCDMOであるBIOVECTRAが提携を発表しました。この提携により、ABECはカナダのノバスコシア州ウィンザーにあるBIOVECTRAの製造施設にCSRシングルユース微生物発酵ソリューションを設計、製造、設置することになりました。ABEC CSRシングルユース発酵ソリューションの導入は、BIOVECTRAの急速な成長を遂げている微生物発酵プロセスを改善し、製品とバッチ間の迅速な移行を可能にするものであり、このような要因が市場成長を後押しすると期待されています。
* **アジア太平洋地域:** アジア太平洋地域は、いくつかの主要因に牽引され、**バイオ医薬品発酵システム**市場で急速な成長を経験しています。インド、中国、韓国などの国々におけるヘルスケアインフラへの投資の増加は、バイオ医薬品製造能力を拡大し、市場需要を促進しています。この地域は、大規模な熟練労働力と比較的低い生産コストという利点があり、生物学的製剤の外部委託生産にとって魅力的な目的地となっています。さらに、有利な規制政策とバイオテクノロジーおよび革新を促進するための政府の取り組みが、この地域の市場成長に大きく貢献しています。例えば、ウッタルプラデーシュ州政府は、製薬およびバイオテクノロジー産業における地位を強化するための措置を積極的に実施しています。州はこれらの分野での使命を推進するために3つの重要なプロジェクトを設立しており、その中にはピリビットに高度なバイオテクノロジーパークを開発する計画も含まれます。このパークは、発酵ベース製品の輸入に対処しつつ、この分野での自給自足を促進するように設計されており、これらの努力は、ウッタルプラデーシュ州を製薬およびバイオテクノロジー分野で有名な中心地として確立すると期待されています。これらの要因が相まって、アジア太平洋地域の市場成長を加速させています。
* **欧州、ラテンアメリカ、中東およびアフリカ:** これらの地域もグローバル市場の重要な一部を構成していますが、本レポートでは詳細な市場動向に関する言及は限定的です。しかし、それぞれの地域においても、ヘルスケアインフラの整備、バイオ医薬品開発への投資、慢性疾患の増加といった要因が、**バイオ医薬品発酵システム**の需要に影響を与えていると考えられます。
### 結論
グローバル**バイオ医薬品発酵システム**市場は、慢性疾患の有病率増加とバイオ医薬品への需要拡大という強力な促進要因に支えられ、今後も堅調な成長を続けると予測されます。限られた生産能力や拡張性の課題といった抑制要因は存在するものの、シングルユースバイオリアクター、灌流システム、自動制御システムといった革新的な発酵技術の進歩が、これらの課題を克服し、生産効率と柔軟性を大幅に向上させる機会を創出しています。北米は引き続き市場を牽引する主要地域であり、アジア太平洋地域が急速な成長を遂げています。製品タイプ、用途、最終用途の各セグメントにおいても、技術革新と需要の変化が市場構造を形成しており、**バイオ医薬品発酵システム**は、将来の医療とバイオ医薬品製造の発展において不可欠な役割を担い続けるでしょう。
Report Coverage & Structure
- セグメンテーション
- 調査方法論
- 無料サンプルを入手
- 目次
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制約と仮定
- 市場範囲とセグメンテーション
- 考慮される通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興用途/最終用途
- 市場トレンド
- 推進要因
- 市場の警告要因
- 最新のマクロ経済指標
- 地政学的な影響
- 技術的要因
- 市場評価
- ポーターの5つの力分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- ヨーロッパ
- APAC
- 中東およびアフリカ
- ラテンアメリカ
- ESGトレンド
- 世界のバイオ医薬品発酵システム市場規模分析
- 世界のバイオ医薬品発酵システム市場概要
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- 北米市場分析
- はじめに
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- 米国
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- カナダ
- ヨーロッパ市場分析
- はじめに
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- 英国
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他のヨーロッパ
- APAC市場分析
- はじめに
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- 中国
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- 韓国
- 日本
- インド
- オーストラリア
- シンガポール
- 台湾
- 東南アジア
- その他のアジア太平洋地域
- 中東およびアフリカ市場分析
- はじめに
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- アラブ首長国連邦
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他の中東およびアフリカ
- ラテンアメリカ市場分析
- はじめに
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- ブラジル
- 製品タイプ別
- はじめに
- 製品タイプ別金額
- 上流工程製品
- 金額別
- バイオリアクター/発酵槽
- バイオリアクター/発酵槽別金額
- バイオプロセスアナライザー
- バイオプロセスアナライザー別金額
- プロセス監視システム
- プロセス監視システム別金額
- その他の上流工程製品
- その他の上流工程製品別金額
- 下流工程製品
- 金額別
- ろ過と分離
- ろ過と分離別金額
- クロマトグラフィー
- クロマトグラフィー別金額
- 消耗品と付属品
- 消耗品と付属品別金額
- その他の下流工程製品
- その他の下流工程製品別金額
- 用途別
- はじめに
- 用途別金額
- ワクチン
- 金額別
- モノクローナル抗体
- 金額別
- 組換えタンパク質
- 金額別
- プロバイオティクス
- 金額別
- その他
- 金額別
- エンドユーザー別
- はじめに
- エンドユーザー別金額
- バイオ医薬品企業
- 金額別
- 医薬品開発製造受託機関 (CDMO)
- 金額別
- 学術機関および研究機関
- 金額別
- その他
- 金額別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のラテンアメリカ
- 競合状況
- バイオ医薬品発酵システム市場のプレイヤー別シェア
- M&A契約と提携分析
- 市場プレイヤー評価
- サーモフィッシャーサイエンティフィック株式会社
- 概要
- 企業情報
- 収益
- 平均販売価格 (ASP)
- SWOT分析
- 最近の動向
- GEヘルスケア
- メルクKGaA
- ザルトリウスAG
- ロンザ
- ダナハーコーポレーション
- エッペンドルフAG
- ベクトン
- ディッキンソン・アンド・カンパニー
- ピエール・ゲラン (DCI-Biolafitte)
- ZETAホールディングGmbH
- 調査方法論
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次調査の内訳
- 二次および一次調査
- 主要な業界インサイト
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査仮定
- 仮定
- 制約
- リスク評価
- 付録
- ディスカッションガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
*** 本調査レポートに関するお問い合わせ ***

バイオ医薬品発酵システムとは、遺伝子組換え技術を適用した微生物や動物細胞などを培養し、医薬品として利用されるタンパク質や核酸といった有効成分を効率的に生産するための一連の技術と設備を指します。これらのシステムは、生命科学の進歩と工学技術の融合により発展し、現代医療において、これまで治療が困難であった多くの疾患に対する新たな治療選択肢を提供しています。その核心には、目的の医薬品成分の遺伝子を組み込んだ宿主細胞を、厳密に管理された環境下で増殖させ、大量に生産させるという原理があります。
このシステムで用いられる宿主細胞には、主に細菌、酵母、そして動物細胞の三種類が存在します。細菌、特に大腸菌は、その増殖速度の速さ、高いタンパク質生産能力、比較的簡便な培養条件から、インスリン断片や成長ホルモンなど、比較的単純な構造のタンパク質医薬品の生産に広く利用されています。しかしながら、細菌はヒトのタンパク質が持つ複雑な糖鎖修飾を行う能力に乏しいという限界があります。一方、酵母は真核細胞であり、ある程度の糖鎖修飾能力を持つため、ワクチンや一部の酵素製剤などの生産に適しています。さらに、最も複雑な糖鎖修飾や高次構造を必要とする抗体医薬品などの生産には、チャイニーズハムスター卵巣細胞(CHO細胞)に代表される動物細胞が不可欠です。動物細胞培養は、培養に時間とコストがかかり、設備も複雑になるという課題がありますが、ヒトの生体内で機能する医薬品と極めて類似した構造を持つタンパク質を生産できるという大きな利点があります。
培養システムの運用方法にもいくつかの種類があります。回分培養は、培養開始時に全ての栄養分を加え、細胞が増殖して目的物質を生産した後、培養液全体を回収する最も基本的な方法です。流加培養は、培養中に栄養分を段階的に供給することで、細胞の生存期間と生産期間を延長し、より高い細胞密度と生産性を達成する方法で、バイオ医薬品の生産において最も一般的に用いられています。連続培養は、新鮮な培地を継続的に供給しつつ、古い培養液と細胞の一部を排出することで、定常状態での長期的な生産を可能にする方法ですが、無菌性の維持や品質の均一性管理が難しいため、特定の製品や研究用途に限定されることが多いです。
バイオ医薬品発酵システムによって生産される医薬品は多岐にわたります。例えば、関節リウマチや炎症性腸疾患、乾癬などの自己免疫疾患や、特定の癌の治療に用いられるモノクローナル抗体は、主に動物細胞培養によって生産されます。糖尿病治療薬である遺伝子組換えインスリンや、腎性貧血治療薬のエリスロポエチン、成長ホルモン補充療法薬なども、このシステムから生まれています。さらに、感染症予防のための組換えワクチンや、特定の酵素欠損症に対する酵素補充療法薬など、その応用範囲は広がり続けており、人々の健康と生活の質の向上に大きく貢献しています。
これらのバイオ医薬品を効率的かつ安全に生産するためには、発酵システムを取り巻く様々な関連技術が不可欠です。上流工程では、目的遺伝子を宿主細胞に導入するための遺伝子組換え技術、高生産性かつ安定した細胞株を選抜・開発する技術、そして細胞の増殖と目的物質の生産を最大化するための最適な培地開発技術が重要です。また、培養槽であるバイオリアクターの設計と、温度、pH、溶存酸素濃度、攪拌速度などを厳密に制御する技術も、生産効率と品質を左右します。下流工程では、培養液から目的の医薬品成分を分離・精製する技術が求められます。これには、細胞の分離、クロマトグラフィーを用いた高度な精製、ウイルス除去・不活化、そして最終製品の安定化といった工程が含まれます。さらに、製造プロセスの各段階で製品の純度、力価、安全性、安定性を確認するための厳格な品質管理(Quality Control, QC)と品質保証(Quality Assurance, QA)体制が不可欠であり、高速液体クロマトグラフィー(HPLC)や質量分析法、ELISAなどの分析技術が活用されます。近年では、プロセス分析技術(PAT)の導入により、製造工程をリアルタイムで監視・制御し、品質の一貫性を高める取り組みも進められています。また、清掃・滅菌作業を簡素化し、製造の柔軟性を高める使い捨て培養装置(シングルユースシステム)の利用も拡大しています。
このように、バイオ医薬品発酵システムは、高度な生物工学と精密な工学技術が融合した複雑なシステムであり、その継続的な進化が、今後も革新的な医薬品の創出と医療の発展を支えていくことでしょう。