ヒト肝臓モデル市場 規模・シェア分析 – 成長動向と予測 (2025年~2030年)
ヒト肝臓モデル市場は、製品タイプ(2Dモデル、3Dモデル、リバーオンアチップ、その他)、用途(教育、創薬、その他)、および地域(北米、欧州、アジア太平洋、中東およびアフリカ、南米)によって分類されます。本レポートは、上記のセグメントについて米ドル建ての市場規模を提供します。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
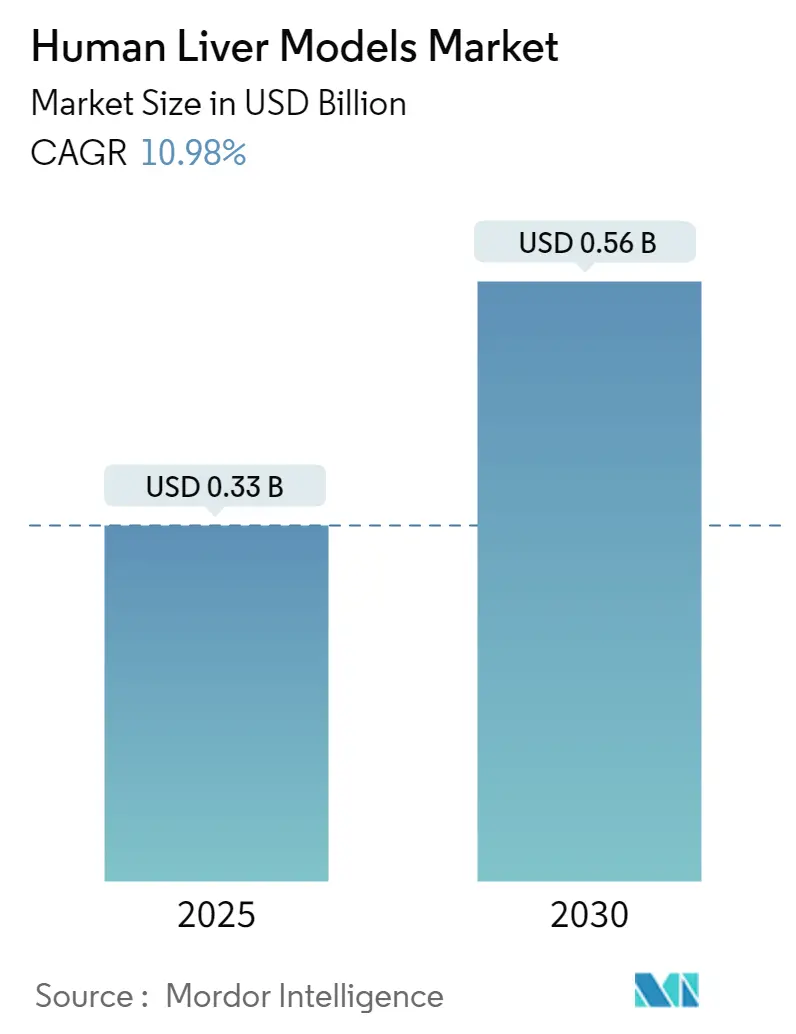
「ヒト肝臓モデル市場」は、2025年から2030年の予測期間において、顕著な成長が見込まれています。Mordor Intelligenceの分析によると、市場規模は2025年に3億3,000万米ドルと推定され、2030年には5億6,000万米ドルに達すると予測されており、予測期間中の年平均成長率(CAGR)は10.98%です。この市場は、製品タイプ(2Dモデル、3Dモデル、リバーオンチップ、その他)、アプリケーション(教育、創薬、その他)、および地域(北米、ヨーロッパ、アジア太平洋、中東・アフリカ、南米)にセグメント化されています。北米が最大の市場であり、アジア太平洋地域が最も急速に成長すると見込まれています。市場の集中度は中程度です。
市場概要
COVID-19パンデミックの影響と回復:
COVID-19パンデミックは、本市場に大きな影響を与えました。2021年10月にCDCが発表したデータによると、肝疾患を持つ高齢患者はCOVID-19による重症化リスクが高いとされていました。肝細胞癌(HCC)患者、特に慢性肝疾患(B型肝炎やC型肝炎など)を持つ人々も、重症COVID-19のリスクが高いことが示されました。パンデミック中、医療業界の焦点がCOVID-19の管理に傾いたため、本市場は一時的に影響を受けました。しかし、現在では研究およびヒト肝臓モデルの需要に関してパンデミック前の状態に戻っており、今後数年間で力強い成長が見込まれています。
市場成長の主要因:
市場成長の主な要因としては、肝疾患の罹患率増加と臓器プリンティング技術の進歩が挙げられます。さらに、動物由来モデルの代替品開発への注力と、結果の精度向上も市場成長を後押しすると予測されています。非脂肪性肝疾患の罹患率増加や、肝疾患につながるアルコール消費量の増加も、予測期間中の市場成長を促進すると期待されています。
肝臓がんの統計と創薬への影響:
現在のライフスタイルの変化により、多くの人々が肝臓がんのリスク要因にさらされています。これらのリスク要因には、2型糖尿病、肝炎、代謝性疾患、過体重、アルコール消費、喫煙などが含まれます。GLOBOCANのデータによると、2020年には世界中で約905,677件(4.7%)の新規肝臓がん症例と、肝臓がんによる830,180件(8.3%)の死亡が報告されました。肝臓がんに対する治療薬への高い需要は、肝臓モデルを用いた創薬において市場参加者に大きな機会をもたらすと予想されます。
肝細胞癌(HCC)と慢性肝疾患の課題:
肝細胞癌(HCC)と慢性肝疾患は、治療選択肢が限られている致死的な疾患です。臨床的に適用可能で扱いやすい実験モデルの不足が、治療研究の妨げとなっています。Precision Bioscienceが2021年9月に発表したデータによると、世界の人口の1%から2%に影響を与えると予測される進行性肝線維症および肝硬変の高い有病率のため、がん発生への肝疾患進行の化学予防には、満たされていない医療ニーズが大きく存在します。したがって、肝疾患の罹患率上昇に伴い、研究目的でのヒト肝臓モデルの需要が高まっており、市場成長を促進しています。
市場の阻害要因:
一方で、肝臓モデルの高コストや、既存のワークフローへの肝臓モデルの組み込みに関する課題が、予測期間中の市場成長を妨げると予想されています。
世界のヒト肝臓モデル市場のトレンドと洞察
リバーオンチップの著しい成長:
リバーオンチップは、肝臓の基本的な機能の主要な特徴をシミュレートできるバイオエンジニアリングシステムです。他のモデルと比較して、よりシンプルで安価であるという利点があります。さらに、創薬および開発における動物モデルの低コスト代替品への需要が高まっていることから、このセグメントは著しい成長を遂げると予測されています。肝臓オルガノイドに関する取り組みの増加や、ヒト臓器モデリングにおける技術的進歩も、市場全体の成長を促進すると期待されています。
また、肝臓感染症の増加や、多くの薬剤開発における肝臓モデルの使用も、予測期間中の市場成長を後押しすると予想されます。CDCが2021年3月に発表したデータによると、米国では毎年約25,000人の男性と11,000人の女性が肝臓がんを発症し、約19,000人の男性と9,000人の女性がこの病気で亡くなっています。世界中でアルコール消費量が増加し、肝疾患につながっていることも、肝臓モデルの需要を高めています。
肝疾患研究のための革新的なin vitro法の探求は、マイクロ流体工学のような新興技術やエンジニアリング技術によって促進される可能性があります。マイクロ流体臓器オンチッププラットフォームは、薬剤開発に関連する時間とコストを削減する可能性を秘めているため、これらの方法の一つとして大きく成長しています。例えば、PubMedが2022年3月に発表したデータは、リバーオンチップが世界中で広く採用されると予想される新興技術の一つであることを示しています。さらに、BioMed Central Journalが2022年12月に発表したデータによると、リバーオンチップと他の臓器とのクロストークを実現するために、肝臓-腎臓チップ、肝臓-腸チップ、肝臓-免疫チップ、そして最終的にはヒューマンオンチップのような次世代の多臓器オンチップの開発が研究で期待されています。したがって、リバーオンチップ技術の重要性が高まるにつれて、このセグメントは今後数年間で力強い成長を遂げると予想されます。
北米が市場で大きなシェアを占める見込み:
北米は、研究開発費の増加、臓器モデルの革新、および革新的な潜在的治療法の採用により、市場の大部分を占めると予想されています。さらに、肝疾患の罹患率増加と、この地域に主要な市場参加者が存在することも、予測期間中の市場成長を促進すると期待されています。
米国における肝臓がんの負担増加は、市場成長を推進する可能性が高いです。例えば、米国がん協会が2022年11月に発表したデータによると、2022年の米国における肝臓がん症例の推定数は約41,260件であり、前年と比較して大幅に増加しています。したがって、肝臓がんの負担が増加するにつれて、米国における本市場は今後数年間で力強く成長すると予想されます。
さらに、米国における肝臓移植への需要増加も市場成長を後押ししています。例えば、米国保健資源サービス局(HRSA)が2022年6月に発表したデータによると、2021年には米国で9,236件の肝臓移植が行われました。これらの肝臓移植のうち、約4,145件は50歳から64歳の人々に行われました。肝臓移植数の増加に伴い、国内でのヒト肝臓モデルの需要が高まっており、市場成長を促進しています。
競争環境
世界のヒト肝臓モデル市場は、中程度の統合度で競争が激しいです。市場参加者は、市場シェアを拡大するために、製品革新、新製品の発売、および地域拡大に注力しています。市場で活動している主要な企業には、Emulate, Inc.、InSphero、BioIVT、Organovo Holdings Inc.、Mimetasなどが含まれます。
最近の業界動向
* 2023年9月: UC Davis Healthは、新しい成人肝臓移植プログラムを開始しました。この動きは、UC Davis移植センターの既存サービスを拡大し、肝疾患患者に包括的なケアを提供します。
* 2022年4月: 臓器オンチップ(OoC)企業であるCN Bioは、非アルコール性脂肪性肝炎(NASH)向けのPhysioMimix ‘in-a-box’ 肝臓OoC試薬キットを発売しました。NASHは、従来のin vivo動物実験ではこの複雑な疾患に対するヒトの反応を予測できないため、現在までに規制当局に承認された治療法がない疾患です。
全体として、肝疾患の増加、技術革新、そして動物モデル代替への需要の高まりが、ヒト肝臓モデル市場の持続的な成長を牽引していくと見込まれます。特にリバーオンチップ技術の進化と北米市場の堅調な拡大が、今後の市場発展の鍵となるでしょう。
このレポートは、ヒト肝臓モデル市場に関する詳細な分析を提供しています。肝臓は血液凝固因子の合成、胆汁生成、タンパク質生成、解毒といった重要な身体機能を果たす臓器であり、ヒト肝臓モデルは薬剤毒性の研究、薬剤効果の理解、肝疾患の進行解明に利用されます。
市場規模と予測:
ヒト肝臓モデル市場は、2024年には0.29億米ドルと推定されています。2025年には0.33億米ドルに達し、その後2025年から2030年にかけて年平均成長率(CAGR)10.98%で成長し、2030年には0.56億米ドルに達すると予測されています。
市場のダイナミクス:
市場の成長を促進する要因としては、慢性疾患の有病率増加と高齢者人口の増加が挙げられます。また、技術的に高度なヒト肝臓モデル(原文では「ストレッチャー」と記載されていますが、レポートの主題からヒト肝臓モデルと解釈されます)への需要が高まっていることも、市場を牽引する主要なドライバーです。
一方、市場の成長を抑制する要因としては、特殊なヒト肝臓モデル(原文では「ストレッチャー」と記載)の高コストや、在宅医療の普及が挙げられています。
さらに、ポーターのファイブフォース分析を通じて、買い手/消費者の交渉力、サプライヤーの交渉力、新規参入者の脅威、代替製品の脅威、競争の激しさといった競争環境が分析されています。
市場セグメンテーション:
市場は以下の主要なセグメントに分類されています。
* 製品タイプ別: 2Dモデル、3Dモデル、Liver-on-a-Chip、その他の製品タイプ。
* 用途別: 教育、創薬、その他の用途。
* 地域別: 北米(米国、カナダ、メキシコ)、ヨーロッパ(ドイツ、英国、フランス、イタリア、スペイン、その他のヨーロッパ)、アジア太平洋(中国、日本、インド、オーストラリア、韓国、その他のアジア太平洋)、中東およびアフリカ(GCC、南アフリカ、その他の中東およびアフリカ)、南米(ブラジル、アルゼンチン、その他の南米)。
地域別の洞察:
地域別に見ると、2025年には北米がヒト肝臓モデル市場において最大の市場シェアを占めると予想されています。また、アジア太平洋地域は予測期間(2025年~2030年)において最も高いCAGRで成長すると推定されています。
競争環境:
主要な市場プレイヤーとしては、Organovo Holdings Inc.、BioIVT、InSphero、Emulate, Inc.、Mimetas、CN Bio、Cyfuse Biomedical K.K.、HuREL Corporationなどが挙げられます。これらの企業は、ビジネス概要、財務状況、製品と戦略、最近の動向に基づいて分析されています。
レポートの範囲と更新日:
このレポートは、世界の主要地域にわたる17カ国の市場規模とトレンドを網羅しており、各セグメントの価値を米ドルで提供しています。最終更新日は2024年10月29日です。

1. はじめに
- 1.1 調査の前提条件と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場の動向
- 4.1 市場概要
-
4.2 市場の推進要因
- 4.2.1 慢性疾患と高齢者人口の増加
- 4.2.2 技術的に高度なストレッチャーへの需要の増加
-
4.3 市場の制約
- 4.3.1 特殊ストレッチャーの高コスト
- 4.3.2 在宅医療の採用の増加
-
4.4 ポーターのファイブフォース分析
- 4.4.1 買い手/消費者の交渉力
- 4.4.2 供給者の交渉力
- 4.4.3 新規参入者の脅威
- 4.4.4 代替品の脅威
- 4.4.5 競争の激しさ
5. 市場セグメンテーション
-
5.1 製品タイプ別
- 5.1.1 2Dモデル
- 5.1.2 3Dモデル
- 5.1.3 肝臓オンチップ
- 5.1.4 その他の製品タイプ
-
5.2 用途別
- 5.2.1 教育
- 5.2.2 創薬
- 5.2.3 その他の用途
-
5.3 地域
- 5.3.1 北米
- 5.3.1.1 米国
- 5.3.1.2 カナダ
- 5.3.1.3 メキシコ
- 5.3.2 ヨーロッパ
- 5.3.2.1 ドイツ
- 5.3.2.2 イギリス
- 5.3.2.3 フランス
- 5.3.2.4 イタリア
- 5.3.2.5 スペイン
- 5.3.2.6 その他のヨーロッパ
- 5.3.3 アジア太平洋
- 5.3.3.1 中国
- 5.3.3.2 日本
- 5.3.3.3 インド
- 5.3.3.4 オーストラリア
- 5.3.3.5 韓国
- 5.3.3.6 その他のアジア太平洋
- 5.3.4 中東およびアフリカ
- 5.3.4.1 GCC
- 5.3.4.2 南アフリカ
- 5.3.4.3 その他の中東およびアフリカ
- 5.3.5 南米
- 5.3.5.1 ブラジル
- 5.3.5.2 アルゼンチン
- 5.3.5.3 その他の南米
6. 競争環境
-
6.1 企業プロフィール
- 6.1.1 Organovo Holdings Inc.
- 6.1.2 BioIVT
- 6.1.3 InSphero
- 6.1.4 Emulate, Inc.
- 6.1.5 Mimetas
- 6.1.6 CN Bio
- 6.1.7 Cyfuse Biomedical K.K.
- 6.1.8 HuREL Corporation
- *リストは網羅的ではありません
7. 市場機会と将来のトレンド
*** 本調査レポートに関するお問い合わせ ***

ヒト肝臓モデルとは、生体内の複雑な肝臓の機能や構造を、in vitro(試験管内)やin vivo(生体内)で再現しようとするシステム全般を指します。これは、薬物代謝、毒性評価、疾患メカニズムの解明、再生医療研究など、多岐にわたる生命科学分野において、動物モデルの限界(種差など)を克服し、よりヒトに近い応答を評価するために開発が進められている重要なツールです。特に、ヒトの肝臓は薬物の代謝や解毒の中心臓器であるため、新薬開発における有効性・安全性評価において、その高精度なモデルの必要性が強く認識されています。
ヒト肝臓モデルには様々な種類が存在します。最も基本的なものは、初代肝細胞や肝細胞株(HepG2など)を用いた2次元(2D)培養モデルです。これは簡便に利用できる利点がありますが、細胞が生体内の環境から大きく乖離するため、機能維持期間が短く、生体内の複雑な構造や機能を十分に再現できないという限界がありました。この限界を克服するために開発されたのが、3次元(3D)培養モデルです。3D培養モデルには、肝細胞やiPS細胞由来の肝細胞を自己組織化させて作製するスフェロイドやオルガノイドがあります。これらは、細胞間相互作用や細胞外マトリックスとの相互作用が生体に近い形で再現され、機能維持期間が延長されるとともに、より生体内の肝臓に近い薬物応答を示すことが報告されています。また、ハイドロゲルなどの足場材料を用いて細胞を培養したり、3Dバイオプリンティング技術を駆使して細胞や生体材料を積層し、より複雑な組織構造を構築する試みも進められています。
さらに、マイクロ流体デバイスを用いた「Organ-on-a-chip(臓器チップ)」も注目されています。これは、微細な流路を持つチップ上で肝細胞を培養し、生体内の血流や微小環境を再現することで、より生理的な条件下での薬物評価や疾患研究を可能にします。複数の臓器モデルを連結し、臓器間の相互作用を評価するマルチオルガンチップの開発も進んでおり、全身レベルでの薬物動態や毒性評価への応用が期待されています。in vivoモデルとしては、免疫不全動物にヒト肝細胞を移植し、生体内でヒト肝臓の機能を発現させるヒト化動物モデルがあります。これは、in vivoでの薬物動態や肝炎ウイルス感染研究など、生体内の複雑な環境下での評価に有用です。
これらのヒト肝臓モデルは、多岐にわたる用途で活用されています。創薬研究においては、新薬候補物質のスクリーニングや有効性評価、薬物代謝酵素の誘導・阻害評価に用いられます。また、医薬品や化学物質の肝毒性(DILI)予測やメカニズム解析といった毒性評価にも不可欠です。疾患モデルとしては、非アルコール性脂肪肝炎(NASH)、肝線維症、肝炎ウイルス感染症、肝がんなどの病態をin vitroで再現し、疾患メカニズムの解明や新規治療法の開発に貢献しています。将来的には、肝臓移植の代替技術や人工肝臓の開発といった再生医療分野への応用も期待されています。
ヒト肝臓モデルの発展を支える関連技術も目覚ましい進歩を遂げています。特に、人工多能性幹細胞(iPS細胞)技術は、患者由来のiPS細胞から肝細胞を分化誘導することで、疾患特異的なモデルや個別化医療に資するモデルの構築を可能にしました。3Dバイオプリンティング技術は、細胞と生体材料を精密に配置し、血管網や胆管など、より生体に近い複雑な肝臓組織を構築する可能性を広げています。マイクロ流体技術はOrgan-on-a-chipの基盤であり、微小環境の精密制御やハイスループットスクリーニングへの応用を可能にしています。さらに、ゲノム編集技術(CRISPR/Cas9など)を用いることで、疾患関連遺伝子の導入や除去を効率的に行い、特定の疾患モデルをより正確に作成できるようになりました。これらのモデルの機能評価には、バイオセンサーや高度なイメージング技術が不可欠であり、リアルタイムでのモニタリングや詳細な解析を可能にしています。
市場背景としては、動物実験代替への強いニーズが挙げられます。倫理的観点や種差の問題から、動物実験を減らし、よりヒトに近いモデルでの評価への移行が世界的に進んでいます。また、新薬開発のコスト高騰と成功率の低さという課題に対し、in vitroでの高精度な評価モデルは、開発プロセスの効率化と成功率向上に大きく貢献すると期待されています。個別化医療の進展も市場を牽引する要因の一つであり、患者由来iPS細胞を用いたモデルにより、個々の患者に合わせた薬物応答予測が可能になりつつあります。これらの背景から、Organ-on-a-chipや3D細胞培養市場は急速に成長しており、製薬企業、化学メーカー、受託研究機関(CRO)などでの導入が加速しています。一方で、モデルの標準化、再現性の確保、スケールアップ、そして複雑な生体機能(免疫細胞との相互作用、神経支配など)の完全な再現といった課題も残されています。
将来展望として、ヒト肝臓モデルはさらなる高機能化・複雑化が期待されています。血管網、胆管、免疫細胞、神経細胞など、より多くの細胞種を組み込んだ複合的なモデルの開発が進み、最終的には複数の臓器モデルを連結した全身モデル(Human-on-a-chip)の実現も視野に入っています。これにより、薬物の全身的な影響や臓器間相互作用を評価できるようになるでしょう。個別化医療への貢献も大きな柱であり、患者iPS細胞由来モデルを用いた個別化薬物スクリーニングや副作用予測は、精密医療の実現に向けた重要な基盤技術となります。また、人工肝臓としての機能代替や移植医療への応用といった臨床応用への展開も期待されており、疾患の病態解明や新規バイオマーカーの探索にも貢献するでしょう。さらに、モデルから得られる膨大なデータをAIやデータサイエンスと融合させることで、創薬プロセスのさらなる効率化や予測モデルの構築が進むと考えられます。これらの技術が社会に広く受け入れられるためには、モデルの信頼性向上と、規制当局による評価基準の確立が不可欠であり、国際的な連携のもとで標準化が進められることが望まれます。