固形がん治療薬市場 規模・シェア分析 – 成長トレンド・予測 (2025年~2030年)
固形がん治療薬市場レポートは、がん種(乳がん、肺がんなど)、薬剤タイプ(カルボプラチン、シスプラチンなど)、投与経路(静脈内、経口、皮下、腫瘍内、その他の投与経路)、および地域(北米、欧州、アジア太平洋、中東・アフリカ、南米)別に分類されます。市場予測は金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
固形腫瘍治療薬市場の概要
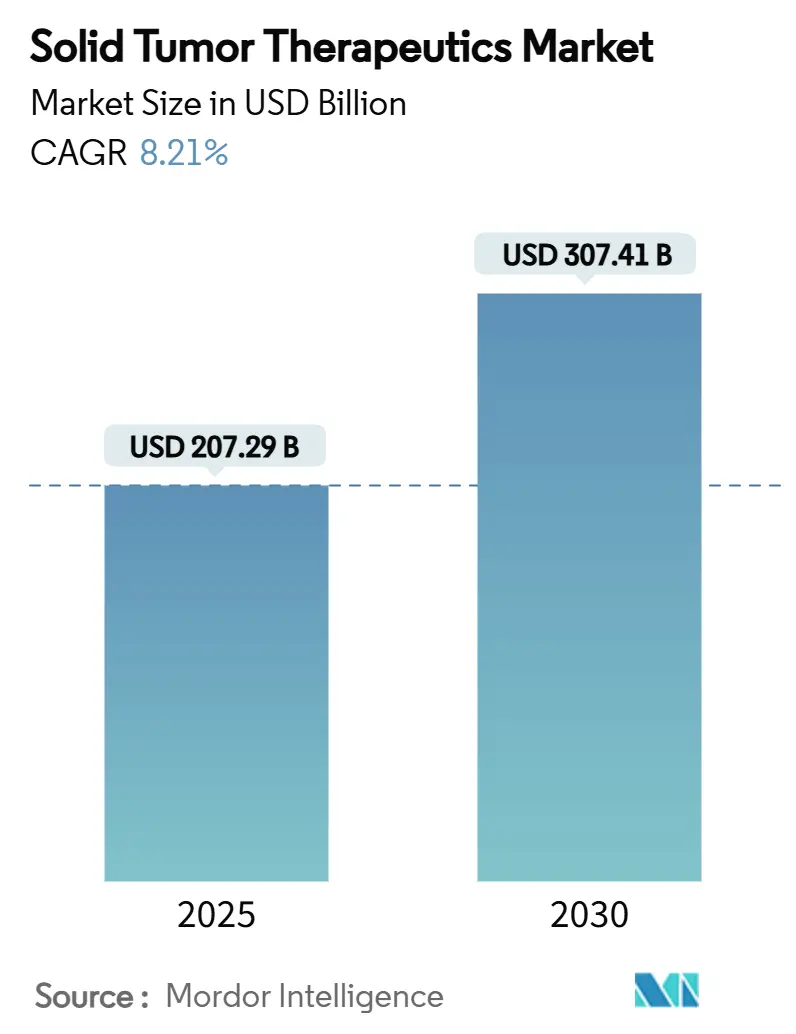
固形腫瘍治療薬市場は、2025年に2,072.9億米ドルに達し、2030年には3,074.1億米ドルに成長すると予測されており、予測期間中の複合年間成長率(CAGR)は8.21%です。抗体薬物複合体(ADC)、免疫チェックポイント阻害剤の併用療法、バイオマーカーに基づく治療法の革新が市場を牽引しています。2050年までに年間3,200万件の新規症例が予測されるがんの罹患率上昇が、長期的な需要を支えています。米国における価値に基づく償還制度や欧州における成果連動型契約は、支払者の信頼を高めています。北米は強力な知的財産保護により価格決定の主導権を維持していますが、アジア太平洋地域では規制当局の承認加速によりイノベーションの差が縮まっています。大手多国籍企業と中堅バイオテクノロジー企業の統合が進み、競争環境が変化しており、AIを活用した創薬パートナーシップへの投資が前臨床期間を短縮しています。
主要な報告書のポイント
* がんの種類別: 乳がんが2024年に25.67%の収益シェアを占め、市場をリードしました。前立腺がんは2030年までに10.34%のCAGRで拡大すると予測されています。
* 薬剤の種類別: ベバシズマブが2024年に固形腫瘍治療薬市場シェアの12.45%を占めました。シスプラチンは同期間に12.45%のCAGRを記録すると予想されています。
* 投与経路別: 静脈内投与が2024年の収益の46.54%を占めました。経口投与は2030年までに10.67%のCAGRで成長する見込みです。
* 地域別: 北米が2024年に42.43%のシェアを維持しました。アジア太平洋地域は2030年までに9.54%のCAGRで最も速く成長すると予測されています。
世界の固形腫瘍治療薬市場のトレンドと洞察
市場の推進要因
1. 世界的ながん罹患率と有病率の上昇:
固形腫瘍治療薬市場は、がんの負担増大と直接的に関連しています。がんの新規診断数は2050年までに年間3,200万件に達すると予測されており、その約85%を固形腫瘍が占めます。アジア太平洋地域では、都市化とライフスタイルの変化がリスク要因を悪化させ、最も急激な増加が見られます。中国だけでも世界の罹患率の約30%を占めており、多国籍企業は地方の償還制度に合わせた市場参入計画を立てています。米国と西欧における高齢化も、新規治療法の対象となる患者数を増やしています。これらの疫学的パターンは、次世代の固形腫瘍治療薬の安定した需要を保証しています。
2. 標的療法および免疫腫瘍療法における技術進歩:
抗体薬物複合体(ADC)は最もダイナミックな治療法となっており、2023年の売上高100億米ドルから2033年には推定390億米ドルに拡大すると見込まれています。後期段階のADC資産の80%が固形腫瘍を標的としています。HER2低発現乳がんに対するトラスツズマブ デルクステカンや肺がんに対するダトポタマブ デルクステカンなどの画期的な承認は、化学療法と比較して50%を超える無増悪生存期間の改善をもたらしています。PD-1阻害剤とCTLA-4阻害剤および標準化学療法の併用は、転移性非小細胞肺がん(NSCLC)において、化学療法単独の11%と比較して18%の5年全生存率を達成しています。アルゴリズム駆動型創薬プラットフォームの成熟に伴い、企業は創薬期間を短縮するために10億米ドル以上をAIパートナーシップに投じています。これらの科学的進歩は、固形腫瘍治療薬市場の長期的な拡大への信頼を強化しています。
3. 精密医療とコンパニオン診断の採用拡大:
ROME試験の実世界データによると、組織およびリキッドバイオプシープロファイルに合わせた治療は、従来の治療法における7.7ヶ月を上回る11.05ヶ月の中央全生存期間を延長することが示されています。マイクロサテライト不安定性高発現腫瘍におけるペムブロリズマブのような腫瘍非特異的承認は、バイオマーカースクリーニングプログラムを促進しています。リキッドバイオプシー技術は、侵襲的な処置を回避することでアクセスギャップを縮小しています。循環腫瘍DNAアッセイは現在、耐性変異のモニタリングに標準的に使用されています。これらの進歩にもかかわらず、多遺伝子パネルの償還は依然として一貫性がなく、低所得市場での普及を遅らせています。しかし、分子検査能力の拡大は、固形腫瘍治療薬市場の将来の軌道にとって不可欠です。
4. がん研究における政府および民間資金の増加:
世界のがん治療薬支出は2028年までに4,090億米ドルに達すると予測されており、2023年に開始された2,000件以上の新規臨床試験がこれを後押ししています。中国は規制経路を合理化した後、これらの試験の39%を占め、米国はファースト・イン・ヒューマン試験で主導的地位を維持しています。ベンチャーキャピタルは、変動の激しい株式市場の中でも、固形腫瘍に対するCAR-T細胞やアルファ線放出放射性医薬品などの高リスクプログラムを引き続き支援しています。米国の「Cancer Moonshot」や中国の「Healthy China 2030」のような公的イニシアチブは、トランスレーショナル研究に資金を投入しています。これらの資金調達メカニズムは、固形腫瘍治療薬市場の持続的な成長に不可欠な活発なパイプラインを支えています。
市場の抑制要因
1. がん治療薬に対する厳格な規制承認プロセス:
がん治療薬の開発期間の中央値は依然として10~15年であり、第I相から承認までの失敗率は90%を超えます。FDAの2021年の価値志向のガイダンスは、アクティブコンパレーターデータの要求を伴い、臨床試験の複雑さを増しています。併用療法は、複数の腫瘍タイプにわたる多腕試験を必要とし、さらにリソースを圧迫します。中国の優先審査制度は承認期間を263.5日に短縮しましたが、依然として広範な有効性エビデンスが必要であり、商業化を最大3年間遅らせる可能性があります。これらの累積的な影響は、固形腫瘍治療薬市場の短期的な成長速度を抑制しています。
2. 高額な治療費が患者アクセスを制限:
新規固形腫瘍治療薬の定価は、年間治療費が20万米ドルを超えることが多く、多くの新興国の国民一人当たりの医療予算をはるかに上回っています。バイオシミラーのトラスツズマブは取得費用を最大90%削減しましたが、医師の慎重な姿勢や複雑な支払者フォーミュラリーによって普及が妨げられています。東南アジアから北米への医療ツーリズムの流れは、自国では手頃な価格ではない治療法に対する国境を越えた需要を示しています。段階的価格設定や自己負担支援プログラムは手頃な価格を改善しますが、大規模に普及することは稀です。結果として、価格感応度は固形腫瘍治療薬市場の構造的なブレーキとなっています。
セグメント分析
1. がんの種類別: 乳がんの優位性がイノベーションパイプラインを牽引
乳がんは2024年の収益の25.67%を占め、固形腫瘍治療薬市場で最大のシェアを維持しました。トラスツズマブ デルクステカンによって可能になったHER2低発現分類は、治療可能な患者群を60%拡大し、収益成長を加速させました。2番目に大きいセグメントである肺がんは、EGFR変異を有するステージIII疾患におけるオシメルチニブの39.1ヶ月の中央無増悪生存期間から恩恵を受けました。
前立腺がんは、乏転移性疾患における無増悪期間を延長する転移指向型アプローチに支えられ、2030年までに10.34%のCAGRで最も速く成長すると予測されています。結腸直腸がんプログラムでは全切除療法が評価されており、子宮頸がんの動態はHPVワクチン接種が有病率パターンを変化させるにつれて変化しています。膵臓がんおよび神経内分泌腫瘍における腫瘍治療電場から新規免疫調節剤に至るイノベーションは、固形腫瘍治療薬業界全体の収益源を多様化させています。
2. 薬剤の種類別: ベバシズマブのリーダーシップは新たなADCによって挑戦される
ベバシズマブは2024年の収益の12.45%を占め、固形腫瘍治療薬市場で最大のシェアを占めましたが、バイオシミラーが価格圧力をかけています。カルボプラチン、シスプラチン、パクリタキセルは、手頃な価格と臨床的な馴染みやすさから、低資源環境で依然として主要な薬剤です。
シスプラチンは、プラチナ製剤ベースの化学療法がチェックポイント阻害剤と併用された場合に免疫活性化を促進することを示す研究により、2030年までに12.45%のCAGRで成長する態勢が整っています。エルロチニブ、スニチニブ、エベロリムスなどの低分子標的薬は、併用療法プログラムを通じて勢いを取り戻しています。エベロリムスとランレオチドの併用は、消化管膵神経内分泌腫瘍(NETs)において無増悪生存期間を29.7ヶ月に延長しました。CAR-T細胞、放射性医薬品、二重特異性抗体などの急速に台頭する治療法は、固形腫瘍治療薬業界のさらなる多様化を示唆しています。
3. 投与経路別: 静脈内投与の優位性は経口投与の挑戦に直面
静脈内投与は2024年に46.54%の収益を維持し、病院の注入サービスを支える併用療法の基盤であり続けています。モノクローナル抗体の皮下投与製剤は、治療時間を短縮しており、支払者は施設費用を削減するために外来治療への移行を奨励しています。
経口薬は、患者の利便性とチロシンキナーゼ阻害剤およびCDK4/6阻害剤の成功に牽引され、10.67%のCAGRが予測されています。高効力、低分子量化合物へのスポンサーの注力は、静脈内投与の標準薬の経口再製剤化パイプラインを拡大しています。腫瘍内投与および埋め込み型送達システムは、局所制御のために進歩しており、固形腫瘍治療薬市場における投与経路の選択肢を広げています。
地域分析
北米は2024年に42.43%の収益シェアを占め、高額な価格設定、広範な保険適用、充実した臨床試験ネットワークが新規薬剤の迅速な採用を支えました。がん診療の継続的な統合は、流通業者の交渉力を強化していますが、高額薬剤に対する支払者の監視は厳しさを増しています。
欧州は2番目に大きい地域であり、ドイツ、英国、フランスがEMAの協調的な枠組みの下で先進治療法の採用を主導しています。参照価格設定と医療技術評価(HTA)の審査は、定価のインフレを抑制し、メーカーに機密割引の交渉を促していますが、それでも固形腫瘍治療薬市場にとって魅力的なマージンを維持しています。
アジア太平洋地域は、2030年までに9.54%のCAGRで最も速く成長している地域です。中国は2024年に228件の新規医薬品を承認し、その37%が抗悪性腫瘍薬であったことから、創薬および商業化のハブへと変貌しています。国内のイノベーターは新規償還リストへの掲載の71%を確保し、日本とインドは効率的な立ち上げ期間と未治療患者集団により臨床試験投資を獲得しました。中東・アフリカおよび南米は長期的な成長の可能性を秘めていますが、限られたインフラと予算の制約が短期的な成長を妨げています。全体として、地理的な多様化は、固形腫瘍治療薬市場内でバランスの取れたエクスポージャーを求める企業にとって不可欠です。
競合状況
市場は中程度の集中度を示しており、大手企業は特許切れに先立ってパイプラインを補充するために競争しながら、成熟したフランチャイズを守っています。ファイザーによるシーゲン社の430億米ドルでの買収や、ブリストル・マイヤーズ スクイブによるカルナ社の140億米ドルでの買収は、失われたブロックバスター収益を相殺できる早期臨床段階の資産への戦略的転換を反映しています。ロシュは2025年に医薬品売上高のリーダーシップを維持すると予想されており、テセントリク、アバスチン、ハーセプチンを活用していますが、トラスツズマブのバイオシミラーは主要市場で価格を最大90%削減しています。
競争は現在、併用療法設計と精密医療プラットフォームに集中しています。アストラゼネカと第一三共は、ADCにおける次世代リンカー・ペイロード技術を用いた二重阻害アプローチを拡大しています。小規模なバイオテクノロジー企業は、膠芽腫や膵臓がんなどの困難な適応症を標的とし、満たされていないニーズの高いニッチ市場で大きな価値を獲得することを目指しています。
デジタル機能は差別化要因となりつつあります。サノフィとFormation Bioのパートナーシップは、機械学習を使用して前臨床候補の選択を加速させており、ノバルティスは化合物最適化のために10億米ドル以上をAIコラボレーションに投じています。結果として、競争優位性は、企業がデータ分析と実世界エビデンスを固形腫瘍治療薬市場における開発および商業化戦略に統合する速度にますます依存しています。
最近の業界動向
* 2025年5月: Novocure社は、PANOVA-3データにおいて、切除不能膵腺がん患者において、腫瘍治療電場とゲムシタビンおよびナブパクリタキセルの併用が、対照群の14.2ヶ月に対し、16.2ヶ月の中央全生存期間を達成したと発表しました。FDAへの申請は2025年後半に予定されています。
* 2025年5月: Candel Therapeutics社は、局所前立腺がんにおけるCAN-2409の第3相結果を報告し、再発リスクの30%減少と80.4%の病理学的完全奏効を示しました。生物学的製剤承認申請は2026年後半に計画されています。
* 2025年4月: Memorial Sloan Ketteringは、ミスマッチ修復欠損直腸がん患者において、ドスタルリマブが100%の完全臨床奏効を可能にし、治療を受けた患者の80%で手術を回避したことを示しました。
* 2025年2月: 中国国家薬品監督管理局(NMPA)は2024年に228件の医薬品申請を承認し、その中には固形腫瘍を標的とするイボネシマブとゴリドシチニブの承認が含まれていました。
* 2025年1月: ダトポタマブ デルクステカンは、前治療歴のある進行NSCLC患者を対象としたTROPION-Lung01試験においてドセタキセルを上回り、二次治療としての規制当局への申請を支持しました。
* 2024年12月: トラスツズマブ デルクステカンは、ホルモン受容体陽性、HER2低発現転移性乳がん患者において、化学療法による8.1ヶ月に対し、13.2ヶ月の無増悪生存期間を達成しました。
このレポートは、固形腫瘍治療薬市場に関する詳細な分析を提供しています。固形腫瘍治療薬は、乳がん、肺がん、大腸がん、前立腺がん、子宮頸がんなど、様々な固形腫瘍を特異的に治療する医薬品と定義されています。
主要な市場動向と予測:
固形腫瘍治療薬市場は、2025年に2,072.9億米ドルに達すると推定されています。2025年から2030年にかけては、年平均成長率(CAGR)8.21%で成長し、約1,000億米ドルの新規収益が加わると予測されています。
特に、抗体薬物複合体(ADC)は、標的送達と高効力ペイロードを組み合わせることで生存率向上に貢献し、投資が増加しており、その売上は2033年までに4倍になると見込まれています。
市場を牽引する要因:
市場の成長を促進する主な要因は以下の通りです。
* 世界的ながん罹患率および有病率の上昇。
* 標的療法や免疫腫瘍療法における技術革新。
* 精密医療とコンパニオン診断の普及拡大。
* がん研究への政府および民間資金の増加。
* 抗体薬物複合体や放射性リガンド療法の画期的な承認。
* 創薬および臨床意思決定支援における人工知能(AI)の統合。
市場の阻害要因:
一方で、市場の成長を妨げる要因も存在します。
* がん治療薬に対する厳格な規制承認プロセス。
* 高額な治療費による患者アクセスの制限。
* 新興経済国における償還および価格設定の課題。
* 複雑なバイオ医薬品の製造能力の制約。
市場セグメンテーション:
レポートでは、市場を以下の主要なセグメントに分類して分析しています。
* がんの種類別: 乳がん、肺がん、大腸がん、前立腺がん、子宮頸がん、その他の種類。乳がんは2024年の総収益の25.67%を占め、市場を牽引しています。
* 薬剤の種類別: カルボプラチン、シスプラチン、ゲムシタビン、パクリタキセル、ドキソルビシン、ベバシズマブ、エルロチニブ、スニチニブ、エベロリムス、その他の薬剤。
* 投与経路別: 静脈内投与、経口投与、皮下投与、腫瘍内投与、その他の投与経路。経口製剤は、患者の利便性から年平均成長率10.67%で最も急速に成長しています。
* 地域別: 北米、欧州、アジア太平洋、中東・アフリカ、南米。アジア太平洋地域は、中国、日本、インドでの臨床試験拡大と承認加速により、年平均成長率9.54%で最も急速な成長が予測されています。
競争環境と将来展望:
市場には、Abbott Laboratories、Amgen, Inc.、AstraZeneca PLC、Bristol-Myers Squibb Company、Eli Lilly and Company、F. Hoffmann-La Roche AG、Merck & Co.、Pfizer, Inc.、Novartis AG、Daiichi Sankyo、Johnson & Johnson、Takeda Pharmaceutical Companyなど、多数の主要企業が存在し、競争が激化しています。レポートでは、これらの企業のプロファイル、市場集中度、市場シェア分析も含まれており、未開拓の領域や満たされていないニーズの評価を通じて、将来の市場機会についても言及しています。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
-
4.1 市場の推進要因
- 4.1.1 世界的な癌の発生率と有病率の上昇
- 4.1.2 標的療法および免疫腫瘍療法における技術的進歩
- 4.1.3 精密医療とコンパニオン診断の採用拡大
- 4.1.4 腫瘍学研究における政府および民間資金の増加
- 4.1.5 抗体薬物複合体および放射性リガンド療法の画期的な承認
- 4.1.6 創薬および臨床意思決定支援における人工知能の統合
-
4.2 市場の阻害要因
- 4.2.1 腫瘍薬に対する厳格な規制承認プロセス
- 4.2.2 患者アクセスを制限する高額な治療費
- 4.2.3 新興経済国における償還および価格設定の課題
- 4.2.4 複雑なバイオ医薬品の製造能力の制約
- 4.3 規制環境
-
4.4 ポーターの5つの力分析
- 4.4.1 新規参入の脅威
- 4.4.2 買い手/消費者の交渉力
- 4.4.3 供給者の交渉力
- 4.4.4 代替品の脅威
- 4.4.5 競争の激しさ
5. 市場規模と成長予測 (金額、米ドル)
-
5.1 癌の種類別
- 5.1.1 乳癌
- 5.1.2 肺癌
- 5.1.3 結腸直腸癌
- 5.1.4 前立腺癌
- 5.1.5 子宮頸癌
- 5.1.6 その他の癌の種類
-
5.2 薬剤の種類別
- 5.2.1 カルボプラチン
- 5.2.2 シスプラチン
- 5.2.3 ゲムシタビン
- 5.2.4 パクリタキセル
- 5.2.5 ドキソルビシン
- 5.2.6 ベバシズマブ
- 5.2.7 エルロチニブ
- 5.2.8 スニチニブ
- 5.2.9 エベロリムス
- 5.2.10 その他の薬剤の種類
-
5.3 投与経路別
- 5.3.1 静脈内
- 5.3.2 経口
- 5.3.3 皮下
- 5.3.4 腫瘍内
- 5.3.5 その他の投与経路
-
5.4 地域別
- 5.4.1 北米
- 5.4.1.1 米国
- 5.4.1.2 カナダ
- 5.4.1.3 メキシコ
- 5.4.2 欧州
- 5.4.2.1 ドイツ
- 5.4.2.2 英国
- 5.4.2.3 フランス
- 5.4.2.4 イタリア
- 5.4.2.5 スペイン
- 5.4.2.6 その他の欧州
- 5.4.3 アジア太平洋
- 5.4.3.1 中国
- 5.4.3.2 日本
- 5.4.3.3 インド
- 5.4.3.4 オーストラリア
- 5.4.3.5 韓国
- 5.4.3.6 その他のアジア太平洋
- 5.4.4 中東・アフリカ
- 5.4.4.1 GCC
- 5.4.4.2 南アフリカ
- 5.4.4.3 その他の中東・アフリカ
- 5.4.5 南米
- 5.4.5.1 ブラジル
- 5.4.5.2 アルゼンチン
- 5.4.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
-
6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要事業セグメント、財務、従業員数、主要情報、市場順位、市場シェア、製品とサービス、および最近の動向の分析を含む)
- 6.3.1 アボット・ラボラトリーズ
- 6.3.2 アムジェン
- 6.3.3 アストラゼネカ
- 6.3.4 バクスター・インターナショナル
- 6.3.5 ベーリンガーインゲルハイム
- 6.3.6 ブリストル・マイヤーズ スクイブ
- 6.3.7 イーライリリー・アンド・カンパニー
- 6.3.8 F. ホフマン・ラ・ロシュ
- 6.3.9 GSK
- 6.3.10 メルク & Co.
- 6.3.11 ファイザー
- 6.3.12 ノバルティス
- 6.3.13 シーゲン
- 6.3.14 第一三共
- 6.3.15 ジョンソン・エンド・ジョンソン
- 6.3.16 サノフィ
- 6.3.17 武田薬品工業
- 6.3.18 バイエル
- 6.3.19 エーザイ
- 6.3.20 ベイジーン
- 6.3.21 リジェネロン
- 6.3.22 エクセリクシス
- 6.3.23 イノベント
7. 市場機会 & 将来展望
*** 本調査レポートに関するお問い合わせ ***

固形がん治療薬とは、臓器や組織に塊として形成される固形がんの増殖を抑制し、縮小、あるいは消失させることを目的とした薬剤の総称でございます。肺がん、乳がん、胃がん、大腸がん、肝臓がん、膵臓がんなど、多岐にわたるがん種が固形がんに分類されます。これらの治療薬は、がんの根治を目指すだけでなく、進行がんにおいては病状の進行を遅らせ、患者様の延命や生活の質の向上を図る上で極めて重要な役割を担っております。近年、がん研究の進展に伴い、その種類と作用機序は多様化し、治療成績の向上に大きく貢献しております。
固形がん治療薬は、その作用機序によって大きくいくつかの種類に分類されます。まず、化学療法薬は、がん細胞の増殖を直接的に阻害する薬剤であり、DNA合成阻害剤や細胞分裂阻害剤などが含まれます。これらはがん細胞だけでなく正常細胞にも影響を与えるため、骨髄抑制、脱毛、吐き気などの副作用が課題となることがございます。次に、分子標的薬は、がん細胞に特異的に発現する分子(受容体や酵素など)を標的とし、がんの増殖や生存に必要なシグナル伝達を阻害することで効果を発揮します。EGFR阻害薬やALK阻害薬、VEGF阻害薬などが代表的であり、特定の遺伝子変異を持つ患者様に対して高い効果が期待され、化学療法薬に比べて副作用が比較的少ない場合もございます。
さらに、近年目覚ましい進歩を遂げているのが免疫チェックポイント阻害薬でございます。これは、がん細胞が免疫細胞にかける「ブレーキ」を解除し、患者様自身の免疫力を活性化させてがんを攻撃させる薬剤です。PD-1阻害薬、PD-L1阻害薬、CTLA-4阻害薬などが開発され、肺がん、悪性黒色腫、腎細胞がんなど幅広いがん種で長期的な効果が報告されております。また、乳がんや前立腺がんなど、ホルモンががんの増殖に関与する場合には、ホルモンの作用を阻害または抑制するホルモン療法薬が用いられます。これら以外にも、がん溶解性ウイルス療法や遺伝子治療、細胞療法(CAR-T細胞療法など)といった新たなアプローチも固形がんへの応用を目指し、研究開発が進められております。
固形がん治療薬の用途は多岐にわたります。単一の薬剤で治療を行う単剤療法のほか、複数の薬剤を組み合わせることで相乗効果を高めたり、薬剤耐性の出現を遅らせたりする併用療法が広く行われております。例えば、化学療法と分子標的薬、あるいは免疫チェックポイント阻害薬と化学療法を組み合わせることで、より高い治療効果を目指すことがございます。また、手術前に腫瘍を縮小させて切除率を高める術前補助療法や、手術後に残存する可能性のあるがん細胞を排除し再発を予防する術後補助療法としても用いられます。進行・再発がんに対しては、病状の進行を抑制し、患者様の延命や症状緩和、生活の質の維持・向上を目的として継続的に投与されることが一般的でございます。近年では、患者様個々のがんの遺伝子変異や特性に基づいて最適な薬剤を選択する個別化医療(プレシジョン・メディシン)が主流となりつつあり、治療効果の最大化と副作用の最小化が図られております。
固形がん治療薬の進歩を支える関連技術も多岐にわたります。まず、診断技術の進化は個別化医療の実現に不可欠でございます。次世代シークエンサーを用いた遺伝子パネル検査(NGS)により、がんの遺伝子変異を網羅的に解析し、最適な分子標的薬や免疫チェックポイント阻害薬の選択が可能となりました。また、血液からがん細胞由来のDNAなどを検出するリキッドバイオプシーは、非侵襲的にがんの診断や治療効果のモニタリングを可能にし、治療戦略の迅速な変更に貢献しております。薬剤をがん組織に選択的に送達し、全身への副作用を軽減する薬剤送達システム(DDS)も重要な技術であり、ナノ粒子製剤やリポソーム製剤、そして抗体と薬物を結合させた抗体薬物複合体(ADC)などが開発され、治療効果の向上に寄与しております。さらに、治療効果や副作用を予測するバイオマーカーの開発、そして新薬開発の効率化や個別化医療の推進に貢献するAI(人工知能)やビッグデータ解析も、今後の固形がん治療薬の発展において不可欠な要素となっております。
固形がん治療薬の市場は、世界的に見ても非常に大きく、今後も成長が予測されております。高齢化社会の進展に伴うがん患者数の増加や、新規作用機序を持つ革新的な薬剤の登場が市場拡大の主要な要因でございます。特に、分子標的薬や免疫チェックポイント阻害薬は、その高い治療効果と幅広いがん種への適用拡大により、市場を牽引しております。多くの製薬企業が研究開発に巨額の投資を行い、新規薬剤の開発競争が激化している状況でございます。一方で、高額な新薬の登場は医療費の増大という課題も生み出しており、費用対効果の評価や薬価制度の見直しが各国で議論されております。また、患者様への早期アクセスを可能にするための迅速承認制度や条件付き早期承認制度など、規制当局の動向も市場に大きな影響を与えております。
将来の固形がん治療薬は、さらなる個別化医療の深化を目指して進化していくと考えられます。より精密なバイオマーカーの発見や、多遺伝子解析に基づく治療戦略の確立、そしてAIを活用した治療選択支援システムの導入が進むでしょう。また、がん微小環境を標的とする薬剤や、がん細胞の新たな脆弱性を突く新規作用機序の薬剤開発も活発化すると予測されます。免疫チェックポイント阻害薬と他の治療法(化学療法、放射線療法、分子標的薬など)との最適な併用療法の確立も重要な研究課題であり、これにより治療効果の最大化と薬剤耐性の克服が期待されます。副作用の予測バイオマーカーの開発や支持療法の改善により、患者様の治療負担の軽減も図られるでしょう。さらに、実際の臨床現場で得られるリアルワールドデータを活用することで、治療効果や安全性の評価がより精緻になり、新たな治療戦略の発見にも繋がると考えられます。固形がん治療薬は、がんの予防や超早期発見技術との連携も深めながら、がんという難病の克服に向けて、今後も革新的な進歩を遂げていくことでしょう。