細胞および遺伝子治療の臨床試験市場の規模と展望、2026-2034

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
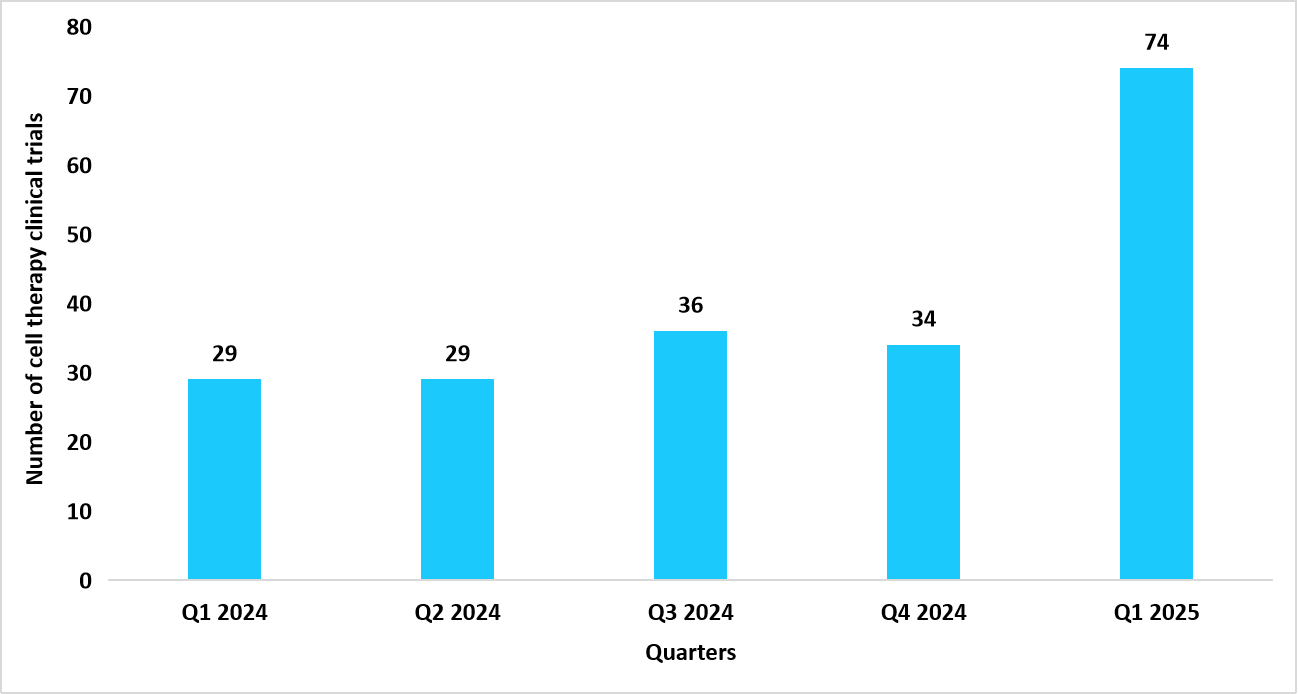
細胞および遺伝子治療の臨床試験市場は、2025年に139.3億米ドル、2034年には502.7億米ドルに達すると予測されており、予測期間中の年平均成長率(CAGR)は15.37%と見込まれています。この市場の持続的な成長は、臨床試験の数が増加していることに起因しており、これらの試験は新しい治療法の安全性、効果、および治療の可能性を検証する上で重要な役割を果たしています。
細胞および遺伝子治療の臨床試験市場は、細胞および遺伝子材料を修正してさまざまな病気を治療、予防、または潜在的に治癒するための革新的な治療介入の安全性、効果、長期的な結果を評価するための研究開発活動を含んでいます。この市場は、臨床試験の段階(フェーズI、フェーズII、フェーズIII、フェーズIV)や、腫瘍学、心臓病、筋骨格疾患、感染症、皮膚科、免疫学と炎症、眼科、血液学、消化器病などの適応症に基づいて分類されます。
細胞および遺伝子治療の臨床試験市場は、先進的な治療法のパイプラインの拡大、規制の支援の増加、さまざまな疾患領域における臨床成功率の向上によって、バイオテクノロジーおよび製薬分野における変革的なセグメントとして位置付けられています。
最近、米国食品医薬品局(FDA)は、「小規模集団における細胞および遺伝子治療製品の臨床試験のための革新的なデザイン」という草案指針を発表し、単腕試験、ベイズモデル、外部対照試験などの柔軟な方法論の使用を奨励しています。この移行は、データの整合性と患者の安全性を維持しながら、治療の開発を加速させることを目的としています。さらに、個別化自家療法から、標準化された生産と広範な臨床アクセスのためにドナー由来の細胞を使用する同種「オフ・ザ・シェルフ」療法への移行は、市場の成長を促進しています。
細胞および遺伝子治療の臨床試験市場の主要な推進要因は、治療法の開発の精度、安全性、スケーラビリティを向上させるゲノム編集技術とデリバリープラットフォームの急速な進展です。例えば、2025年3月、CRISPR Therapeuticsは、ベータサラセミアを対象とした高度なCRISPR Cas12aベースの臨床試験を開始し、オフターゲット効果を減少させながら遺伝子編集の効率を向上させることを発表しました。これらの技術的な進展は、試験の成功率を向上させ、複雑な遺伝病、腫瘍学的疾患、稀な病気に対する治療のパイプラインを拡大しています。
一方で、細胞および遺伝子治療の臨床試験市場には、試験承認や患者の安全性に関連する複雑な倫理的考慮事項やコンプライアンス要件が大きな制約要因として存在しています。FDAおよびEMAによると、CGT試験は、遺伝子改変および細胞ベースの治療の高リスク性により、広範な前臨床検証、長期的な安全性監視、厳格な製造基準を要求します。これにより、承認プロセスが長引き、運営コストが増加し、特に小規模なバイオテクノロジー企業にとって臨床プログラムのスケーリングが困難になることがあります。
また、細胞および遺伝子治療の臨床試験市場には、再生医療における研究および治療の進展を加速するために、政府や国際機関からの大規模な資金提供や投資が重要な機会を提供しています。例えば、2025年1月、米国国立衛生研究所(NIH)は、希少遺伝性疾患および腫瘍学に焦点を当てた大規模な臨床試験と翻訳研究を支援するために、体細胞ゲノム編集(SCGE)プログラムの下で9億5000万ドルの資金を発表しました。この資金は、臨床試験のエコシステムを強化し、インフラを向上させ、バイオテクノロジーのコラボレーションを支援し、患者リクルートネットワークを拡大します。
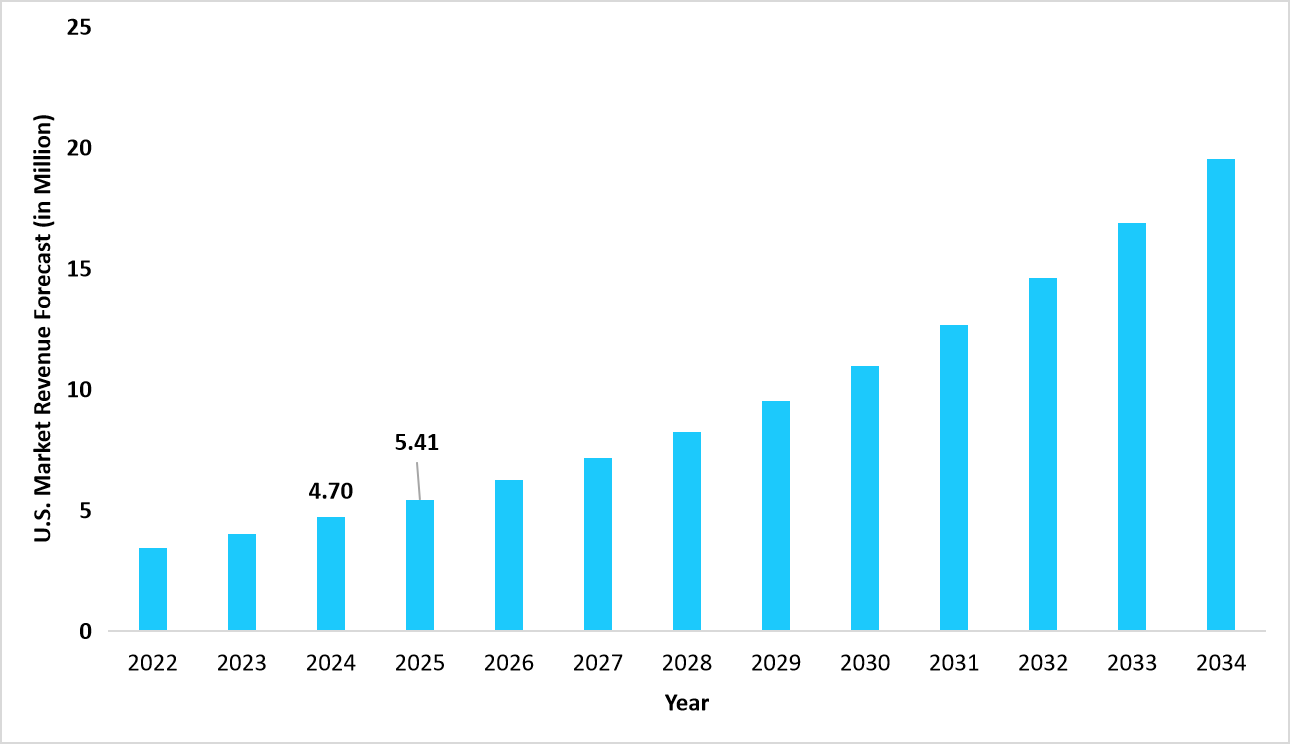
北米地域は、2025年に43.17%の収益シェアを持って市場を支配しています。この成長は、希少疾患や孤児疾患に特化した試験ネットワークおよび高度な臨床インフラの強力な存在に起因しています。米国の細胞および遺伝子治療の臨床試験市場の主な推進要因は、再生医療の進展に向けたベンチャーキャピタルおよび政府の資金の流入です。
アジア太平洋地域は、地域におけるバイオ製造能力の急速な拡大と臨床試験の実施に向けた地元のパートナーシップによって、予測期間中に最も高いCAGR(17.24%)で成長すると予測されています。中国、日本、韓国、シンガポールなどの国々は、先進的なバイオプロセシング施設およびウイルスベクター生産に多額の投資を行い、グローバルなバイオテクノロジー企業を引き寄せています。
インド市場は、遺伝性疾患や希少疾患の有病率の上昇、患者の認識向上、診断能力の向上によって推進されています。進んだゲノム検査と精密診断が主要病院や私立のラボで利用可能になることで、細胞および遺伝子治療の臨床試験に適した患者の早期特定が可能になっています。
ヨーロッパ市場は、高度な治療法の製造拠点および特化した臨床試験施設への投資が増えていることによって推進されています。ドイツ、英国、オランダなどの国々は、ベクター生産から患者への供給までのエンドツーエンドの臨床開発を支援するために、GMP認証を受けた細胞および遺伝子治療センターの設立を進めています。
中東およびアフリカ市場は、精密医療およびゲノム研究インフラの開発に対する政府の関心が高まっていることにより、安定的に拡大しています。
ラテンアメリカ市場は、地域の病院が多国籍臨床試験に参加することによって拡大しています。
フェーズIIIセグメントは、59.28%のシェアを持って市場を支配しており、これは後期のパイプライン候補が増加していることに起因しています。腫瘍学セグメントは、2025年に48.37%の収益シェアを持っており、白血病やリンパ腫、固形腫瘍を含むさまざまながんを対象とした細胞および遺伝子治療の臨床試験の高い数によって支えられています。
Report Coverage & Structure
細胞および遺伝子治療の臨床試験レポートの構造概要
本レポートは、細胞および遺伝子治療の臨床試験に関する詳細な分析を提供するもので、以下のように複数のセクションに分かれています。
1. イントロダクション
最初のセクションでは、研究の目的や範囲が明確に定義され、細胞および遺伝子治療の臨床試験市場に関する基本的な情報が提供されます。この部分では、研究の制限や仮定も示され、全体の市場スコープが概観されます。
2. 市場機会の評価
このセクションでは、細胞および遺伝子治療の臨床試験市場における新たな機会や成長ポテンシャルが探求されます。特に、新興地域や企業、応用分野が焦点となります。
3. 市場動向
ここでは、細胞および遺伝子治療の臨床試験市場に影響を与える主要なドライバーや警告要因が分析されます。また、最新のマクロ経済指標や地政学的影響、技術要因も取り上げられ、全体的な市場環境が評価されます。
4. 市場評価
このセクションでは、ポーターのファイブフォース分析やバリューチェーン分析を通じて、細胞および遺伝子治療の臨床試験市場の競争状況や価値の流れが詳述されます。
5. 規制フレームワーク
北米、欧州、アジア太平洋、中東・アフリカ、ラテンアメリカの各地域における規制の枠組みが分析され、各地域の市場特性や規制の違いが説明されます。
6. ESGトレンド
環境、社会、ガバナンスに関連するトレンドが市場に与える影響についても考察され、持続可能性の観点から細胞および遺伝子治療の臨床試験市場がどう変化しているかが示されます。
7. 市場規模分析
細胞および遺伝子治療の臨床試験市場の規模が、フェーズ別および適応症別に詳しく分析されます。各フェーズ(フェーズI、II、III、IV)や、適応症(腫瘍学、心臓病、筋骨格系疾患、感染症、皮膚科、免疫学・炎症、眼科、血液学、消化器疾患、その他)に基づいて、具体的な市場データが提供されます。
8. 地域別市場分析
北米、欧州、アジア太平洋、中東・アフリカの各市場における細胞および遺伝子治療の臨床試験の状況が詳細に分析され、各地域の市場特性や成長機会が強調されます。
このレポートは、細胞および遺伝子治療の臨床試験市場に関する包括的な理解を提供し、業界関係者が意思決定を行うための重要なインサイトをもたらします。
*** 本調査レポートに関するお問い合わせ ***

細胞および遺伝子治療の臨床試験とは、病気の治療において、細胞や遺伝子を使用する新しい医療手法の安全性と効果を評価するために実施される試験のことを指します。これらの治療法は、特定の疾患の治療や予防を目的としており、通常の薬物治療や外科手術では効果が見込めない場合に特に重要な役割を果たします。
細胞治療は、患者自身の細胞や他者から提供された細胞を使用して、病気の治療を行います。例えば、幹細胞を用いた治療は、再生医療の分野で注目されています。幹細胞は、さまざまな細胞に分化する能力を持ち、それを利用することで損傷した組織や臓器を修復することが可能です。一方、遺伝子治療は、遺伝子の改変や補充を通じて、遺伝性疾患やがんなどの治療を目指します。具体的には、欠損している遺伝子を補う、異常な遺伝子を修正する、または新たな機能を持つ遺伝子を導入する方法があります。
臨床試験は、これらの治療法が実際に患者に対してどのように機能するかを科学的に評価するために不可欠です。臨床試験は通常、段階を追って行われます。第1相試験では主に安全性が評価され、第2相試験では効果が検討されます。第3相試験では、より多くの患者を対象にして、他の治療法と比較することにより、治療法の有効性と安全性を確立します。
細胞および遺伝子治療の臨床試験は、特に難治性の疾患に対する新たな治療法の開発において重要な役割を果たしています。たとえば、遺伝性の血液疾患や特定のがんに対する遺伝子治療は、革新的な治療法として期待されています。また、これらの治療法は、個別化医療の進展とも密接に関連しており、患者一人ひとりの遺伝的背景や病歴に基づいたオーダーメイドの治療が可能になることも目指しています。
さらに、細胞および遺伝子治療の研究は、さまざまな関連技術の発展とも結びついています。例えば、CRISPR-Cas9技術は、遺伝子編集の革新をもたらし、特定の遺伝子の改変を容易に行えるようにしました。また、細胞培養技術やバイオマーカーの発見、データ解析技術の進展も、臨床試験の質を向上させる要因となっています。
細胞および遺伝子治療の臨床試験は、今後の医療において重要な役割を果たすことが期待されており、さまざまな疾患に対する新しい治療法の開発が進む中で、研究者や医療従事者はその安全性と有効性を確保するために日々努力しています。このような試験を通じて、未来の医療がより効果的で患者に優しいものになることを願っています。