治験用物資市場の規模と見通し、2025-2033

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
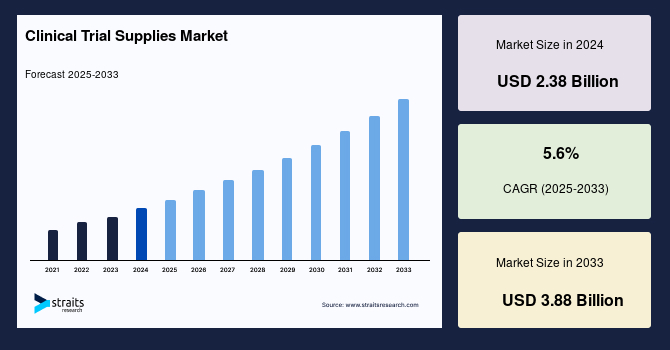
世界の治験用物資市場は、2024年に23.8億米ドルの規模と評価され、2025年には25.1億米ドルから2033年には38.8億米ドルに達すると予測されており、予測期間(2025年~2033年)中のCAGRは5.6%を示しています。治験サイトの拡大やバイオ医薬品とバイオシミラーの研究開発の増加が市場を後押ししています。治験用物資は、成功する治験のために必要不可欠な一連の素材とリソースを含みます。これらの物資の中心には、調査対象となる治験薬、バイオ医薬品、および医療機器があります。これらの治験薬は、その潜在的な治療効果に基づいて慎重に選択され、治験に使用される前に厳密な試験と評価を受けます。通常、治験のスポンサーまたは製造業者がこれらを提供し、品質、安全性、および有効性の規制要件を満たす必要があります。
さらに、治験用物資には、プラセボが含まれています。プラセボは、調査中の治療薬と同様に見えるように設計された不活性物質で、調査中の治療薬の特定の効果を評価し、プラセボ効果から区別するために使用されます。プラセボは、調査中の治療薬の真の有効性を確立し、偏りのない結果を保証するために重要です。加えて、治験用物資には、ラベルや包装、ランダム化キット、試験特有の書類や文書、サンプル収集と分析のための研究室用品など、さまざまな補助材料が含まれる場合があります。これらの物資は、正確な文書化、製品の一貫性の維持、治験の円滑な運営を保証するために不可欠です。
治験用物資における品質と規制の遵守は極めて重要です。それらは、良好な製造実践(GMP)やその他の関連ガイドラインを遵守し、高品質の物資が汚染されず、正確にラベル付けされていることを保証する必要があります。厳格な在庫管理は、治験用物資の適切な管理と説明責任を維持するために重要です。
現在、多くの治験は発展途上国で行われています。治験のコストの増加と患者募集の複雑さが、バイオ医薬品企業にアジア太平洋、ラテンアメリカ、中央および東ヨーロッパ、中東などの地域に治験をアウトソーシングすることを奨励しています。発展途上国における疾患の多様性は、バイオ医薬品企業が希少疾患に関する治験を実施することを助けています。例えば、アジア太平洋地域は、シンガポールや中国の政府が生物医学研究を促進するために資金を割り当てているため、バイオ医薬品企業にとってより大きな経済的利益を提供しています。ラテンアメリカでは、言語の壁が低いため、患者募集が容易であり、インフォームドコンセントを容易に取得できるため、治験プロセスが迅速になります。
治験におけるバイオ医薬品および温度感受性医薬品の顕著な増加が見られます。現在、医薬品の38.0%は温度感受性があり、後期段階の医薬品の35.0%はバイオ医薬品です。この数値は、バイオ医薬品の需要が増加しているため、増加すると予測されます。バイオ医薬品は従来の薬剤に比べて副作用が少ないため、温度感受性医薬品の保管に対する要求が高まっています。したがって、治験におけるバイオ医薬品の増加は、コールドチェーン施設の需要を増やすと期待されています。2022年までにトップ10のバイオ医薬品のうち8つがコールドチェーン施設を必要とすると推定されています。開発途上国および先進国におけるバイオシミラーの高い需要は、コールドチェーン供給をさらに促進し、予測期間中に治験用物資市場の成長に寄与すると予測されています。
世界市場にとって最大の課題は、地域ごとの規制の多様性と倫理的ジレンマです。各国には個別の出荷要件があります。加えて、各製薬会社は試験薬の保管要件が異なります。世界の治験用物資市場は、アウトソーシングと治験管理プロセスの合理化において大きな機会を提供します。製薬会社およびバイオテクノロジー企業は、財政的負担を減らし、医薬品発見を加速するための戦略的アプローチとしてアウトソーシングにますます頼っています。この傾向は、専門的な治験用物資会社や契約研究機関(CRO)にとって、複数の治験を管理するための包括的なサービスとソリューションを提供する機会を創出します。
治験用物資と管理のアウトソーシングにはいくつかの利点があります。まず、製薬会社やバイオテクノロジー企業が研究開発などの主要な能力に集中できるようになります。一方で、治験の物流、包装、ラベル付け、配布のために専門的なサービスプロバイダーに依存できます。これらの活動をアウトソーシングすることにより、企業はリソースを最適化し、運営コストを削減し、効率を向上させることができます。
さらに、アウトソーシングにより、専門的な専門知識とインフラへのアクセスが可能になります。治験用物資会社とCROは、治験に関連する複雑な規制要件、品質基準、物流の課題を管理する広範な知識と経験を持っています。彼らはベンダー、保管施設、配布ネットワークとの関係を確立しており、世界中の試験サイトへの物資のタイムリーで適切な配達を保証します。
北アメリカは、世界の治験用物資市場で最も重要なシェアを持ち、予測期間中にCAGR 5.4%で成長すると見込まれています。北アメリカは、すべての地域の中で最も多くの治験が行われており、この地域の市場成長の主要な推進力となっています。治験と市場のプレイヤー数の増加、高度な技術の利用可能性が、この地域の優位性の要因です。治験の大部分は、米国やカナダなどの国で行われています。この地域では英語が広く使用されており、言語の壁が低くなっています。そのため、北アメリカは治験を行うのに好まれています。多くのCROおよびバイオ医薬品会社がこの地域に存在し、技術の進歩とともに効果的な供給の需要が増加しています。したがって、この地域は予測期間中に治験用物資市場シェアの大幅な成長を目撃すると予測されています。
ヨーロッパは、予測期間中にCAGR 5.8%を示すと予測されています。ヨーロッパは、技術の進歩、この地域での治験の増加、革新的なバイオ医薬品会社とCROの存在により、治験用物資の主要市場の一つです。Nice Insightsによるアウトソーシング調査によれば、2016年には西ヨーロッパへのアウトソーシングプロジェクトが11.0%から14.0%に3.0%増加しました。これは、バイオ医薬品企業が確立された市場、例えばヨーロッパや北アメリカで研究を行うことを好むためであり、これらの市場は確立された医療インフラを持っています。東ヨーロッパなどの新興経済国は、迅速なプロセスと費用対効果の高い治験のアウトソーシング市場で急速な成長を示すと期待されています。
アジア太平洋は、世界の治験用物資市場の最も急速に成長する地域の一つと予測されています。臨床研究の大規模な成長が、この国の市場の成長を評価し、したがって、世界市場の拡大に寄与すると予想されます。これらの地域での臨床研究の成長を促進する主な要因には、アジア太平洋諸国での患者1人あたりのコストの低さ、多様な患者群の簡単な募集が含まれます。
ラテンアメリカは、治験サイトの数で最も成長している場所の一つです。その多様な人口、患者への容易なアクセス、北アメリカへの近接性、比較的低い輸送コストが要因となっています。これらの要因が、この地域での治験市場を推進しています。コロンビア、ペルー、チリ、アルゼンチン、メキシコ、ブラジルは、ラテンアメリカの治験の90.0%を占めています。ブラジル、中国、アルゼンチンでの治験申請承認期間を短縮するための最近の規制改革が、市場を後押しすると期待されています。
中東とアフリカは、治験を行うための新興市場の一つであり、質の高いケアの需要の増加、多様な人口、患者募集の容易さが要因です。さらに、この地域はヨーロッパの製薬企業がラテンアメリカよりもアフリカ地域に近接しているため、物流上の利点を提供しています。
フェーズIセグメントは、世界市場を支配しており、予測期間中にCAGR 6.1%を示すと予測されています。フェーズI治験の大部分はアウトソーシングされており、60.0%以上の試験が研究センター、CRO、および学術機関にアウトソーシングされています。サンプル人口の少なさと高い資本投資が、治験の大部分をアウトソーシングする主な要因です。フェーズI治験のアウトソーシングの増加と治験のグローバル化は、フェーズIの治験用物資市場を推進すると期待されています。心血管疾患、中枢神経系、感染症、腫瘍学などの主要な治療分野は、フェーズIプロジェクトの最大数を持っています。この高い活動量は、治験のサプライチェーンの複雑さを増大させ、したがって、世界の治験用物資の需要を増大させると予想されています。
製造セグメントは、世界市場を支配しており、予測期間中にCAGR 5.7%を示すと予測されています。製造セグメントには、薬剤およびプラセボの製造、比較薬の調達、ラベル付けおよび包装が含まれます。治験の増加は、素材供給の高い需要をもたらし、質の高い薬剤の需要を増やしています。複雑な分子とバイオ医薬品の高い需要は、世界市場の製造セグメントを後押しすると期待されています。大部分の素材供給はアウトソーシングされており、効率的な治験用物資の需要を引き上げています。製造におけるアウトソーシングは、複雑な分子を製造するための新しい技術の導入と、費用対効果の高い製品を開発する需要の増加に起因しています。
製薬セグメントは、世界市場を支配しており、予測期間中にCAGR 5.6%を示すと予測されています。研究開発パイプラインでの製薬薬剤の減少が安定しており、それがバイオ薬剤に置き換えられることが予測されており、予測期間中にセグメント成長に悪影響を及ぼすと予測されています。トップ10の革新的な薬剤の中での製薬薬剤の数は大幅に減少しており、バイオ薬剤に置き換えられると予測されています。製薬薬剤は治験セグメントで最も多くの薬剤を占めていますが、バイオ薬剤の増加数がこの数に影響を与える可能性があります。
腫瘍学セグメントは、世界市場を支配しており、予測期間中にCAGR 6.5%を示すと予測されています。腫瘍学の治験は、癌とその症状を発見、治療、制御するのを助けるために行われます。腫瘍学の治験材料は、主包装と二次包装の2種類の包装で提供されます。包装の主な目的は、患者に処方された薬剤を服用させることです。包装は、バイアルを漏れから保護し、エアロゾル化からガスを保護する必要があります。包装は、投与要件に応じて行う必要があります。United Press Internationalによると、米国の病院では、誤った投与量のために何百万もの癌薬のバイアルを廃棄しています。
Report Coverage & Structure
レポートの構造概要
このレポートは、治験用物資市場に関する包括的な分析を提供しており、以下のような主要なセクションで構成されています。
1. セグメンテーションと調査方法論
- このセクションでは、市場のセグメンテーションと調査方法論について説明しています。また、調査の範囲や目的、制限事項、および為替と価格設定の考慮事項が含まれています。
2. 市場機会評価
- 新興地域・国、企業、アプリケーション/エンドユースに関する市場機会が評価されています。
3. 市場動向
- 市場の推進要因、警告要因、最新のマクロ経済指標、地政学的影響、技術要因についてのトレンドが分析されています。
4. 市場評価
- ポーターの5フォース分析やバリューチェーン分析が行われ、規制フレームワークが地域ごと(北米、ヨーロッパ、APAC、中東・アフリカ、LATAM)に詳述されています。
5. ESGトレンド
- 環境、社会、ガバナンス(ESG)に関連するトレンドが取り上げられています。
6. グローバル治験用物資市場規模分析
- 市場の導入部では、フェーズ(フェーズI、II、III、その他)、製品とサービス、エンドユース、治療用途ごとに分析されています。
- それぞれのカテゴリについて、価値ごとの詳細な分析が提供されています。
7. 地域別市場分析
- 北米、ヨーロッパ、APACなど、主要地域ごとに詳細な市場分析が提供されています。
- 各地域では、フェーズ、製品とサービス、エンドユース、治療用途に基づく分析が含まれています。
- 国別(例:アメリカ、カナダ、イギリス、ドイツ、フランス、日本など)に細分化された詳細な評価も含まれています。
このレポートは、グローバルな治験用物資市場の現状と将来の可能性を多角的に分析するための重要な情報を提供しています。
*** 本調査レポートに関するお問い合わせ ***

治験用物資とは、一般的に医薬品や医療機器の開発過程において使用される物資を指します。これは、新しい治療法や医薬品の安全性や有効性を確認するために実施される臨床試験、すなわち治験で用いられる重要な要素です。治験用物資には、試験薬、プラセボ、治験用機器などが含まれます。これらは、適切な規制基準に従って製造され、試験の目的に応じて適切に管理されます。
治験用物資は、その種類によって異なる用途を持ちます。例えば、試験薬は、新しい治療法の有効性を評価するために使用されます。この試験薬は、まだ一般市場に出回っていないため、製造過程から品質管理まで厳密な管理が求められます。一方、プラセボは、試験薬の効果を正確に評価するための対照として用いられます。プラセボは、見た目や味が試験薬と同一であるが、活性成分を含まないという特性を持っています。治験用機器は、医療機器の新たな機能や性能を試験する際に使用され、これも同様に厳しい管理下で使用されます。
これらの治験用物資の使用には、関連する技術や手法が必要です。例えば、試験薬の製造には、GMP(Good Manufacturing Practice)と呼ばれる製造管理及び品質管理の基準が適用されます。この基準は、製品の安全性や品質を確保するために、製造工程全体を通じて厳格な管理を行うことを求めています。また、治験用物資の保管や輸送にも、適切な条件が求められます。これには、温度管理や光の影響を避けるための特別な包装技術が含まれます。
さらに、治験用物資の管理には、電子的なシステムやデータベースが活用されることが一般的です。これにより、物資の追跡や在庫管理が効率的に行われ、治験の進行をスムーズにすることができます。また、これらのシステムは、治験データの正確性や整合性を維持するためにも重要な役割を果たしています。
治験用物資は、治験の成功に不可欠な要素であり、その適切な管理と使用が、新しい医薬品や医療技術の開発において重要な役割を果たしています。これにより、患者にとって安全で効果的な治療法が提供されることが期待されます。