クローン病治療薬市場規模と展望 2025-2033年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
**クローン病治療薬市場の包括的分析:詳細な市場概要、促進要因、抑制要因、機会、およびセグメント分析**
**I. クローン病治療薬市場の概要**
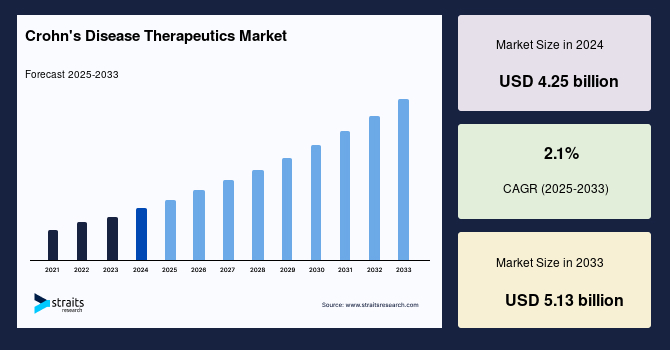
世界のクローン病治療薬市場は、2024年に42.5億ドルの規模を記録し、2025年には43.4億ドル、2033年には51.3億ドルに達すると予測されており、予測期間(2025年~2033年)における年平均成長率(CAGR)は2.1%で推移する見込みです。この成長は、クローン病の有病率の増加と、より効果的で安全な治療法の必要性によって牽引されています。北米地域は、予測期間中に10.50%の複合年間成長率で成長すると予想されており、世界のクローン病治療薬市場において最大のシェアを占める主要なステークホルダーとなるでしょう。
クローン病は、局所性腸炎とも呼ばれる慢性炎症性腸疾患(IBD)の一種であり、異常な免疫系反応によって小腸および大腸の内壁に炎症を引き起こします。この疾患は、消化管のあらゆる部分に影響を及ぼす可能性があり、その炎症は断続的に発生したり、広範囲に及んだりすることがあります。クローン病の主要な病型には、回結腸炎、回腸炎、胃十二指腸炎、および空回腸炎の4つが挙げられます。回結腸炎は小腸と大腸の一部、すなわち結腸の炎症を指し、最も一般的な病型です。回腸炎は小腸(回腸)の炎症と腫れを特徴とします。胃十二指腸炎は胃と小腸の上部(十二指腸)の炎症と刺激が特徴的な症候群です。空回腸炎では、小腸の上半分(空腸)に斑状の炎症が発生します。これらの病型は、症状、診断、および治療アプローチにそれぞれ異なる影響を与えます。
歴史的に、クローン病患者は結腸がんのリスクが高いため、潰瘍性大腸炎と同様に、がんのリスクを低減するために外科的治療が頻繁に用いられてきました。しかし、胃腸手術には感染、辺縁性潰瘍、吸収不良、狭窄などのリスクが伴い、これらのリスクがIBDの治療における外科手術の普及を妨げる要因となっています。
現在のクローン病治療薬の主流は生物学的製剤であり、抗腫瘍壊死因子(TNF)抗体、抗インターロイキン抗体、抗インテグリン抗体などが様々な炎症性疾患、特にクローン病の治療に用いられています。これらは通常、ステロイドやアミノサリチル酸製剤の効果に抵抗性を示す患者にとって満足のいく治療法と見なされています。しかし、一部の患者、特に抗TNF製剤に対しては、治療効果が時間の経過とともに減弱したり、全く反応しなくなったりするケースも存在します。このため、既存の治療法よりも免疫反応を引き起こしにくい新しい治療法の開発が喫緊の課題となっています。
近年、クローン病治療薬市場には多くの新しい治療薬クラスが数年以内に市場に投入される計画があり、注目を集めています。例えば、ステラーラ(ウステキヌマブ)は2016年に承認された最後の生物学的製剤の一つであり、その後の治療選択肢の拡充が期待されています。抗インテグリン阻害剤やインターロイキン阻害剤などの生物学的製剤は、その改善された臨床プロファイルと患者にとって実用的な投与方法により、クローン病治療薬市場で勢いを増しています。中等度から重度のクローン病治療薬として、既にヒュミラ(アダリムマブ)、レミケード(インフリキシマブ)、シンジア(セルトリズマブペゴル)といった抗TNF製剤、エンタイビオ(ベドリズマブ)やタイサブリ(ナタリズマブ)といった抗インテグリン製剤、そしてインターロイキン12/23阻害剤であるスキリージ(リサンキズマブ)などの複数の生物学的製剤が承認されています。
現在、クローン病治療薬市場では、ジョンソン・エンド・ジョンソン(J&J)、アッヴィ、武田薬品工業、UCB、バイオジェンという5つの主要企業が承認されたブランド薬を保有しており、これらの企業が市場の成長を牽引しています。さらに、S1P受容体モジュレーターの導入により、クローン病治療薬市場は近年大きく進化を遂げました。エンテローム・バイオ社のEB-8018やメソブラスト社のレモステムセル-Lなど、新規治療法が現在のクローン病の研究開発プログラムにおいて活発に研究されています。クローン病の研究開発戦略は、中等度から重度の病態に対するS1Pモジュレーターと他の治療薬を組み合わせた併用療法へと向かう傾向が強まっています。
**II. 市場成長の促進要因**
クローン病治療薬市場の成長は、いくつかの強力な要因によって促進されています。
1. **クローン病の有病率増加:** 世界的にクローン病の診断数が増加しており、これは治療を必要とする患者人口の拡大に直結しています。この有病率の増加は、製薬企業が新しい治療法の研究開発に投資し、革新的な製品を市場に投入する強力な動機となっています。多くの企業が規制当局や研究機関と協力して、最先端の治療法を開発・上市しようと努めています。
2. **革新的な治療法の開発と承認:** バイオテクノロジーと医薬品開発の進歩により、クローン病の病態生理学に基づいた標的治療薬が次々と開発されています。特に、抗TNF、抗インターロイキン、抗インテグリン抗体などの生物学的製剤は、ステロイドやアミノサリチル酸製剤に抵抗性を示す患者に対して満足のいく治療効果をもたらしています。また、S1P受容体モジュレーターやヤヌスキナーゼ(JAK)阻害剤などの新しい作用機序を持つ薬剤の登場も、市場の成長を大きく後押ししています。
3. **生物学的製剤の臨床プロファイルの改善と投与利便性:** 抗インテグリン阻害剤やインターロイキン阻害剤などの新しい生物学的製剤は、従来の治療薬と比較して、より改善された臨床プロファイルと患者にとって実用的な投与方法(例えば、自宅での自己注射など)を提供しています。これにより、患者の治療アドヒアランスが向上し、治療効果の最大化に貢献しています。
4. **主要製薬企業の市場牽引力:** ジョンソン・エンド・ジョンソン、アッヴィ、武田薬品工業、UCB、バイオジェンといった大手製薬企業が、承認済みのブランド薬を保有し、研究開発に多額の投資を行うことで、市場の成長を強力に牽引しています。これらの企業は、製品ポートフォリオの強化、新薬開発、市場拡大に向けた戦略的な取り組みを進めています。
5. **研究開発への投資増加:** 産業界および政府機関からの研究開発能力とインフラへの多額の投資が期待されており、これが市場に有利な機会を創出しています。多くの主要プレイヤーは、競合他社に対する優位性を確立するために、新製品の開発、研究開発への大規模な支出、主要な買収や提携に注力しています。
6. **戦略的成長イニシアチブ:** 主要企業は、製品ポートフォリオを強化するために、有機的および無機的な成長戦略の実施に注力しています。これには、合弁事業や買収、地理的拡大、研究開発への投資、新規薬剤の創出などが含まれ、グローバルなクローン病治療薬市場での競争力を高めています。
7. **医療費支出の増加と償還制度の整備:** 特に北米や欧州などの先進地域では、医療費支出が増加しており、クローン病治療薬に対する適切な償還制度が整っていることが市場の成長を支えています。これにより、高価な生物学的製剤へのアクセスが改善され、より多くの患者が治療を受けられるようになります。
8. **新薬承認とライセンス契約の推進:** 各国での新薬承認や企業間のライセンス契約は、市場の成長にポジティブな影響を与えます。例えば、日本市場では、ギリアド・ファーマが2023年にフィルゴチニブの発売を計画しており、このような動きが市場を活性化させます。
**III. 市場成長の抑制要因**
クローン病治療薬市場は成長を続ける一方で、いくつかの要因がその拡大を抑制する可能性があります。
1. **外科的治療に伴うリスク:** クローン病患者は結腸がんのリスクが高いことから、潰瘍性大腸炎と同様にがんリスク低減のために外科的治療が選択されることがあります。しかし、胃腸手術には感染、辺縁性潰瘍、吸収不良、狭窄などの合併症リスクが伴います。これらのリスクは、炎症性腸疾患(IBD)の治療における外科手術の広範な採用を妨げる可能性があります。
2. **既存治療薬への無反応患者の存在と免疫反応:** 抗腫瘍壊死因子(TNF)抗体などの生物学的製剤は、クローン病治療の主要な柱となってきましたが、一部の患者はこれらの治療に反応しなかったり、時間の経過とともに効果を失ったりすることがあります。特に抗TNF製剤では、高い割合の患者が治療に反応しないことが、新しい作用機序(MOA)の研究を促す要因となっています。また、生物学的製剤は免疫反応を引き起こす可能性があり、これが治療効果の減弱や副作用につながることもあります。
3. **臨床試験の中止と開発の挫折:** 新規クローン病治療薬の開発は、非常に複雑でコストがかかり、成功率が低いことが知られています。例えば、武田薬品工業は2021年にオンタマリマブ(第III相)のクローン病治療薬としての臨床試験を中止しました。これは、炎症性腸疾患(IBD)に対するSHP647(オンタマリマブ)の臨床開発プログラムへの資金提供を中止するというスポンサーの決定によるものです。同様に、ファイザー社も2021年にPF-06687234(第II相)の臨床試験を中止しました。これは、スポンサーが研究開発の優先順位と戦略を変更したことによるものです。このような臨床試験の中止は、市場への新薬導入を遅らせ、市場全体の成長を妨げる可能性があります。
4. **コルチコステロイドの限界と副作用:** コルチコステロイドは、クローン病の重症度にかかわらず、病気の寛解導入に効果的であるとされています。しかし、これらの薬剤は再燃を防ぐには至りません。さらに、長期使用に関連する副作用(骨粗鬆症、糖尿病、高血圧など)があるため、継続的な治療薬として使用することはできません。多くの国や地域でほとんどのコルチコステロイドの特許が既に期限切れとなっており、ジェネリック医薬品の普及が進むことで、ブランド薬の市場価値を低下させる可能性があります。
**IV. 市場機会**
クローン病治療薬市場は、いくつかの重要な機会を秘めており、将来の成長を促進する可能性を秘めています。
1. **新規治療薬クラスの開発:** 今後数年間で、多くの新しい治療薬クラスが市場に投入される予定です。これらの新薬は、既存の治療法では効果が得られなかった患者や、より優れた安全性プロファイルを持つ治療法を求める患者に新たな選択肢を提供します。特に、新しい作用機序(MOA)に基づいた薬剤の開発は、既存の治療薬への無反応問題に対処する上で重要です。
2. **新しい作用機序(MOA)への注目:** 既存の抗TNF療法に反応しない患者の割合が高いことから、製薬企業や研究機関は、炎症経路の異なる側面を標的とする新しい作用機序(MOA)の研究に注力しています。これにより、より個別化された治療アプローチや、難治性患者に対する効果的な治療法の開発が期待されます。
3. **中等度から重度の患者を対象とした新薬の導入:** 2023年から2025年にかけて、主に中等度から重度の患者集団を対象とした新薬の導入が市場の大幅な成長の主要な要因となると予想されています。これらの新薬は、既存の治療法では十分な効果が得られない患者や、より重篤な症状を持つ患者のアンメットニーズに応えるものです。
4. **ジェネリック医薬品の普及と市場参入:** ジェネリック医薬品の人気が高まることで、より多くのクローン病治療薬業界のプレイヤーがブランド薬のジェネリック版を導入することが予想されます。これは、治療コストの削減を通じて、より多くの患者が治療にアクセスできるようになり、市場全体の規模を拡大する機会となります。
5. **S1P受容体モジュレーターの進化:** S1P受容体モジュレーターの導入により、クローン病治療薬市場は近年大きく進化しました。これらの薬剤は、リンパ球の腸管への移動を阻害することで炎症を抑制し、新たな治療選択肢として注目されています。今後の研究開発により、その有効性と安全性がさらに確立されることが期待されます。
6. **研究開発パイプラインにおける革新的治療法:** エンタローム・バイオ社のEB-8018やメソブラスト社のレモステムセル-Lなど、革新的な治療法がクローン病の現在の研究開発プログラムで積極的に研究されています。これらの新規薬剤は、疾患の根本原因を標的とする可能性があり、将来的に治療パラダイムを大きく変える可能性があります。
7. **併用療法の進展:** クローン病の研究開発戦略は、中等度から重度の病態に対するS1Pモジュレーターと他の治療薬を組み合わせた併用療法へと向かう傾向が強まっています。併用療法は、単剤療法よりも高い治療効果や持続的な寛解を達成する可能性があり、患者の予後改善に貢献することが期待されます。
8. **政府および産業界からの研究開発支援:** 産業界および政府機関からの研究開発能力とインフラへの多額の投資が期待されており、これが市場に有利な機会を創出しています。このような支援は、新規薬剤の開発を加速させ、クローン病治療薬市場全体のイノベーションを促進します。
**V. セグメント分析**
**1. 地域別分析**
* **北米市場:** 世界市場において最も大きなシェアを占めており、予測期間中に10.50%のCAGRで成長すると予想されています。米国が最大の市場シェアを保持しています。この地域のクローン病治療薬市場の成長は、主要なプレイヤーの存在、疾患有病率の増加、および民間企業や政府機関による医療イニシアチブの増加に起因しています。高度な医療インフラと研究開発への投資も、市場拡大を後押ししています。
* **欧州市場:** 予測期間中に11.24%のCAGRで成長すると予想されています。英国は欧州のクローン病治療薬市場において最も重要な地域です。同国のクローン病市場は、クローン病患者の有病率、主要なプレイヤーの存在、確立された医療インフラによる医療アクセス向上により、実質的な成長が見込まれています。ベンダーによる新薬開発のための研究開発への注力も、市場に大きく影響すると予測されます。中程度の償還制度と医療費支出の増加も、同国の市場成長に影響を与える要因です。
* **アジア太平洋市場:** 予測期間中に著しい成長が期待されています。日本はアジア太平洋地域で最も急速に成長しているクローン病治療薬市場です。ヤヌスキナーゼ(JAK)阻害剤などの新興治療法が市場の成長を後押しすると予測されています。日本の市場成長は、クローン病患者の高い有病率、主要なプレイヤーの存在、確立された医療インフラによる医療アクセス向上に起因しています。複数のベンダーも、大きな成長機会があることから、日本でのクローン病新薬の発売を計画しています。例えば、ギリアド・ファーマは2023年にフィルゴチニブの日本での発売を計画しています。製品承認とライセンス契約は、日本の市場成長にポジティブな影響を与えるでしょう。
**2. 薬物クラス/治療法別分析**
* **抗TNF-α阻害剤:** 市場への最大の貢献者であり、予測期間中に10.29%のCAGRで成長すると予想されています。抗TNF-α療法は10年以上にわたりクローン病市場の主要な治療法として歴史的に位置づけられてきました。しかし、治療に反応しない患者の割合が高いことから、最近の進展では新しい作用機序(MOA)の研究が促されています。
* **その他の生物学的製剤(抗インテグリン、インターロイキン阻害剤など):** スキリージ(リサンキズマブ)のような最近承認された生物学的製剤は、予測期間中に世界のクローン病治療薬市場を支配すると予想されています。抗インテグリン阻害剤やインターロイキン阻害剤などの生物学的製剤は、その改善された臨床プロファイルと患者にとって実用的な投与方法により、クローン病治療薬市場で勢いを増しています。
* **新興治療法:** S1P受容体モジュレーターやヤヌスキナーゼ(JAK)阻害剤など、新たな治療薬クラスの登場が市場に新たな機会をもたらしています。これらの薬剤は、既存の治療法で効果が得られない患者や、より優れた安全性プロファイルを持つ治療法を求める患者に新たな選択肢を提供します。
**3. 性別セグメント**
* **女性セグメント:** 最も高い市場シェアを占めており、予測期間中に10.76%のCAGRで成長すると予想されています。クローン病の男女間のわずかな性差を考慮すると、女性は世界のクローン病治療薬市場においてかなりの部分を占めると予測されていました。クローン病は男性と同じ頻度で女性にも影響しますが、女性は必ずしも疾患に関連しているとは限らない他の症状を経験することもあります。女性は、生理痛や不規則な生理、性交痛など、特定のクローン病症状のみを経験する場合があります。
**4. 病型/罹患部位セグメント**
* **小腸・大腸型セグメント:** 市場への最大の貢献者であり、予測期間中に10.33%のCAGRで成長すると予想されています。クローン病は小腸と大腸の両方に影響を及ぼします。これは部分的に分かれて発生することもあれば、長い範囲にわたって発生することもあります。回腸と結腸がクローン病の炎症と損傷の典型的な部位です。
**5. 年齢セグメント**
* **49歳以下セグメント:** 最も高い市場シェアを占めており、予測期間中に10.27%のCAGRで成長すると予想されています。クローン病の発症はどの年齢でも起こり得ますが、最も頻繁に診断されるのは20歳から30歳までの成人および青少年です。症状が他の胃腸疾患と類似しているため、診断までに数年かかることもあります。この若年層での高い有病率と診断集中が、このセグメントの市場シェアを押し上げています。
Report Coverage & Structure
- セグメンテーション
- 調査方法論
- 無料サンプルを入手
- 目次
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制限と仮定
- 市場範囲とセグメンテーション
- 考慮された通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場トレンド
- 推進要因
- 市場の警告要因
- 最新のマクロ経済指標
- 地政学的な影響
- 技術的要因
- 市場評価
- ポーターのファイブフォース分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- ヨーロッパ
- APAC
- 中東およびアフリカ
- LATAM
- ESGトレンド
- 世界のクローン病治療薬市場規模分析
- 世界のクローン病治療薬市場概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- 世界のクローン病治療薬市場概要
- 北米市場分析
- 概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 米国
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- カナダ
- ヨーロッパ市場分析
- 概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 英国
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他のヨーロッパ地域
- APAC市場分析
- 概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 中国
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- 韓国
- 日本
- インド
- オーストラリア
- シンガポール
- 台湾
- 東南アジア
- その他のアジア太平洋地域
- 中東およびアフリカ市場分析
- 概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- アラブ首長国連邦
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他の中東およびアフリカ地域
- LATAM市場分析
- 概要
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- ブラジル
- 薬剤クラス別
- 概要
- 金額別薬剤クラス
- TNF-α阻害薬
- 金額別
- 5-アミノサリチル酸
- 金額別
- その他
- 金額別
- 性別タイプ別
- 概要
- 金額別性別タイプ
- 男性
- 金額別
- 女性
- 金額別
- 疾患タイプ別
- 概要
- 金額別疾患タイプ
- 小腸/大腸型
- 金額別
- 大腸型
- 金額別
- 小腸型
- 金額別
- 年齢層別
- 概要
- 金額別年齢層
- 49歳以下
- 金額別
- 50歳以上
- 金額別
- 薬剤クラス別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のLATAM地域
- 競合状況
- プレイヤー別クローン病治療薬市場シェア
- M&A契約と提携分析
- 市場プレイヤー評価
- アッヴィ株式会社
- 概要
- 事業情報
- 収益
- ASP
- SWOT分析
- 最近の動向
- バイオジェン
- 武田薬品工業
- ヤンセンバイオテック株式会社(ジョンソン・エンド・ジョンソン)
- ブリストル・マイヤーズ スクイブ
- アストラゼネカ
- ファイザー
- レッドヒルファーマ
- 4Dファーマ
- アッヴィ株式会社
- 調査方法論
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 主要な一次情報源
- 一次情報の内訳
- 二次および一次調査
- 主要な業界インサイト
- 市場規模の推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査の前提条件
- 前提条件
- 制限
- リスク評価
- 調査データ
- 付録
- ディスカッションガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
*** 本調査レポートに関するお問い合わせ ***

クローン病治療薬とは、消化管に慢性的な炎症を引き起こす難病であるクローン病の症状を管理し、寛解を誘導・維持し、合併症を予防するために用いられる薬剤の総称でございます。クローン病は、口から肛門までの消化管のあらゆる部位に炎症が生じる可能性があり、腹痛、下痢、血便、体重減少、発熱などの多様な症状を呈します。これらの治療薬は、病気の活動性を抑制し、患者様の生活の質を向上させることを目的としていますが、根本的な治癒をもたらすものではなく、長期的な病状コントロールが重要となります。
治療薬の種類は多岐にわたり、病状の重症度や活動性、患者様の状態に応じて使い分けられます。まず、軽症から中等症の患者様には、抗炎症作用を持つ5-アミノサリチル酸製剤(5-ASA製剤)が用いられることがございます。メサラジンなどが代表的で、消化管の炎症部位に直接作用し、症状の改善を促します。より強い炎症を抑える必要がある場合には、強力な抗炎症作用を持つステロイド製剤が使用されます。プレドニゾロンやブデソニドなどが挙げられ、急速な寛解導入に効果的ですが、長期使用による副作用のリスクがあるため、症状が改善したら速やかに減量・中止することが目指されます。
ステロイドからの離脱や寛解維持を目的として、免疫調節薬も重要な役割を果たします。これにはアザチオプリン、メルカプトプリン、メトトレキサートなどがあり、免疫系の過剰な反応を抑制することで炎症をコントロールします。効果の発現には時間を要しますが、ステロイドの使用量を減らし、長期的な寛解維持に貢献します。さらに、近年飛躍的な進歩を遂げているのが生物学的製剤でございます。これは特定の炎症性サイトカインや細胞接着分子を標的とする抗体医薬であり、従来の治療で効果不十分な中等症から重症のクローン病患者様に用いられます。代表的なものとして、炎症を引き起こす主要なサイトカインであるTNF-αを阻害するインフリキシマブ、アダリムマブ、セルトリズマブペゴル、ゴリムマブといった抗TNF-α抗体製剤があります。これらは炎症反応を強力に抑制し、粘膜治癒を促進します。また、IL-12とIL-23というサイトカインの働きを抑えるウステキヌマブや、消化管に炎症細胞が浸潤するのを防ぐ抗インテグリン抗体製剤であるベドリズマブも、新たな治療選択肢として活用されています。さらに、IL-23のみを特異的に阻害するリサンキズマブも登場し、治療の幅を広げています。
これらの生物学的製剤に加え、経口投与可能な低分子化合物であるJAK阻害薬もクローン病治療に導入されつつあります。ウパダシチニブなどが知られており、細胞内のシグナル伝達経路を阻害することで炎症を抑制します。その他、合併症である膿瘍や瘻孔に対しては抗菌薬が使用されたり、栄養状態の改善のために経腸栄養剤や経静脈栄養が行われたりすることもございます。これらの薬剤は、単独ではなく組み合わせて用いられることも多く、患者様一人ひとりの病態に合わせた個別化された治療計画が立てられます。
クローン病治療薬の進歩は、関連する診断技術やモニタリング技術の発展と密接に関わっております。内視鏡検査、カプセル内視鏡検査、MRIなどの画像診断技術は、病変の正確な評価と治療効果の判定に不可欠です。また、CRP、ESR、便中カルプロテクチンなどのバイオマーカーは、非侵襲的に病状の活動性を把握し、治療方針の決定に役立ちます。生物学的製剤の治療においては、薬物血中濃度モニタリング(TDM)が導入され、個々の患者様における薬剤の有効性や安全性を最適化するための重要な技術となっています。
将来的な関連技術としては、患者様の遺伝子情報や腸内細菌叢の解析に基づいた個別化医療のさらなる進展が期待されています。これにより、どの患者様にどの薬剤が最も効果的か、副作用のリスクはどうかといった予測が可能となり、より効果的で安全な治療の提供が目指されます。また、幹細胞治療などの再生医療は、難治性の瘻孔性クローン病に対する新たな治療法として研究が進められており、将来的な応用が期待される分野でございます。これらの薬剤と技術の進歩により、クローン病患者様の症状がより適切に管理され、生活の質の向上が図られています。