等温核酸増幅技術市場の規模とシェア分析 – 成長トレンドと予測(2025年~2030年)
等温核酸増幅技術(INAAT)市場レポートは、業界を技術別(ヘリカーゼ依存性増幅(HDA)など)、製品別(機器など)、用途別(感染症診断など)、エンドユーザー別(病院・検査機関など)、および地域別(北米、ヨーロッパ、アジア太平洋など)に分類しています。市場予測は、金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
等温核酸増幅技術(INAAT)市場は、2025年から2030年の予測期間において、堅調な成長が見込まれています。本レポートは、技術、製品、用途、エンドユーザー、地域といったセグメント別に市場を分析し、その成長トレンドと予測を提供しています。
市場の概要と成長要因
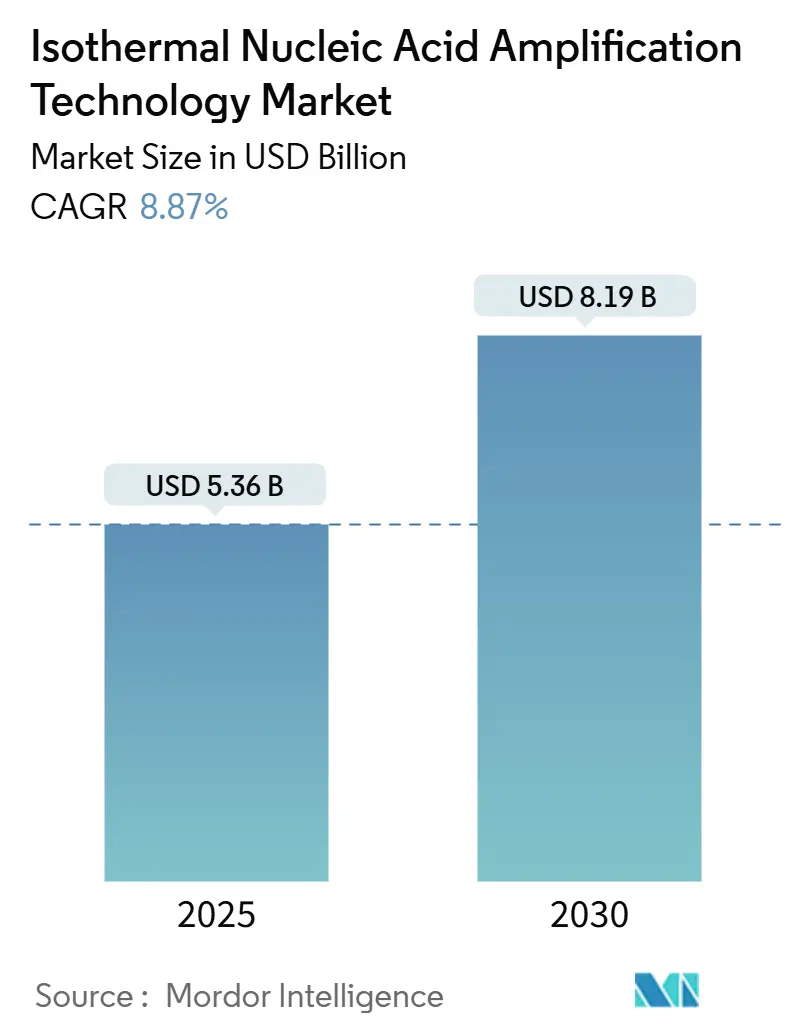
INAAT市場規模は、2025年には53.6億米ドルと推定され、2030年までに81.9億米ドルに達すると予測されており、予測期間中の年平均成長率(CAGR)は8.87%です。この成長は、主に一定温度での増幅が可能であるというINAATの特性によって推進されています。この特性により、かさばるサーマルサイクラーが不要となり、迅速なポイントオブケア(PoC)検査が実現します。病院では、緊急治療室でINAATプラットフォームを導入し、結果が出るまでの時間を数時間から数分に短縮しています。試薬サプライヤーは、安定した高利益率の消耗品販売から恩恵を受けています。製造業者は、マイクロ流体技術、凍結乾燥試薬、比色検出を統合することで、テストあたりのコストを削減し、非検査室環境での利用を拡大しています。アジア太平洋地域では、デバイス承認の合理化により市場投入までの期間が短縮され、INAATの採用が加速しています。一方、北米は、確立された償還制度により、収益面で市場をリードしています。欧州では、感染症の早期診断と治療の必要性が高まっていることから、INAAT技術の採用が拡大しています。特に、COVID-19パンデミックは、迅速かつ正確な診断ツールの重要性を浮き彫りにし、INAATのような分子診断技術への投資を加速させました。
市場の主要プレーヤーは、製品ポートフォリオの拡大、戦略的提携、研究開発への投資を通じて競争力を強化しています。例えば、新しいバイオマーカーの発見や、より使いやすいデバイスの開発が進められています。これにより、INAATは、病院や診療所だけでなく、薬局や家庭での使用にも適した、よりアクセスしやすい診断ソリューションへと進化していくと期待されています。
課題としては、INAAT技術の初期導入コスト、特定のアプリケーションにおける感度と特異性の最適化、そして規制当局の承認プロセスが挙げられます。しかし、これらの課題は、技術革新と市場の成熟とともに克服されていくでしょう。INAAT市場は、今後も診断医療分野において重要な役割を果たし、患者ケアの向上に貢献していくと見込まれています。
このレポートは、等温核酸増幅技術(Isothermal Nucleic Acid Amplification Technology, INAAT)市場に関する詳細な分析を提供しています。
1. 市場の定義と調査範囲
INAAT市場は、臨床、獣医、食品安全、研究診断において、一定温度でDNAまたはRNAを増幅する商用機器、試薬、および統合テストキットを対象としています。Mordor Intelligenceによる評価は、17の主要国における病院、リファレンスラボ、ポイントオブケア(PoC)施設、学術機関での初回販売ハードウェアおよび消耗品から生じる収益をカバーしています。PCRサーマルサイクラーや受託試験の収益は対象外です。
2. 調査方法
本調査は、一次調査とデスク調査を組み合わせて実施されました。一次調査では、グローバルなアッセイサプライヤーのプロダクトマネージャー、病院チェーンの調達責任者、臨床病理学教授へのインタビューを通じて、LAMP、NEAR、RPAなどの手法の普及率、試薬の割引パターン、および予備的な量に関する仮定が検証されました。デスク調査では、PubMed、CDC、WHO、ECDC、中国NHCなどの査読済み論文や感染症データベース、貿易統計、特許出願、輸入関税、企業の財務情報など、数百の公開情報源が活用されました。
市場規模の算出と予測は、感染症検査量と献血スクリーニング手順をINAATの普及率と加重平均試薬ASPで乗じるトップダウンアプローチと、サプライヤーの集計や機器の設置状況から確認するボトムアップアプローチを併用しています。結核発生率、C型肝炎スクリーニング義務、PoCデバイスの承認、試薬ASPの低下、年間医療費の伸びなどが主要なモデル入力として使用され、多変量回帰とシナリオ分析を組み合わせた5年間の予測が行われています。
Mordor IntelligenceのINAAT市場ベースラインは、明確に開示された診断手順数と検証済みの試薬価格に基づいているため、他の調査と比較して信頼性が高いとされています。競合他社の調査では、PCR消耗品をINAATに含めたり、割引を考慮しない定価を使用したり、確認されていないPoC展開を過度に予測したりする傾向があるため、推定値に乖離が生じることが指摘されています。
3. エグゼクティブサマリー(主要な調査結果)
* 市場成長の推進要因: ポイントオブケア診断の急速な普及、機器コストの低減、北米およびアジア太平洋地域における継続的な規制支援が市場を牽引しており、2030年までの年平均成長率(CAGR)は8.87%と予測されています。
* 主要な技術セグメント: ループ媒介等温増幅(LAMP)が収益の44.34%を占め、CAGR 13.36%で最も急速に成長しているセグメントです。
* 最も急速に拡大する地域: アジア太平洋地域は、承認プロセスの合理化とインフラ投資により、CAGR 15.64%で成長すると予測されています。
* 将来最も高い成長が期待されるアプリケーション: 腫瘍学およびリキッドバイオプシー検査は、非侵襲的がんスクリーニングの医療および支払い者による受け入れが進むにつれて、CAGR 16.11%で拡大すると見込まれています。
* INAAT普及の主な障壁: 既存のPCRインフラ、償還ギャップ、酵素供給の不安定性が、今後2〜4年間の普及に影響を与える主要な制約となっています。
4. 市場の動向
4.1 市場の推進要因:
* ポイントオブケア感染症診断の採用拡大
* 高齢化人口と慢性疾患の負担増加
* PCRからINAATへのワークフローの移行
* テストあたりのコスト経済性の低減
* マイクロ流体バッテリー駆動カートリッジ(UTR)の進化
* CRISPR強化アッセイの特異性向上(UTR)
4.2 市場の抑制要因:
* PCRおよびDCRプラットフォームとの競合
* 認知度と償還のギャップ
* Bst試薬用酵素供給の不安定性
* CLIA-Waiver / IVDRの厳格なエビデンス要件(UTR)
4.3 ポーターのファイブフォース分析:
新規参入の脅威、買い手の交渉力、サプライヤーの交渉力、代替品の脅威、競争上のライバル関係の観点から市場が分析されています。
5. 市場規模と成長予測(USD価値)
市場は以下のセグメントで分析・予測されています。
* 技術別: ヘリカーゼ依存増幅(HDA)、ニッキング酵素増幅反応(NEAR)、ループ媒介等温増幅(LAMP)、鎖置換増幅(SDA)、核酸配列ベース増幅(NASBA)、転写媒介増幅(TMA)、シングルプライマー等温増幅(SPIA)、その他の技術。
* 製品別: 機器、試薬および消耗品。
* アプリケーション別: 感染症診断、腫瘍学およびリキッドバイオプシー、血液スクリーニングおよび輸血安全性、食品・水安全性検査、獣医および農業診断。
* エンドユーザー別: 病院およびリファレンスラボ、ポイントオブケア/分散型クリニック、学術・研究機関。
* 地域別: 北米、欧州、アジア太平洋、中東・アフリカ、南米の主要国および地域。
6. 競争環境
市場集中度、市場シェア分析、および主要企業のプロファイルが含まれています。プロファイル対象企業には、Abbott Laboratories、BioMérieux SA、Eiken Chemical Co., Ltd.、Hologic Inc.、Qiagen N.V.、Roche Diagnostics、Thermo Fisher Scientificなどが挙げられます。
7. 市場機会と将来展望
ホワイトスペースと満たされていないニーズの評価を通じて、市場の機会が特定されています。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
-
4.2 市場の推進要因
- 4.2.1 臨床現場即時検査(POCT)における感染症診断の採用
- 4.2.2 高齢化と慢性疾患の負担
- 4.2.3 ワークフローのPCRからINAATへの移行
- 4.2.4 検査あたりのコスト経済性の低下
- 4.2.5 マイクロ流体バッテリー駆動カートリッジ (UTR)
- 4.2.6 CRISPR強化アッセイ特異性 (UTR)
-
4.3 市場の阻害要因
- 4.3.1 PCRおよびDCRプラットフォームとの競合
- 4.3.2 認知度と償還のギャップ
- 4.3.3 Bst試薬の酵素供給の変動性
- 4.3.4 厳格なCLIA免除/IVDRエビデンスのハードル (UTR)
-
4.4 ポーターの5つの力分析
- 4.4.1 新規参入者の脅威
- 4.4.2 買い手の交渉力
- 4.4.3 供給者の交渉力
- 4.4.4 代替品の脅威
- 4.4.5 競争上の対抗関係
5. 市場規模と成長予測 (USD建て)
-
5.1 テクノロジー別
- 5.1.1 ヘリカーゼ依存性増幅 (HDA)
- 5.1.2 ニッキング酵素増幅反応 (NEAR)
- 5.1.3 ループ媒介等温増幅 (LAMP)
- 5.1.4 鎖置換増幅 (SDA)
- 5.1.5 核酸配列ベース増幅 (NASBA)
- 5.1.6 転写媒介増幅 (TMA)
- 5.1.7 シングルプライマー等温増幅 (SPIA)
- 5.1.8 その他のテクノロジー
-
5.2 製品別
- 5.2.1 機器
- 5.2.2 試薬 & 消耗品
-
5.3 用途別
- 5.3.1 感染症診断
- 5.3.2 腫瘍学およびリキッドバイオプシー
- 5.3.3 血液スクリーニングおよび輸血安全性
- 5.3.4 食品・水質安全性検査
- 5.3.5 獣医および農業診断
-
5.4 エンドユーザー別
- 5.4.1 病院 & リファレンスラボ
- 5.4.2 ポイントオブケア / 分散型クリニック
- 5.4.3 学術 & 研究機関
-
5.5 地域別
- 5.5.1 北米
- 5.5.1.1 米国
- 5.5.1.2 カナダ
- 5.5.1.3 メキシコ
- 5.5.2 欧州
- 5.5.2.1 ドイツ
- 5.5.2.2 英国
- 5.5.2.3 フランス
- 5.5.2.4 イタリア
- 5.5.2.5 スペイン
- 5.5.2.6 その他の欧州
- 5.5.3 アジア太平洋
- 5.5.3.1 中国
- 5.5.3.2 日本
- 5.5.3.3 インド
- 5.5.3.4 オーストラリア
- 5.5.3.5 韓国
- 5.5.3.6 その他のアジア太平洋
- 5.5.4 中東 & アフリカ
- 5.5.4.1 GCC
- 5.5.4.2 南アフリカ
- 5.5.4.3 その他の中東 & アフリカ
- 5.5.5 南米
- 5.5.5.1 ブラジル
- 5.5.5.2 アルゼンチン
- 5.5.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
-
6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要セグメント、利用可能な財務情報、戦略情報、主要企業の市場ランク/シェア、製品&サービス、および最近の動向を含む)
- 6.3.1 アボット・ラボラトリーズ
- 6.3.2 アンプリフィカ・ラボ
- 6.3.3 ベクトン・ディッキンソン&カンパニー
- 6.3.4 バイオメリューSA
- 6.3.5 ディアソリンSpA
- 6.3.6 栄研化学株式会社
- 6.3.7 ゲノメラ・インク
- 6.3.8 ホロジック・インク
- 6.3.9 ルシジェン(LGCバイオサーチ)
- 6.3.10 メリディアン・バイオサイエンス
- 6.3.11 モルバイオ・ダイアグノスティクス
- 6.3.12 ニューイングランド・バイオラボ
- 6.3.13 オプティジーン・リミテッド
- 6.3.14 キアゲンN.V.
- 6.3.15 クイデルオーソ・コーポレーション
- 6.3.16 ロシュ・ダイアグノスティックス
- 6.3.17 テカン・ゲノミクス・インク
- 6.3.18 サーモフィッシャーサイエンティフィック
- 6.3.19 ツイストDxリミテッド
- 6.3.20 ユースター・バイオテクノロジーズ
7. 市場機会&将来展望
*** 本調査レポートに関するお問い合わせ ***

等温核酸増幅技術は、特定の核酸(DNAまたはRNA)を一定の温度条件下で増幅させる一連の技術を指します。従来のポリメラーゼ連鎖反応(PCR)が、DNAの変性、アニーリング、伸長という3つのステップを繰り返すために温度サイクルを必要とするのに対し、等温核酸増幅技術は、その名の通り、単一の温度で反応が進行するため、専用の温度制御装置が不要であるか、より簡便な装置で実施できるという大きな利点があります。この特性により、迅速性、簡便性、携帯性に優れ、特に現場での検査(Point-of-Care Testing: POCT)への応用が期待されています。
この技術の定義をさらに深掘りしますと、核酸増幅のメカニズムはPCRとは異なります。PCRが熱変性によって二本鎖DNAを一本鎖に分離するのに対し、等温増幅技術の多くは、酵素(ヘリカーゼやリコンビナーゼなど)の働きやプライマーの設計を工夫することで、熱変性なしにDNA鎖を分離し、増幅反応を進めます。これにより、反応時間の短縮や装置の小型化・低コスト化が可能となり、医療診断、食品検査、環境モニタリングなど、多岐にわたる分野での実用化が進んでいます。
等温核酸増幅技術には、いくつかの主要な種類が存在します。
最も広く知られているのが、LAMP法(Loop-mediated Isothermal Amplification)です。これは、4~6種類のプライマーと鎖置換活性を持つDNAポリメラーゼを用いることで、標的核酸を効率的に増幅します。反応は60~65℃程度の一定温度で進行し、非常に高い特異性と感度を持ち、短時間で大量の増幅産物を生成します。増幅産物は濁度や蛍光、あるいは金属指示薬による呈色反応などで簡便に検出できるため、POCTに適しています。
次に、RPA法(Recombinase Polymerase Amplification)があります。これは、リコンビナーゼ酵素がプライマーを標的DNAに結合させ、その後、鎖置換活性を持つDNAポリメラーゼが伸長反応を行うことで増幅します。反応温度は25~42℃と比較的低温で、LAMP法よりもさらに迅速に増幅が完了するという特徴があります。
HDA法(Helicase-Dependent Amplification)は、DNAヘリカーゼ酵素が二本鎖DNAを一本鎖に分離する働きを利用して増幅を行います。PCRの熱変性の代わりにヘリカーゼを用いることで、一定温度での増幅を可能にしています。
SDA法(Strand Displacement Amplification)は、制限酵素と鎖置換活性を持つDNAポリメラーゼを組み合わせて増幅を行います。制限酵素が特定の部位を切断し、その後にポリメラーゼが新しい鎖を合成しながら既存の鎖を押し出すことで、連鎖的に増幅が進みます。
NASBA法(Nucleic Acid Sequence-Based Amplification)は、RNAを標的とした増幅技術で、逆転写酵素、RNase H、RNAポリメラーゼの3種類の酵素を組み合わせて、RNAからRNAを増幅します。これは、特にウイルスRNAの検出に有用です。
その他にも、CPA法(Cross Priming Amplification)やSmartAmp法など、様々な等温核酸増幅技術が開発されており、それぞれ異なるメカニズムと特性を持っています。
これらの技術は、多岐にわたる分野で活用されています。
最も主要な用途は、感染症診断です。新型コロナウイルス感染症(COVID-19)のパンデミック時には、LAMP法をはじめとする等温核酸増幅技術が、迅速かつ簡便な検査法として注目され、PCR検査の代替や補完として広く利用されました。インフルエンザウイルス、デングウイルス、結核菌、MRSAなどの細菌、マラリア原虫などの寄生虫の検出にも応用されています。特に、医療資源が限られた地域や、緊急性の高い状況でのPOCTとして非常に有効です。
食品安全検査においても重要な役割を果たしています。サルモネラ菌、O157大腸菌、リステリア菌などの食中毒菌の迅速な検出や、アレルゲン、遺伝子組み換え作物(GMO)のスクリーニングにも利用されています。これにより、食品の品質管理や安全性の確保に貢献しています。
環境モニタリングでは、水質や土壌中の病原体、汚染物質の検出に用いられます。例えば、レジオネラ菌やノロウイルスなどの水系感染症の原因となる微生物の監視に役立っています。
農業・畜産分野では、植物の病害診断や家畜の感染症診断に利用され、農作物の品質向上や畜産物の安全確保に貢献しています。
研究分野においても、遺伝子発現解析や遺伝子型判定など、様々な基礎研究に応用されています。
さらに、バイオテロ対策として、生物兵器の迅速な検出システムへの組み込みも検討されています。
等温核酸増幅技術は、他の関連技術と組み合わせることで、その性能をさらに高めています。
マイクロ流体デバイス(Lab-on-a-chip)との統合は、増幅反応から検出までの一連のプロセスを小型チップ上で完結させることを可能にし、真のPOCTデバイスの実現に貢献しています。
増幅産物の検出には、バイオセンサーが利用されます。蛍光色素やプローブを用いたリアルタイム検出、濁度変化による肉眼での判定、金コロイドなどの金属指示薬を用いた呈色反応、電気化学的手法など、様々な検出方法が開発されています。
近年注目されているのが、CRISPR-Casシステムとの組み合わせです。等温核酸増幅によって増幅された標的核酸を、CRISPR-Casシステムが特異的に認識・切断することで、超高感度かつ高特異的な検出が可能になります(例:SHERLOCK、DETECTR)。これにより、単一分子レベルでの検出も視野に入ってきています。
また、増幅産物をラテラルフローイムノアッセイ(LFA)のような簡易なストリップテストで検出するシステムも開発されており、視覚的に結果を判定できるため、専門知識が不要で、より広範な利用が期待されています。
市場背景としては、等温核酸増幅技術の市場は急速に拡大しています。この成長の主な推進要因は、迅速で携帯可能な診断ソリューションへの需要の高まりです。特に、COVID-19パンデミックは、分散型検査の重要性を浮き彫りにし、等温核酸増幅技術の認知度と採用を大幅に加速させました。新興感染症の頻発、慢性疾患の増加、食品安全への意識向上なども市場を牽引しています。
しかし、課題も存在します。一部の等温増幅法は、PCRと比較して多重検出(複数の標的を同時に検出する能力)が難しい場合があります。また、感度や特異性においてPCRに劣るケースや、偽陽性・偽陰性のリスクを低減するためのさらなる技術改良が求められています。規制当局の承認プロセスや、標準化の確立も市場拡大における重要な要素です。それでも、POCT市場における等温核酸増幅技術の存在感は増しており、多くの企業がこの分野に投資し、新しい製品やソリューションを開発しています。
将来展望として、等温核酸増幅技術はさらなる進化を遂げると予想されます。
まず、統合化と自動化が進むでしょう。マイクロ流体デバイス、AI、ロボティクスとの融合により、サンプル前処理から結果判定までを完全に自動化するシステムが開発され、より簡便で信頼性の高い検査が実現されると考えられます。
多重検出能力の向上も重要な課題です。複数の病原体や遺伝子変異を同時に検出できる技術の開発が進むことで、より包括的な診断が可能になります。
感度と特異性のさらなる向上は、常に追求されるテーマです。CRISPR-Casシステムとの組み合わせのように、他の先進技術との融合により、PCRに匹敵するか、それを超える性能を持つシステムが登場する可能性があります。
新たな応用分野の開拓も期待されます。個別化医療におけるコンパニオン診断、遺伝子治療のモニタリング、環境中の微量なDNA/RNAの検出など、これまで困難であった分野での活用が進むでしょう。
また、コストのさらなる低減も重要な要素です。特に開発途上国での利用を促進するためには、より安価で堅牢なデバイスと試薬の開発が不可欠です。
等温核酸増幅技術は、その本質的な利点である「簡便性」と「迅速性」を最大限に活かし、医療、公衆衛生、産業、環境など、社会の様々な側面において、より安全で健康的な未来を築くための基盤技術として、その重要性を増していくことでしょう。