HIV治験市場規模と展望、2026年~2034年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
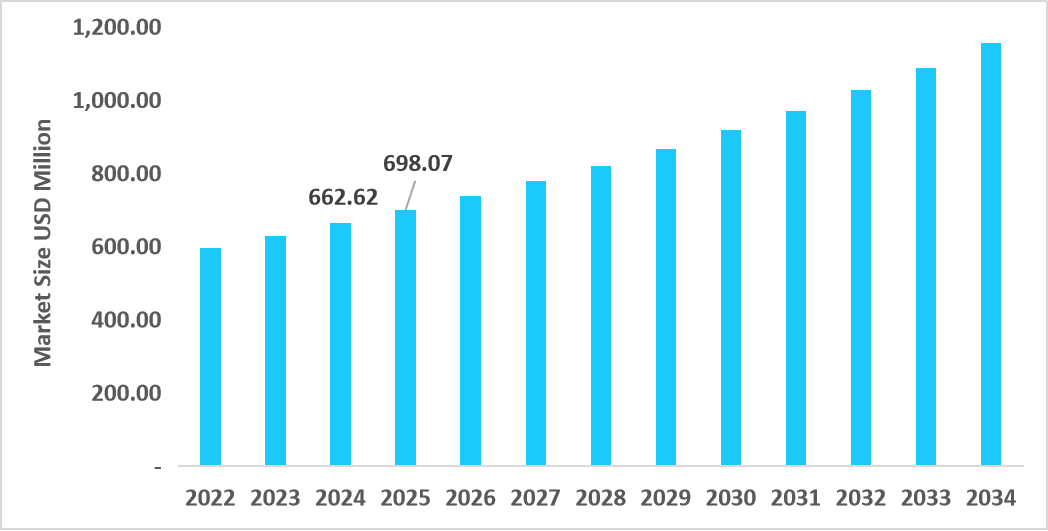
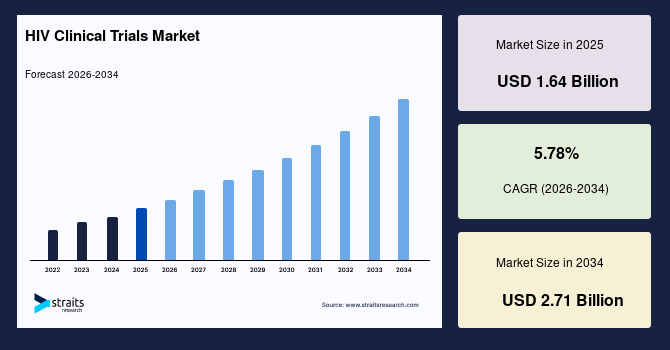
HIV治験の世界市場は、2025年には16.4億米ドルと推計されており、2034年までに27.1億米ドルに達すると予測され、予測期間中の年平均成長率(CAGR)は5.78%で推移する見込みです。この市場の著しい成長は、主にAI駆動型患者マッチングシステムの導入に起因しており、これによりHIV治験における被験者募集の効率が向上し、結果が最適化されています。
**市場概要と主要トレンド**
HIV治験市場は、治験の段階、研究デザイン、およびスポンサーの種類によって多角的に構成されています。治験の段階別では、第I相、第II相、第III相、第IV相治験が含まれ、それぞれが治験薬の安全性、有効性、および長期的なアウトカムの評価に焦点を当てています。具体的には、第I相治験は少数の健康な被験者に対して薬の安全性と薬物動態を評価し、第II相治験は少数の患者に対して有効性と最適な投与量を探索します。第III相治験は大規模な患者集団で有効性と安全性を確認し、第IV相治験は上市後の長期的な安全性と有効性を監視します。研究デザイン別では、介入研究、観察研究、および拡大アクセス研究があり、これらは多様な研究手法を反映しています。介入研究は特定の治療法や介入の効果を評価するもので、観察研究は患者集団のデータを収集・分析し、拡大アクセス研究は治療選択肢が限られた患者に治験薬への早期アクセスを提供するものです。また、市場には製薬企業、バイオ医薬品企業、非営利団体、その他の研究機関など、様々なスポンサーが関与しています。
現在のHIV治験市場における重要なトレンドの一つは、小児集団への重点の増加です。例えば、ViiV Healthcare社は、HIV感染小児における最適化された抗レトロウイルス療法レジメンを評価するためのODYSSEY治験を開始しました。小児研究に焦点を当てることは、満たされていない治療ニーズに対応し、年齢に適した製剤を確保し、世界中のより若い患者のための安全で効果的な治療法を支援することで、市場を拡大します。
さらに、Merck & Co. Inc.やJanssen Pharmaceuticalsなどの主要なHIV治験スポンサーは、患者募集と維持を改善するために、分散型および仮想治験モデルを採用しています。これらの治験では、遠隔医療、遠隔モニタリング、およびデジタルデータ収集を活用することで、地理的な障壁を低減し、参加者のエンゲージメントを高めています。このトレンドは、治験の迅速な実施とより広範な人口へのアクセスを可能にし、企業が世界市場における競争力を強化する上で有利な立場をもたらします。
**市場成長の推進要因**
HIV治験市場の成長を推進する主要な要因は、抗レトロウイルス療法(ART)の開発における著しい進展です。HIV感染症の有病率の増加と、患者のアドヒアランス(治療への順守)を向上させる必要性が、長期作用型注射剤療法の開発を加速させています。従来の経口ARTは毎日の服用が必要であり、患者にとって負担となる場合がありましたが、長期作用型注射剤は投与頻度を大幅に減らすことで、アドヒアランスの改善に寄与すると期待されています。例えば、2024年にはViiV Healthcare社がカボテグラビルを基盤としたレジメンを複数のグローバル第III相治験で推進し、Gilead Sciences社は新しい治験薬により長期作用型ポートフォリオを拡大しました。これらの進展は、企業が投与頻度を減らし、満たされていない臨床ニーズ(例えば、服薬コンプライアンスが困難な患者層)に対応するために、これらの治療法を優先していることを示しており、結果としてHIV治験市場の成長を強力に牽引しています。
**市場成長の阻害要因**
一方で、長期にわたる多段階のHIV治験において被験者を募集することは、地理的障壁や厳格な適格基準のために依然として大きな課題となっています。HIV感染症は社会的なスティグマを伴うことが多く、これが患者の治験参加への抵抗感につながることもあります。また、特定の遺伝的背景や併存疾患を持つ患者、あるいは特定の治療歴を持つ患者など、治験の対象となる集団が非常に限定される場合もあります。高い脱落率や多様な集団(例えば、異なる人種、民族、社会経済的背景を持つ人々)を登録することの難しさは、治験の進行を遅らせ、コストを増加させ、スポンサーが堅牢で一般化可能なデータを生成する能力を制限します。最近実施されたCHOICES研究では、HIV陽性者におけるオピオイド使用障害に対する徐放性ナルトレキソン(XR-NTX)の評価を目的としていましたが、HIVと薬物使用に関連するスティグマを含む様々な障壁に直面しました。このように、限られた患者募集と高い脱落率は、市場の成長と新しいHIV治療法のタイムリーな開発に対する重要な阻害要因となっています。
**市場機会**
市場の成長にとって大きな機会となるのは、HIVの機能的治癒を目指す治療用ワクチンの開発です。現在の抗レトロウイルス療法はHIVを効果的に抑制し、患者の生活の質を大幅に向上させましたが、ウイルスを完全に根絶することはできず、生涯にわたる治療が必要です。治療を中断するとウイルスが再活性化するため、患者は長期間にわたる薬物療法を継続しなければなりません。このため、ウイルスの潜在的なリザーバー(休眠状態のウイルスが潜む細胞)を標的とするワクチンに焦点を当てる企業は、この重要な満たされていないニーズに対応しています。機能的治癒を実現するワクチンが開発されれば、患者は生涯にわたるARTから解放され、医療システムにとっても大きなメリットとなります。したがって、機能的治癒戦略への投資は、製造業者が新しい候補薬を開発し、これらのワクチン候補の臨床試験を実施することを可能にし、市場に新たな成長の道を開くでしょう。
**セグメント分析**
**治験段階別**
治験段階別に見ると、第II相治験セグメントが2025年に31.67%の収益シェアを占め、市場を支配しました。この優位性は、適応的治験デザインへの注力によって推進されており、研究者は中間結果に基づいて投与量、コホートサイズ、または治療群を変更することができます。この柔軟性により、有効性の評価が加速され、リソースの無駄が削減され、より大規模で費用のかかる第III相治験に進む前に有望な治療法を正確に特定することが可能になります。
一方、第I相治験セグメントは、予測期間中に6.03%という最速のCAGR成長を記録すると予測されています。これは、ヒト化in vitroモデルとオルガンオンチップ技術の利用が増加していることに起因します。これらの革新技術は、より生理学的に関連性の高い設定で安全性と薬物動態を早期に評価することを可能にし、候補薬の選択を加速させます。これにより、動物実験の必要性を減らし、ヒトでの治験の成功確率を高めることが期待されています。
**研究デザイン別**
研究デザイン別では、介入研究セグメントが2025年に65.72%の収益シェアを占め、市場を支配しました。この優位性は、適応プラットフォーム治験デザインの採用が増加していることに起因します。これらの研究は、単一のプロトコル内で複数のHIV治療法を同時に評価することを可能にし、迅速な比較、効率的なリソース利用、および中間結果に基づく治療群の動的な変更を検証することで、効果的な介入法の特定を加速させます。
拡大アクセス研究セグメントは、予測期間中に6.49%という最速のCAGRで成長すると推定されています。この成長は、治療選択肢が限られている患者が、治験段階の有望なHIV治療法に早期にアクセスできるコンパッショネートユースプログラムの増加によって支えられています。これらのプログラムは、患者の未充足ニーズに対応するだけでなく、より広範な臨床開発と市場承認のための規制支援を強化する役割も果たしています。
**スポンサー別**
スポンサー別では、製薬・バイオ医薬品企業セグメントが2025年に市場を支配しました。この成長は、HIV治療法のためのAI支援型ドラッグリパーパシングへの戦略的投資によって促進されています。AIを活用した計算モデルは、既存の化合物の中から潜在的な抗HIV活性を持つものを効率的に特定することを可能にし、これによりリード開発を加速させ、研究開発コストを削減し、臨床的成功の可能性を高めています。
非営利団体セグメントは、予測期間中に6.18%のCAGRを記録すると予想されています。これは、分散型コミュニティ主導のHIV治験における役割が増大していることに起因します。地域の診療所やアウトリーチネットワークを活用することで、非営利団体はアクセスが困難な集団(例:地理的に孤立した地域や社会的に疎外されたコミュニティ)に対する治験のアクセシビリティを向上させ、参加者の多様性を高め、有効性データを生成することで、HIV研究を支援しています。
**地域分析**
**北米**
北米は2025年に世界市場で45.84%の市場シェアを占め、その優位性を確立しました。この優位性は、大規模な研究イニシアチブを支える強力な政府および機関からの資金援助によって加速されています。国立衛生研究所(NIH)や国立アレルギー・感染症研究所(NIAID)などの機関は、ワクチンおよび治癒に焦点を当てたプログラムに継続的に投資しています。この堅固な資金提供エコシステムは、イノベーションを加速させ、HIV研究および治療開発における北米のグローバルリーダーとしての地位を強化しています。特に米国のHIV治験市場の成長は、NIH、学術機関、主要製薬企業間の強固な官民研究連携によって加速されています。これらのパートナーシップは、基礎研究から臨床応用への橋渡し研究(トランスレーショナル研究)を促進し、広範な患者募集を可能にし、遺伝子編集や治療用ワクチンなどの革新的な治療法におけるイノベーションを育んでいます。
**アジア太平洋**
アジア太平洋地域は、2026年から2034年にかけて7.06%のCAGRで成長し、HIV治験市場において最も急速に成長している地域として台頭しています。これは、インドとタイの都市部および半都市部における分散型およびコミュニティベースの治験への参加が増加していることに起因しています。このアプローチは、患者のアクセシビリティを向上させ、維持率を高め、リアルなデータ収集を可能にすることで、革新的なHIV治療法の迅速な評価を支援し、この地域が臨床研究の主要ハブとして浮上するのを後押しします。オーストラリアの市場成長は、アボリジナルおよびトレス海峡諸島民の健康プログラムを研究イニシアチブに強力に統合していることによって支えられています。この包摂性により、文化的に配慮した治験デザインが確保され、サービスが行き届いていない集団からの参加が改善され、地域間の健康格差に対処し、包括的な臨床研究実践を推進する上で貴重な疫学的洞察が生成されています。
**欧州**
欧州のHIV治験市場の成長は、EAVI2020やEuroCoordイニシアチブのような汎欧州研究コンソーシアムおよび地域間臨床ネットワークの拡大によって推進されています。これらのイニシアチブは、多国間治験の実施を合理化し、データ調和を強化し、EU加盟国間の規制整合性を強めることで、新規治療法の開発を加速させ、患者の多様性を改善し、欧州のHIV研究エコシステム全体での科学的交流を促進しています。英国市場は、Genomics EnglandやUK Biobankによって支援されるような先進的なゲノム研究ハブの設立により成長を遂げています。これらの研究ハブは、精密な患者層別化とバイオマーカーの特定を可能にし、個別化されたHIV治療アプローチにおけるイノベーションを促進し、国内全体で標的治療候補の迅速な開発を支援しています。
**ラテンアメリカ**
ラテンアメリカのHIV治験市場の成長は、ブラジルとアルゼンチンにおける地域的なファーマコゲノミクス研究プロジェクトの設立によって増強されています。これは、HIV患者間の遺伝的多様性に焦点を当てたものです。これらのプログラムは、薬物応答の変動に関する理解を深め、集団固有の治療法開発を支援し、臨床研究におけるリード開発を増加させます。アルゼンチン市場の成長は、中央集権型電子健康記録(EHR)ネットワークによって強化されており、研究者は患者の履歴を効率的に追跡し、治療アドヒアランスを監視し、臨床研究に適格な参加者を効率的に特定することができます。この高度なデジタルシステムは治験募集を加速させ、それが市場成長を支援しています。
**中東・アフリカ**
中東およびアフリカのHIV治験市場は、特に南アフリカとケニアにおける地域的なバイオバンキングおよびサンプル共有ネットワークの存在により拡大しています。これらのイニシアチブは、多様な遺伝子およびウイルスサンプルへのアクセスを促進し、国境を越えた共同研究を支援し、地域住民に合わせた診断および治療ツールの開発を加速させています。サウジアラビアにおける世界市場の成長は、King Fahd Medical Research Centerのような専門的な感染症研究センターへの同国の投資によって支えられています。これらのセンターは、高度な実験施設を提供し、国際的なHIV研究ネットワークとの協力を促進しています。
**競争環境**
世界のHIV治験市場は、主要な製薬企業、バイオテクノロジー企業、および研究機関がイノベーションを推進する、中程度に統合された市場です。主要プレイヤーには、Gilead Sciences社、ViiV Healthcare社、Merck & Co.社などが含まれ、これらの企業は広範なR&Dパイプラインとグローバルな治験ネットワークを通じて市場を支配しています。これらの企業は、戦略的提携に焦点を当て、ワクチン研究を加速させ、アクセスプログラムを拡大することで、世界的なプレゼンスと治療ポートフォリオを強化し、競争力を維持しています。HOOKIPA Pharma Inc.は、HIV治療用ワクチン開発を積極的に推進している革新的なバイオテクノロジー企業です。同社は、Gilead Sciences社との協力により、その新規ワクチン候補HB-500を通じて評価を高めています。
Report Coverage & Structure
“`html
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制約事項と仮定
- 市場範囲とセグメンテーション
- 考慮される通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場トレンド
- 推進要因
- 市場警戒要因
- 最新のマクロ経済指標
- 地政学的影響
- 技術要因
- 市場評価
- ポーターの5フォース分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- 欧州
- アジア太平洋
- 中東・アフリカ
- 中南米
- ESGトレンド
- 世界のHIV治験市場規模分析
- 世界のHIV治験市場概要
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- 北米市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- 米国
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- カナダ
- 欧州市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- 英国
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他の欧州
- アジア太平洋市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- 中国
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- 韓国
- 日本
- インド
- オーストラリア
- 台湾
- 東南アジア
- その他のアジア太平洋
- 中東・アフリカ市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- アラブ首長国連邦
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他の中東・アフリカ
- 中南米市場分析
- はじめに
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- ブラジル
- フェーズ別
- はじめに
- フェーズ別金額
- フェーズI
- 金額別
- フェーズII
- 金額別
- フェーズIII
- 金額別
- フェーズIV
- 金額別
- 研究デザイン別
- はじめに
- 研究デザイン別金額
- 介入研究
- 金額別
- 観察研究
- 金額別
- 拡大アクセス研究
- 金額別
- 治験依頼者別
- はじめに
- 治験依頼者別金額
- 製薬・バイオ医薬品企業
- 金額別
- 非営利団体
- 金額別
- その他
- 金額別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他の中南米
- 競合状況
- HIV治験市場のプレイヤー別シェア
- M&A契約と提携分析
- 市場プレイヤー評価
- Gilead Sciences
- 概要
- 事業情報
- 収益
- 平均販売価格
- SWOT分析
- 最近の動向
- ViiV Healthcare
- GSK plc
- Johnson & Johnson
- Merck & Co. Inc.
- Pfizer Inc.
- Bristol Myers Squibb
- AbbVie Inc.
- Sanofi
- PPD Inc.
- IQVIA Inc.
- ICON plc
- WuXi AppTec
- Bionor Holding AS
- Charles River Laboratories
- Syneos Health
- BioNTech SE
- Sangamo Therapeutics
- Parexel International Corporation
- その他
- 調査方法論
- 調査データ
- 二次データ
- 主な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次情報の内訳
- 二次・一次調査
- 主要な業界インサイト
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査の仮定
- 仮定
- 制約事項
- リスク評価
- 付録
- 議論ガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
“`
*** 本調査レポートに関するお問い合わせ ***

HIV治験とは、ヒト免疫不全ウイルス(HIV)感染症に対する新たな治療薬、予防薬、ワクチンの有効性と安全性を評価するため、ヒトを対象に行われる臨床研究の総称です。これにより、HIV感染症はかつて致死的な病から管理可能な慢性疾患へと変革し、感染者の生活の質向上と公衆衛生改善に大きく貢献してきました。その継続的な努力が、世界中の多くの人々の命と健康を守り続けています。
治験は通常、段階的に進められます。第一相では少数の被験者で薬剤の安全性や体内動態、適切な投与量を評価し、第二相では数百人規模のHIV感染者で初期の有効性と安全性を確認します。第三相では数千人規模の多様な集団で既存治療法と比較し、有効性と安全性を大規模に検証、承認申請の根拠とします。承認後も、長期的な影響などを調査する第四相治験が行われることがあります。
HIV治験の主要な目的は、抗レトロウイルス療法(ART)の絶え間ない進化です。より強力で副作用の少ない新規薬剤の開発、多剤併用療法の最適化、服薬アドヒアランス向上のための持続性注射剤やインプラントといった新しい投与形態の研究が含まれます。また、HIV感染を防ぐ予防ワクチンの開発も重要な治験領域であり、ウイルスの多様性や免疫応答の複雑さから多くの課題が存在するものの、予防的・治療的ワクチンの