インビボCRO市場規模と展望、2025-2033年

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
## インビボCRO市場に関する詳細な市場調査レポート概要
### 1. 市場概要とインビボCROの定義
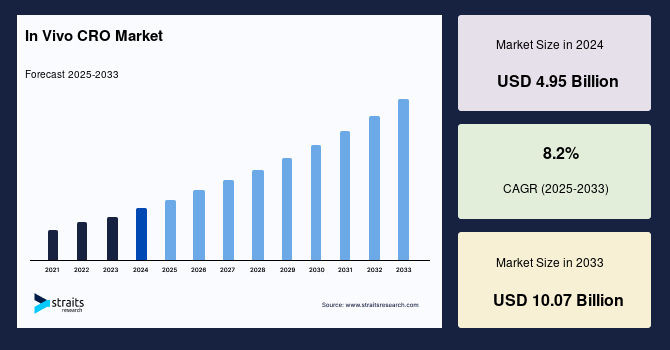
世界のインビボCRO市場は、2024年に49.5億米ドルの規模に達し、2025年には53.6億米ドル、そして2033年までには100.7億米ドルに成長すると予測されており、予測期間(2025年~2033年)における年平均成長率(CAGR)は8.2%に達すると見込まれています。新興国における受託研究機関による国際標準の採用が進むことで、製薬・バイオテクノロジー企業からの受託研究に対する需要が向上し、市場の成長に貢献すると予測されています。
インビボCRO(Contract Research Organization)とは、生命体を用いた実験や試験の管理に特化した、アウトソーシング型の臨床研究サービスを提供する専門機関です。製薬・バイオテクノロジー分野の複雑性と厳しい規制要件を考慮すると、インビボCROは新しい医薬品や治療法の開発を促進する上で不可欠な存在です。インビボCRO企業は、新規医薬品候補の安全性、有効性、薬物動態を評価するために、動物モデルを頻繁に組み込んだ前臨床試験および臨床試験を設計・実施します。彼らは製薬企業、学術機関、政府機関と密接に連携し、倫理基準および規制要件への遵守を徹底しています。これらの機関は、最先端の設備と、毒性学、薬理学、獣医学に関する専門知識を有しています。
インビボCROは、試験プロトコルの作成、被験者の募集、データ収集、分析、報告を含む包括的なサービスを提供します。彼らは、動物の適切なケアについて教育を受けた資格のある科学者、獣医、およびサポートスタッフと協力し、厳格な品質管理手順に従っています。このように、インビボCROは、医薬品開発の初期段階から後期段階まで、多様なニーズに応えることで、その重要性を増しています。
### 2. 市場の成長要因 (Drivers)
インビボCRO市場の成長を牽引する主要な要因は多岐にわたります。
まず、**新興国における国際標準の採用拡大**が挙げられます。品質管理システムに関する国際標準が、米国、欧州連合、日本などの先進国のインビボCROによって遵守されている一方で、新興国の政府も、受託研究機関が規制に適合していることを監視・検証するための新たな規制メカニズムを導入しています。これにより、新興国における受託研究機関が国際標準を採用する動きが加速し、製薬・バイオテクノロジー企業からの受託研究に対する需要が高まると予測されます。
次に、**製薬・バイオテクノロジー企業のアウトソーシングビジネスモデルへの移行**が顕著です。事業運営に伴う課題の増大と市場ダイナミクスの変化が複合的に作用し、多くの製薬・バイオテクノロジー企業はコスト削減とリスク管理の改善のためにアウトソーシングモデルを採用しています。これにより、インビボCROへの需要が構造的に増加しています。
さらに、**革新的な細胞・遺伝子治療の開発と商業化への投資増加**も大きな推進力です。細胞・遺伝子治療は複雑であり、高度な専門知識を必要としますが、現在の医療分野における未充足ニーズを満たすものとして期待されています。2021年4月時点でFDAによって承認された細胞・遺伝子治療は16件に上り、2020年には約362件の細胞・遺伝子治療が臨床試験段階に進んでいます。このように、潜在的な細胞治療候補の数が急速に増加し、臨床開発の様々な段階を迅速に進むにつれて、これらの治療法の研究開発サービスを提供する機関への需要が増大しています。これにより、バイオテクノロジー企業や学術機関などのエンドユーザーは、インビボCROの専門知識と科学的理解に依存するようになっています。インビボCROは、規制要件に関する明確な指針と、臨床試験のためのより広範な地理的リーチを提供するため、インビボCROサービス市場をさらに推進することになります。
地域特有の要因としては、**北米における政府機関からの研究活動奨励のための資金提供の増加**(例:米国国立衛生研究所(NIH))や、**アジア太平洋地域におけるCROの費用対効果の高さ**(特にインドや中国)が挙げられます。欧州では、大手製薬企業によるアウトソーシングへの支出増加、未充足ニーズのある希少疾患への注力、生物学的製薬の特許切れ、新規バイオシミラーの導入などが市場成長を促進すると考えられます。中南米では、政府の変更が医薬品市場を強化し、インビボ試験の需要を生み出すと予測されています。中東・アフリカ地域では、研究開発プロジェクトとライフサイエンス組織の数の増加が市場拡大の主要な原動力となるでしょう。
### 3. 市場の阻害要因 (Restraints)
インビボCRO市場は成長を続けているものの、いくつかの阻害要因も存在します。
まず、**インビボ産業が成熟市場へと発展したことによる競争激化**が挙げられます。これにより、価格上昇圧力と収益性への圧力が生じています。世界的に産業競争のレベルは着実に高まっており、ブラジル、韓国、台湾、中国といった新興国が世界市場でますます強力な競争相手となっています。また、オランダ、ドイツ、バミューダ、日本に本拠を置く製薬・バイオテクノロジー企業も、米国企業と激しく競合しています。
次に、**発展途上国のサービスプロバイダーにおける規制遵守の課題**があります。最近制定された法律に発展途上国のサービスプロバイダーが準拠していない場合があり、その結果、欧州や米国で事業を行う製薬・バイオテクノロジー企業は、コンプライアンス上の困難な問題に直面する可能性があります。このため、一部の企業は規制違反を避けるために、社内研究機関や地域のサービスプロバイダーを利用することを好む傾向があります。インフラの拡大と高品質なサービスへの需要の高まりにより、世界のインビボCROは既存の規制基準への準拠が求められており、これによりCROは品質保証・管理システムを開発し、規制遵守を確保することが不可欠となっています。
さらに、**特定の動物モデルにおける限界**も課題として挙げられます。例えば、腫瘍学分野では、マウス腫瘍がヒトのがんと比較して不均一性のレベルが低いという問題があり、これががん動物モデルの研究者にとって課題となっています。ヒトのがんは非常に高い不均一性を示すため、マウスモデルの均一性が低いことは、ヒトのがんの複雑な特性を完全に模倣することを困難にする場合があります。
### 4. 市場機会 (Opportunities)
インビボCRO市場には、複数の重要な機会が存在し、今後の成長をさらに加速させる可能性を秘めています。
最も顕著な機会の一つは、**新興国における国際標準の採用拡大**です。これにより、これらの地域の受託研究機関が国際的な品質基準に準拠するようになり、先進国の製薬・バイオテクノロジー企業からの信頼と需要が高まります。これにより、アウトソーシングの地理的範囲が拡大し、インビボCRO市場全体の活性化に繋がります。
また、**細胞・遺伝子治療の開発と商業化の加速**は、インビボCROにとって大きな成長機会をもたらします。これらの複雑な治療法は高度な専門知識と厳格な規制遵守を要求するため、インビボCROの専門性が不可欠となります。FDAによる承認数の増加や臨床試験段階に進む候補の急増は、これらの治療法の研究開発サービスを提供するインビボCROへの持続的な需要を生み出しています。インビボCROは、規制要件に関する明確なガイダンスと、世界規模での臨床試験の実施能力を提供することで、この分野において不可欠なパートナーとしての地位を確立しています。
さらに、**インビボCROの専門知識、科学的理解、規制に関する明確な情報提供、および広範な地理的リーチ**は、市場における主要な機会です。特に、多様な規制環境下でグローバルな臨床試験を実施する能力は、製薬・バイオテクノロジー企業にとって非常に価値があります。
地域別の機会としては、**北米における高品質な研究と実績**、政府機関による積極的な資金提供が、さらなる研究投資を促すでしょう。**アジア太平洋地域**では、経済発展と高度なヘルスケアインフラに加え、インドや中国などの新興経済国へのインビボサービスのアウトソーシングが増加しており、CROによる提携や投資の増加が市場拡大を加速させると予測されています。**欧州**では、希少疾患への注力、生物学的製剤の特許切れ、新規バイオシミラーの導入が市場成長を促進し、コンビナトリアルケミストリー、ゲノミクス、ハイスループットスクリーニング、プロテオミクスといった創薬アプローチにおける急速な変化が、データ管理システムの進歩によるデータ量の大幅な増加に伴い、創薬から開発段階への移行を変化させています。**中南米**では、インビボ試験能力を強化するための努力が多くのグループによって行われており、政府の変更が医薬品市場を強化し、インビボ試験の需要を生み出すと予測されています。**中東・アフリカ**地域は、高品質な医療施設、発展したインフラ、低い運営コストといった利点を提供し、地域における研究開発プロジェクトとライフサイエンス組織の増加が市場拡大の主要な推進力となるでしょう。
### 5. セグメント分析
#### 5.1. 地域別分析
* **北米:** 世界市場で最も大きなシェアを占めており、予測期間中に8.5%のCAGRを示すと推定されています。この優位性は、技術的に高度なインビボCROの存在、米国国立衛生研究所(NIH)などの政府機関による研究活動奨励のための資金提供の増加に起因します。地域の企業の高品質なサービスと実績により、予測期間中にはさらなる研究投資が行われると予想されます。加えて、多数の医薬品開発活動、多くの製薬・バイオテクノロジー企業の存在、および地域における臨床試験の数の多さが市場拡大に貢献しています。
* **アジア太平洋:** 予測期間中に9.4%のCAGRで最も速い成長を示すと予想されています。インドや中国などの国々における臨床研究機関(CRO)の費用対効果の高さが、この地域の経済発展と高度なヘルスケアインフラに加えて、成長を牽引すると見込まれています。CROによる提携や投資の増加、およびインドや中国といった新興経済国へのインビボサービスのアウトソーシングの割合の増加が、予測期間中の市場拡大を加速させる要因として挙げられます。
* **欧州:** 予測期間中、市場成長を牽引する要因としては、大手製薬企業によるアウトソーシングへの支出増加、未充足ニーズのある希少疾患への重点化、生物学的製薬の特許切れ、および新規バイオシミラーの導入などが挙げられます。欧州では、創薬アプローチにおいて急速な変化が起きています。コンビナトリアルケミストリー、ゲノミクス、ハイスループットスクリーニング、プロテオミクスといった技術は、データベース管理システムの進歩による利用可能なデータ量の大幅な増加により、創薬から開発段階への移行を変革しています。
* **中南米:** 予測期間中、著しくかつ収益性の高い成長を遂げると推定されています。この地域では、インビボ試験能力を強化するために多くの異なるグループが多大な努力を払っています。政府の変更が医薬品市場を強化し、それがインビボ試験への地域的需要を生み出すと予測されています。
* **中東・アフリカ:** この地域における研究開発プロジェクトとライフサイエンス組織の数の増加が、予測期間中の市場拡大の主要な推進力となると予測されています。この地域は、市場での地位を強化するために、世界の他の地域で一般的な慣行を採用し、他の地域のインビボCROと密接に協力しています。さらに、中東・アフリカ(MEA)のインビボCRO産業は、高品質な医療施設、発展したインフラ、低い運営コストといった利点を提供し、これらすべてが市場の成長に貢献しています。
#### 5.2. 動物種別分析
グローバルなインビボCRO市場は、げっ歯類と非げっ歯類に二分されます。
* **げっ歯類:** このセグメントが世界市場を支配しており、予測期間中に8.6%のCAGRを示すと予測されています。げっ歯類は、行動的、生化学的、遺伝的構成において人間との強い類似性があるため、医学研究のモデルとして頻繁に利用されています。彼らは臨床試験で最も頻繁に使用される種であり、人間の様々な疾患兆候を模倣することができます。バイオメディカル研究財団(FBR)によると、すべての実験動物の95%がげっ歯類であるとされています。ラットとマウスは小さく、世話が簡単で、環境に順応しやすい特性を持っています。頻繁に繁殖し、寿命が短いため、短期間で複数のげっ歯類の世代を観察することが可能です。FBRは、重症複合免疫不全(SCID)マウスのような免疫不全動物が、がんや健康なヒト組織の研究モデルとして利用できると述べています。
* **非げっ歯類:** げっ歯類と比較して利用頻度は低いものの、特定の研究目的や、げっ歯類では再現が難しい生理学的または病理学的特性を持つ疾患の研究において重要な役割を果たしています。
#### 5.3. 疾患領域別分析
グローバルなインビボCRO市場は、自己免疫/炎症性疾患、疼痛管理、腫瘍学、中枢神経系疾患、糖尿病、肥満、その他の疾患に分類されます。
* **腫瘍学:** このセグメントが最大の市場シェアを占めており、予測期間中に8.2%のCAGRを示すと予測されています。マウスは、ヒトとマウスの腫瘍が多くの生理学的および遺伝的特性を共有しているため、ヒトのがん研究において優れたモデルであることが証明されています。これは、マウスとヒトの間にがんを引き起こす遺伝子の高い割合が共通しているためです。マウスとヒトは、分子、細胞、解剖学的構成において驚くほど類似しています。がんの特定の特性が重要な機能と特性を持つことは広く知られています。マウスのRNI様遺伝子はヒトの遺伝子と80%以上同一であるため、マウスはがんが治療にどのように反応し、どのような基本的なメカニズムを発達させるかを調査するための非常に効果的な実験的に扱いやすいモデルです。しかし、マウス腫瘍はヒトのがんが示す高いレベルの不均一性とは対照的に、不均一性のレベルが低いという課題があり、これはがん動物モデルを研究する科学者にとって課題となっています。最も広く使用され、費用対効果の高い従来の腫瘍研究モデルは、免疫不全動物または免疫応答性動物に直所的または皮下的に移植された異種移植腫瘍または同系腫瘍を持つマウスです。
* **その他:** 自己免疫/炎症性疾患、疼痛管理、中枢神経系疾患、糖尿病、肥満などの疾患領域も、それぞれの治療法開発においてインビボCROサービスの重要な需要源となっています。
#### 5.4. サービスタイプ別分析(毒性学)
グローバル市場は非GLPとGLP毒性学に分かれています。
* **GLP毒性学:** このセグメントが市場への最も重要な貢献者であり、予測期間中に8.8%のCAGRを示すと推定されています。安全性薬理学、遺伝毒性、反復投与毒性などの臨床調査は、人間の安全な曝露のために不可欠であり、GLP(Good Laboratory Practice:優良試験所規範)基準に従って実施される必要があります。これらの臨床調査は、IND(治験薬申請)が提出される前に完了していなければなりません。INDが承認された後も、慢性毒性、発生毒性および生殖毒性、遺伝毒性、発がん性に関する追加のGLP試験が開発の臨床段階中に実施される必要があります。安全性試験の結果を分析する際には、GLPの要件を遵守することが必須です。GLPは、データの信頼性と完全性を保証し、規制当局の承認プロセスにおいて極めて重要な役割を果たします。
* **非GLP毒性学:** GLP毒性学と比較して、初期の探索的研究やスクリーニング目的など、より柔軟なプロトコルと迅速なターンアラウンドが求められる場合に利用されます。厳格な規制要件が適用されないため、コストを抑えつつ初期の安全性評価を行うことが可能です。
### 結論
世界のインビボCRO市場は、製薬・バイオテクノロジー産業におけるアウトソーシングの増加、革新的な治療法(特に細胞・遺伝子治療)への投資の拡大、そして新興国における国際標準の採用といった複数の強力な成長要因によって、今後も堅調な成長が続く見込みです。競争激化や規制遵守の課題といった阻害要因は存在するものの、インビボCROの専門知識と広範なサービス提供能力が、これらの課題を乗り越え、新たな市場機会を捉える原動力となるでしょう。特に、北米の技術的優位性、アジア太平洋地域のコスト効率と成長性、欧州の多様な創薬アプローチ、中南米および中東・アフリカのインフラとR&Dの進展が、地域ごとの市場拡大を牽引します。げっ歯類モデルの広範な利用や腫瘍学分野での需要の高さ、そしてGLP毒性学の重要性は、市場の構造と成長の方向性を示す重要な要素です。インビボCROは、医薬品開発の複雑なプロセスにおいて不可欠なパートナーとして、今後もその役割を拡大していくでしょう。
Report Coverage & Structure
- 目次
- セグメンテーション
- 調査方法
- 無料サンプルを入手
- 目次
- エグゼクティブサマリー
- 調査範囲とセグメンテーション
- 調査目的
- 制限事項と仮定
- 市場範囲とセグメンテーション
- 考慮される通貨と価格設定
- 市場機会評価
- 新興地域/国
- 新興企業
- 新興アプリケーション/最終用途
- 市場動向
- 推進要因
- 市場警戒要因
- 最新のマクロ経済指標
- 地政学的影響
- 技術的要因
- 市場評価
- ポーターの5フォース分析
- バリューチェーン分析
- 規制の枠組み
- 北米
- 欧州
- アジア太平洋
- 中東およびアフリカ
- ラテンアメリカ
- ESGトレンド
- グローバル インビボCRO 市場規模分析
- グローバル インビボCRO 市場概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- グローバル インビボCRO 市場概要
- 北米市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- 米国
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- カナダ
- 欧州市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- 英国
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- ドイツ
- フランス
- スペイン
- イタリア
- ロシア
- 北欧
- ベネルクス
- その他の欧州
- アジア太平洋市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- 中国
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- 韓国
- 日本
- インド
- オーストラリア
- シンガポール
- 台湾
- 東南アジア
- その他のアジア太平洋
- 中東およびアフリカ市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- アラブ首長国連邦
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- トルコ
- サウジアラビア
- 南アフリカ
- エジプト
- ナイジェリア
- その他のMEA
- ラテンアメリカ市場分析
- 概要
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- ブラジル
- タイプ別
- 概要
- タイプ別金額
- げっ歯類
- 金額別
- 非げっ歯類
- 金額別
- 疾患適応症別
- 概要
- 疾患適応症別金額
- 自己免疫/炎症性疾患
- 金額別
- 疼痛管理
- 金額別
- 腫瘍学
- 金額別
- 中枢神経系疾患
- 金額別
- 糖尿病
- 金額別
- 肥満
- 金額別
- その他
- 金額別
- GLPタイプ別
- 概要
- GLPタイプ別金額
- 非GLP
- 金額別
- GLP毒性学
- 金額別
- タイプ別
- メキシコ
- アルゼンチン
- チリ
- コロンビア
- その他のラテンアメリカ
- 競合状況
- インビボCRO 市場プレイヤー別シェア
- M&A契約と提携分析
- 市場プレイヤー評価
- IQVIA Inc.
- 概要
- 事業情報
- 収益
- ASP
- SWOT分析
- 最近の動向
- Crown Bioscience
- Taconic Biosciences, Inc.
- Psychogenic Inc.
- Evotec
- Janvier Labs
- Biocytin
- Gem Pharmatech
- Charles River Laboratories
- Icon Plc
- LabCorp Drug Development
- Parexel International Corporation
- SMO Clinical Research (I) Pvt Ltd.
- IQVIA Inc.
- 調査方法
- 調査データ
- 二次データ
- 主要な二次情報源
- 二次情報源からの主要データ
- 一次データ
- 一次情報源からの主要データ
- 一次情報の内訳
- 二次および一次調査
- 主要な業界インサイト
- 二次データ
- 市場規模推定
- ボトムアップアプローチ
- トップダウンアプローチ
- 市場予測
- 調査の前提
- 前提
- 制限事項
- リスク評価
- 調査データ
- 付録
- 議論ガイド
- カスタマイズオプション
- 関連レポート
- 免責事項
*** 本調査レポートに関するお問い合わせ ***

インビボCROとは、医薬品や医療機器の研究開発において、生体内(インビボ)での試験や評価を専門的に受託する機関を指します。CROはContract Research Organizationの略であり、日本語では「医薬品開発業務受託機関」と訳されます。特に「インビボ」という言葉が付くことで、動物を用いた前臨床試験や、初期の臨床試験における生体反応の評価など、生きた生物個体を用いた研究に特化していることを明確に示しています。製薬企業やバイオテクノロジー企業、学術機関などが、自社で対応しきれない専門的な試験や、大規模なリソースを必要とする研究を外部のインビボCROに委託することで、開発期間の短縮、コスト削減、そして研究の質の向上を図っています。
インビボCROが提供するサービスは多岐にわたりますが、主なものとしては、医薬品候補物質の有効性や安全性を評価するための前臨床試験が挙げられます。具体的には、薬物動態試験(PK試験)として、薬物が体内でどのように吸収され、分布し、代謝され、排泄されるかを評価します。また、薬力学試験(PD試験)では、薬物が生体にどのような作用を及ぼすかを詳細に解析します。安全性試験においては、単回投与毒性試験、反復投与毒性試験、遺伝毒性試験、がん原性試験、生殖発生毒性試験など、多岐にわたる毒性評価を実施し、ヒトへの適用における安全性を確立するための重要なデータを提供しています。さらに、特定の疾患モデル動物を用いた薬効薬理試験を通じて、医薬品候補物質の治療効果を検証することも重要な業務の一つです。近年では、特定の疾患領域、例えばがん、中枢神経疾患、感染症、自己免疫疾患などに特化した専門性の高いインビボCROも増えており、より高度な専門知識と技術を提供しています。
これらのインビボCROのサービスが製薬企業やバイオテクノロジー企業にとって不可欠であるのは、主にいくつかの理由があります。一つは、高度な専門知識と最新の設備へのアクセスです。特に中小規模の企業では、自社で全ての試験設備を整え、専門人材を雇用することが難しい場合が多く、CROの活用は効率的な研究開発を可能にします。また、規制要件への対応も重要な側面です。インビボCROは、医薬品開発の国際的な基準であるGLP(Good Laboratory Practice:医薬品の安全性に関する非臨床試験の実施の基準)をはじめとする厳格な規制に準拠した試験を実施する能力を持っており、信頼性の高いデータを提供することで、国内外の薬事申請を円滑に進める手助けをします。さらに、研究開発の初期段階におけるリスクを分散し、特定のプロジェクトに集中できる環境を整えることで、全体の開発効率を高めることにも貢献しています。
インビボCROの業務を支える技術もまた、日々進化を遂げております。生体イメージング技術はその代表例であり、MRI、PET、SPECT、CT、あるいは蛍光・生物発光イメージングなどを活用することで、動物個体内で薬物の挙動や疾患の状態を非侵襲的にリアルタイムで観察することが可能になりました。これにより、より少ない動物で多くの情報を得ることができ、動物福祉の観点からもメリットがあります。また、CRISPR/Cas9などの遺伝子編集技術の進歩は、特定の遺伝子を欠損させたり、ヒトの遺伝子を導入したりした疾患モデル動物の作製を容易にし、より精度の高い薬効評価を可能にしています。インビボでのサンプル(血液、組織など)から得られたゲノム、プロテオーム、メタボロームといったオミックスデータを解析する技術も重要性を増しており、バイオインフォマティクスやAIを活用したデータ解析は、創薬ターゲットの探索やバイオマーカーの同定に貢献しています。これらの先進技術を積極的に取り入れることで、インビボCROは医薬品開発のさらなる加速と成功確率の向上に寄与し続けているのです。