臓器保存市場 規模・シェア分析 – 成長動向と予測 (2025年~2030年)
臓器保存市場レポートは、手法(静的低温保存(SCS)など)、保存液(ウィスコンシン大学(UW)液、セルシオールなど)、製品タイプ(保存液など)、臓器タイプ(腎臓、肝臓など)、エンドユーザー(移植センター、病院など)、および地域(北米、欧州など)別に区分されます。市場予測は、金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
臓器保存市場の概要
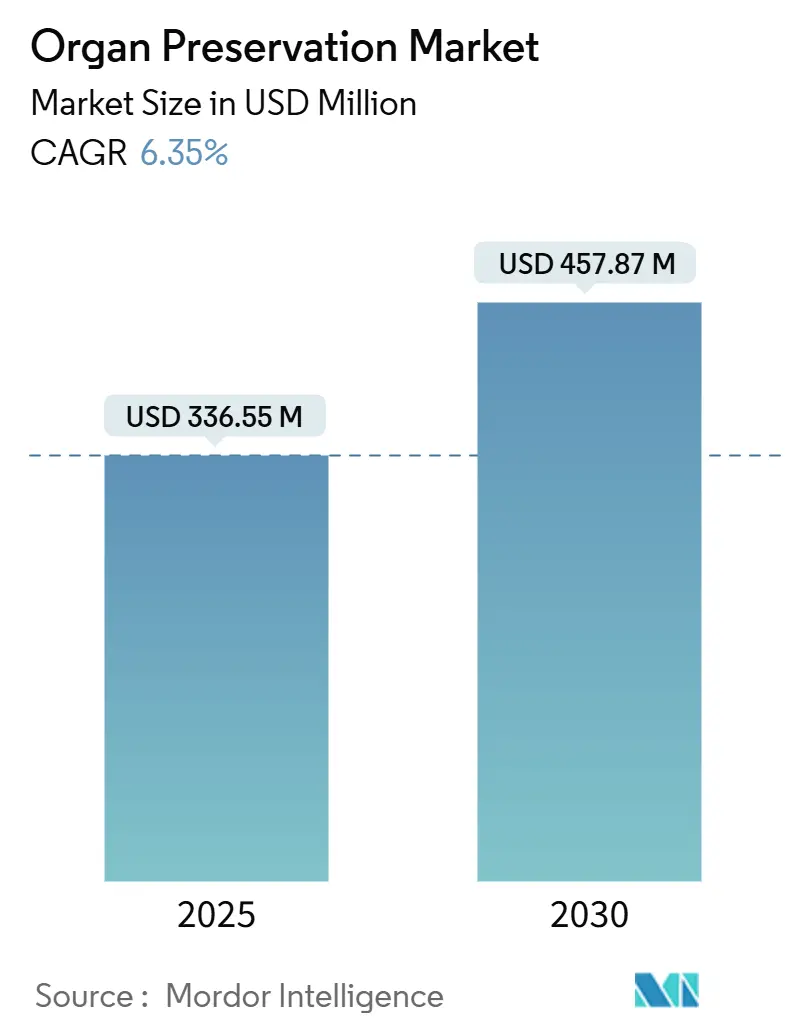
臓器保存市場は、2025年には3億3,655万米ドルに達し、2030年までに4億5,787万米ドルに成長すると予測されており、予測期間中の年平均成長率(CAGR)は6.35%です。この成長は、移植の必要性とドナー供給の間の拡大するギャップを反映しています。例えば、米国では10万3千人が臓器移植を待っている一方で、2024年の実施件数は4万8千件にとどまっています。
市場の主要な動向と推進要因
1. 高齢化人口における多臓器不全の増加: 65歳以上の人口が増加し、慢性腎臓病、糖尿病、心血管疾患などの加齢に伴う疾患が増えることで、臓器移植の需要が高まっています。これにより、長時間の保存や機能評価に対応できる信頼性の高い保存技術が求められています。静的低温保存(SCS)が依然として広く利用されていますが、機械灌流(MP)は、高齢ドナーからの限界臓器を蘇生させる能力において特に価値があります。
2. 保存技術とデバイスの技術進歩: 機械灌流は、ドナー臓器を生理学的温度に保ち、心臓移植における初期グラフト機能不全を大幅に減少させることが示されています。循環死後臓器提供(DCD)心臓の利用も、ノルモサーミック局所灌流(NRP)によって可能になっています。デバイスメーカーは、GPS追跡、圧力調整、温度遠隔測定などの機能を統合し、輸送中の臓器の状態をリアルタイムで監視できるようにしています。X-Thermaのタンパク質模倣氷阻害剤のような凍結保存研究は、保存期間を数時間から数週間に延長することを目指しており、これらの革新は臓器の割り当て時間を短縮し、廃棄率を低下させ、ドナー基準を拡大するのに役立っています。
3. 臓器提供に関する政府およびNGOのイニシアチブの増加: 世界保健総会は、2035年までにすべての加盟国が移植ニーズを満たすことを求める決議WHA77.4を採択しました。米国では、HRSA OPTN近代化イニシアチブが割り当てソフトウェアを近代化し、臓器調達組織(OPO)のパフォーマンス指標を設定しています。メディケアの「臓器移植アクセス増加モデル」は、病院の支払いを腎臓移植量の増加と結びつけています。中国の集中型割り当てプラットフォーム(COTRS)は透明性を高め、提供を促進しています。
4. 体外灌流に対する償還コードの出現: 2024年に発表されたCMS規則は、2025年7月から体外灌流の消耗品および専門サービスに対する独自の支払いバンドルを確立しました。これにより、米国の一部の移植センターでは、Organ Care Systemデバイスの導入承認が迅速化されています。欧州の医療システムも同様のコードを試験的に導入しており、保険会社は3万米ドルの灌流キットが40万米ドルの再移植を回避できることを認識し始めています。
市場の抑制要因
1. 臓器移植および保存デバイスの高コスト: Millimanの推定によると、65歳未満の患者の移植費用は年間5.2%、高齢者では9.1%増加しています。Organ Care System Heartのようなデバイスは、病院に25万米ドル以上の設備投資を要求し、使い捨てセットは1回の手術あたり約4万米ドルかかります。保存液も、University of Wisconsin溶液が1リットルあたり120米ドルであるのに対し、Marshall’s溶液は10米ドルと、価格に大きな差があります。これにより、特に発展途上地域では、ノルモサーミック機械灌流(NMP)の導入が遅れています。
2. ノルモサーミック灌流に対する規制の不確実性: ノルモサーミックデバイスは、世界中で様々な規制枠組みに直面しています。FDAによるOrgan Care System Heartの審査には5,518日を要し、長期にわたる証拠要件が浮き彫りになりました。欧州では、Advanced Therapy Medicinal Product(ATMP)規則が生物製剤を注入した溶液に追加のチェックポイントを導入し、多国間試験を遅らせています。アジア太平洋地域の規制当局は、体外灌流に関する調和されたガイダンスを欠いており、デバイスメーカーは同時ではなく順次申請を行う必要があります。
セグメント分析
* 技術別: 静的低温保存(SCS)は、その簡便さ、低コスト、長年の実績から2024年に臓器保存市場の62.25%を占めました。しかし、ノルモサーミック機械灌流(NMP)は、2030年までに年間10.45%で成長すると予測されており、多施設データでは、氷保存と比較して6ヶ月後の心臓グラフト生存率が94%と高いことが示されています。
* 保存液別: University of Wisconsin溶液は、2024年に臓器保存市場の45.53%を占めました。その高浸透圧で抗酸化物質が豊富な特性は、細胞浮腫やフリーラジカル損傷を最小限に抑えます。一方、Custodiol HTKは、低粘度と多臓器調達におけるコストパリティの魅力から、9.35%のCAGRで拡大しています。
* 製品タイプ別: 保存液は、すべての移植に必要であるため、2024年に臓器保存市場の49.82%を占めました。しかし、輸送システムおよびデバイスは、Paragonix SherpaPak、LIVERguard、BAROguardなどのプラットフォームがGPS座標、内部温度、圧力をリアルタイムで記録し、心臓移植における死亡率を54%削減した研究結果もあることから、9.26%のCAGRで最も速く成長しています。
* 臓器タイプ別: 腎臓は、最大の移植量と堅牢な償還制度により、2024年に臓器保存市場の58.82%を占めました。しかし、虚血性損傷や物流のボトルネックにより、献体腎臓の20%が廃棄されています。機械灌流は、限界腎臓の受け入れを助け、廃棄率を削減しています。肺は、HOPE技術のような画期的な進歩により、10.62%のCAGRで最も高い成長を記録しています。
* エンドユーザー別: 移植センターは、ソリューションと設備の両方を購入し、プロトコル基準を決定し、直接償還を受けるため、2024年に収益の42.82%を占めました。臓器調達組織(OPO)は、ノルモサーミック局所灌流がDCDドナーあたり3つの臓器を回収できることから、11.32%のCAGRで最も速く成長しているエンドユーザーグループです。
地域分析
* 北米: 2024年に臓器保存市場の36.82%を占め、先進的なインフラ、OPTNの目標、灌流に対する支援的な償還制度に支えられています。広範な臨床試験、FDAデバイス承認、堅牢なドナー登録キャンペーンが優位性を維持しています。
* 欧州: 着実ながらも緩やかな成長を示しています。ドイツ、フランス、イタリア、スペイン、英国が導入を主導していますが、費用対効果の評価がデバイス価格に下向きの圧力をかけています。
* アジア太平洋: 中国、インド、日本で移植プログラムの能力が加速しているため、10.62%のCAGRで最も速く成長している地域です。中国のCOTRSプラットフォームは自発的な提供を合法化し、国民の信頼を高めました。インドの医療観光の増加と灌流デバイスの国内製造奨励策が、量と価格競争を促進しています。
競争環境
臓器保存市場は、戦略的買収によって特徴づけられる中程度の断片化が見られます。GetingeによるParagonixの4億7,700万米ドルの買収は、臓器特有の輸送デバイスとグローバルな販売網を提供しました。TransMedicsはノルモサーミック灌流プラットフォームを支配し、2024年第3四半期に64%の収益拡大を報告しています。投資トレンドは、臓器特有の最適化とデータ豊富なエコシステムに有利に働いています。競争は現在、臨床的証拠にかかっており、ParagonixはLIVERguardで移植後合併症を27%削減したと報告しています。大手企業は、サービス契約、トレーニングモジュール、クラウドダッシュボードを活用して、消耗品やソフトウェアサブスクリプションの顧客を囲い込み、移植センターにとって高い切り替えコストを生み出しています。
主要企業: XVIVO Perfusion AB、Organ Recovery Systems Inc.、TransMedics Inc.、Getinge AB、OrganOx Limitedなど。
最近の業界動向:
* 2025年4月: Paragonix Technologiesは、SherpaPakを使用した心臓移植患者の4年後の死亡率が54%減少したと報告しました。
* 2025年1月: LIVERguardが移植後合併症を27%削減したという臨床データが示され、米国の肝臓プログラムの20%以上がこのシステムを導入しています。
* 2024年6月: Paragonixは、FDA承認済みの初の膵臓輸送装置であるPancreasPakを発売し、最大21時間の温度安定保存を保証しています。
このレポートは、臓器保存市場に関する詳細な分析を提供しています。
1. はじめに
本調査は、ドナーの腎臓、肝臓、心臓、肺、膵臓、その他の固形臓器を採取から移植まで生存可能な状態に保つために特別に設計された保存液、輸送システム、および灌流装置の世界的な販売を「臓器保存市場」と定義しています。移植補助薬や長期的なバイオバンキング機器、細胞、血液、組織の保存製品は本調査の対象外です。
2. 市場の状況と推進要因
臓器保存市場は、高齢化人口における多臓器不全の発生率上昇、保存技術およびデバイスの技術進歩、臓器提供に対する政府およびNGOの取り組みの増加、世界的な移植プログラム能力の拡大、体外灌流に対する償還コードの出現、そして限界ドナー向けのAI駆動型臓器生存率分析といった複数の要因によって成長が推進されています。特に、新しいCMS(メディケア・メディケイドサービスセンター)の支払いバンドルが体外灌流の消耗品をカバーするようになったことで、病院が機械灌流デバイスを採用するインセンティブとなっています。
3. 市場の阻害要因
一方で、臓器移植および保存デバイスの高コスト、臓器保存に対する保険償還の限定、独自ソリューションのサプライチェーン制約、新規常温灌流に対する規制の不確実性などが市場の成長を抑制する要因として挙げられます。
4. 市場セグメンテーション
市場は以下の主要なセグメントにわたって詳細に分析されています。
* 技術別: 静的低温保存(SCS)、低体温機械灌流(HMP)、常温機械灌流(NMP)。
* 保存液別: University of Wisconsin (UW) Solution、Custodiol HTK Solution、Celsior、Perfadex Plus、その他。
* 製品タイプ別: 保存液、輸送システムおよびデバイス、アクセサリーおよびモニタリングソフトウェア。
* 臓器タイプ別: 腎臓、肝臓、肺、心臓、膵臓、その他。
* エンドユーザー別: 移植センター、病院、臓器調達機関(OPO)、専門クリニックおよび研究機関。
* 地域別: 北米(米国、カナダ、メキシコ)、ヨーロッパ(ドイツ、英国、フランス、イタリア、スペイン、その他ヨーロッパ)、アジア太平洋(中国、日本、インド、韓国、オーストラリア、その他アジア太平洋)、中東およびアフリカ(GCC、南アフリカ、その他中東およびアフリカ)、南米(ブラジル、アルゼンチン、その他南米)。
5. 市場規模と成長予測
臓器保存市場は、2025年には3億3,655万米ドルの規模に達すると予測されています。特に、常温機械灌流(NMP)は2030年までに年平均成長率(CAGR)10.45%で最も速く成長する技術と見込まれています。また、アジア太平洋地域は、移植プログラムの急速な拡大、規制の近代化、ドナー登録の増加により、CAGR 10.62%で最も魅力的な成長地域となっています。
6. 競争環境
市場は、XVIVO Perfusion AB、Organ Recovery Systems Inc.、Getinge AB、Bridge to Life Ltd.、TransMedics Inc.、OrganOx Limitedなど、多数の主要企業によって構成されています。特に、Paragonix Technologies(現在はGetinge傘下)は、SherpaPak、LIVERguard、BAROguardシステムを提供し、輸送デバイス分野をリードしています。
7. 調査方法論の信頼性
Mordor Intelligenceの調査は、透明性と信頼性を重視しています。調査方法には、移植外科医、臓器調達スタッフ、ソリューション開発者、流通パートナーへの一次調査(インタビュー)と、WHO、UNOS、Eurotransplantの公開データ、学術誌、企業報告書、特許情報などの二次調査が含まれます。市場規模の算出と予測は、2024年の移植件数に臓器別の保存率と必要なソリューション/ハードウェアの平均単位を乗じるトップダウンアプローチを主軸とし、サプライヤーの出荷データや平均販売価格(ASP)に基づくボトムアップチェックで補完されています。機械灌流の普及率、ドナーあたりの臓器回収数、インフレ調整済みASPの変動、ドナー構成、償還マイルストーンなどの主要変数が考慮され、多変量回帰分析とシナリオ分析を用いて2030年までの価値が予測されています。
他社の推定値との比較では、Mordor Intelligenceがポータブル灌流コンソールの計上方法、為替レートの基準年、生体ドナーの手順の含めるか否かといった要因を明確にし、デバイス収益、ASPの継続的な調整、厳格な更新サイクルを通じて、バランスの取れた透明性の高いベースラインを提供している点が強調されています。レポートは毎年更新され、重要なデバイス承認や政策変更があった場合には中間更新が行われます。
8. 主要な質問への回答
本レポートは、臓器保存市場の現在の価値、最も急速に成長している保存技術、最も魅力的な成長地域、償還モデルが技術採用に与える影響、および輸送デバイス分野の主要企業といった重要な質問に明確な回答を提供しています。
1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
-
4.2 市場の推進要因
- 4.2.1 高齢化人口における多臓器不全の発生率の増加
- 4.2.2 保存技術とデバイスの技術進歩
- 4.2.3 臓器提供に対する政府およびNGOの取り組みの増加
- 4.2.4 世界的な移植プログラム能力の拡大
- 4.2.5 体外灌流に対する償還コードの出現
- 4.2.6 限界ドナーのためのAI駆動型臓器生存率分析
-
4.3 市場の阻害要因
- 4.3.1 臓器移植および保存デバイスの高コスト
- 4.3.2 臓器保存に対する保険償還の制限
- 4.3.3 独自ソリューションのサプライチェーン制約
- 4.3.4 新規常温灌流に対する規制の不確実性
-
4.4 ポーターの5つの力
- 4.4.1 供給者の交渉力
- 4.4.2 買い手の交渉力
- 4.4.3 新規参入の脅威
- 4.4.4 代替品の脅威
- 4.4.5 競争の激しさ
5. 市場規模と成長予測 (金額 / 米ドル)
-
5.1 手法別
- 5.1.1 静的低温保存 (SCS)
- 5.1.2 低体温機械灌流 (HMP)
- 5.1.3 常温機械灌流 (NMP)
-
5.2 保存液別
- 5.2.1 ウィスコンシン大学 (UW) 液
- 5.2.2 クストジオール HTK 液
- 5.2.3 セルシオール
- 5.2.4 パーファデックスプラス
- 5.2.5 その他
-
5.3 製品タイプ別
- 5.3.1 保存液
- 5.3.2 輸送システム&デバイス
- 5.3.3 付属品&監視ソフトウェア
-
5.4 臓器タイプ別
- 5.4.1 腎臓
- 5.4.2 肝臓
- 5.4.3 肺
- 5.4.4 心臓
- 5.4.5 膵臓
- 5.4.6 その他
-
5.5 エンドユーザー別
- 5.5.1 移植センター
- 5.5.2 病院
- 5.5.3 臓器提供機関 (OPO)
- 5.5.4 専門クリニック&研究機関
-
5.6 地域別
- 5.6.1 北米
- 5.6.1.1 米国
- 5.6.1.2 カナダ
- 5.6.1.3 メキシコ
- 5.6.2 欧州
- 5.6.2.1 ドイツ
- 5.6.2.2 英国
- 5.6.2.3 フランス
- 5.6.2.4 イタリア
- 5.6.2.5 スペイン
- 5.6.2.6 その他の欧州
- 5.6.3 アジア太平洋
- 5.6.3.1 中国
- 5.6.3.2 日本
- 5.6.3.3 インド
- 5.6.3.4 韓国
- 5.6.3.5 オーストラリア
- 5.6.3.6 その他のアジア太平洋
- 5.6.4 中東およびアフリカ
- 5.6.4.1 GCC
- 5.6.4.2 南アフリカ
- 5.6.4.3 その他の中東およびアフリカ
- 5.6.5 南米
- 5.6.5.1 ブラジル
- 5.6.5.2 アルゼンチン
- 5.6.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
-
6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要事業セグメント、財務、従業員数、主要情報、市場ランク、市場シェア、製品とサービス、および最近の動向の分析を含む)
- 6.3.1 XVIVO Perfusion AB
- 6.3.2 Organ Recovery Systems Inc.
- 6.3.3 Getinge AB
- 6.3.4 Bridge to Life Ltd.
- 6.3.5 TransMedics Inc.
- 6.3.6 21st Century Medicine Inc.
- 6.3.7 Dr. Franz Kohler Chemie GmbH
- 6.3.8 Essential Pharmaceuticals LLC
- 6.3.9 Waters Medical Systems LLC
- 6.3.10 OrganOx Limited
- 6.3.11 CryoLife Inc.
- 6.3.12 BioLife Solutions Inc.
- 6.3.13 Preservation Solutions Inc.
- 6.3.14 Lifeline Scientific Inc.
- 6.3.15 Vascular Perfusion Solutions Inc.
- 6.3.16 KARA Perfusion
- 6.3.17 EBERS Medical Technology SL
7. 市場機会と将来展望
*** 本調査レポートに関するお問い合わせ ***

臓器保存とは、臓器移植を目的として、ドナーから摘出された臓器をレシピエントに移植するまでの間、その機能と生存能力を維持するための医療技術およびプロセス全般を指します。臓器は体外に出ると、血液供給が途絶えることによる虚血状態に陥り、細胞が損傷を受け始めます。この虚血による損傷を最小限に抑え、臓器の品質を保ちながら保存時間を延長することが、臓器保存の最も重要な目的です。これにより、ドナーとレシピエントのマッチング、臓器の輸送、移植手術の準備に必要な時間を確保し、移植の成功率を高めることが可能となります。
臓器保存の方法には、主に静的保存と動的保存の二種類があります。静的保存は、最も広く用いられている方法であり、臓器を特殊な保存液で灌流した後、低温環境下(通常は0〜8℃)で氷上に保管する冷却保存が代表的です。この低温は臓器の代謝活動を大幅に低下させ、酸素消費量を減少させることで、虚血による損傷の進行を遅らせます。保存液としては、UW液(University of Wisconsin solution)、HTK液(Histidine-Tryptophan-Ketoglutarate solution)、Celsior液などが開発されており、それぞれが細胞の腫脹防止、フリーラジカルの除去、エネルギー代謝の維持などに寄与する成分を含んでいます。しかし、静的保存では臓器の代謝が完全に停止するわけではなく、保存時間が長くなるにつれて損傷が蓄積するリスクが高まります。
一方、動的保存、または機械灌流は、臓器に保存液を継続的に循環させることで、より積極的に臓器の機能を維持しようとする方法です。これには、低温で灌流を行う低体温機械灌流(HMP: Hypothermic Machine Perfusion)と、体温に近い温度で灌流を行う常温機械灌流(NMP: Normothermic Machine Perfusion)があります。低体温機械灌流は、静的保存よりも均一な冷却と代謝産物の除去が可能であり、保存時間の延長や臓器の評価に優れています。常温機械灌流は、臓器を生理的条件に近い状態で維持するため、代謝活動を継続させながら、臓器の機能評価をより正確に行うことができます。また、損傷した臓器の修復や、薬剤投与による治療の可能性も秘めており、特に脳死ドナーだけでなく、心停止ドナーからの臓器利用を拡大する上で重要な役割を果たしています。
臓器保存の主な用途は、言うまでもなく臓器移植です。心臓、肺、肝臓、腎臓、膵臓、小腸など、様々な臓器の移植において不可欠な技術であり、ドナーから摘出された臓器を安全にレシピエントへ届けるための生命線となっています。また、臓器保存技術は、移植医療だけでなく、研究開発分野においても重要な役割を担っています。例えば、臓器の生理機能や病態を体外で研究するためのモデルとして、あるいは新しい治療法や薬剤の効果を評価するためのプラットフォームとして利用されています。将来的には、再生医療の分野において、人工臓器やバイオエンジニアリングされた組織の保存、あるいは細胞シートや幹細胞を用いた臓器修復技術と連携することで、その用途はさらに拡大すると考えられています。
関連技術としては、まず保存液の継続的な開発が挙げられます。より効果的に細胞損傷を防ぎ、保存期間を延長するための新しい成分や配合の研究が進められています。次に、機械灌流装置の進化です。ポンプ、酸素供給装置、フィルター、温度制御システム、そして臓器の生理学的パラメータをリアルタイムでモニタリングするセンサーなど、高度な技術が統合された装置が開発されています。これにより、灌流中の臓器の状態を詳細に把握し、最適な保存条件を維持することが可能になっています。さらに、バイオエンジニアリング技術の進展も臓器保存に影響を与えています。例えば、脱細胞化臓器を足場として利用し、そこにレシピエントの細胞を再構築する技術や、3Dバイオプリンティングによる臓器作製技術は、将来的に保存すべき臓器そのものの供給源を変える可能性を秘めています。また、臓器の長期保存を目指す凍結保存、特にガラス化技術の研究も進められていますが、臓器全体での実現にはまだ多くの課題が残されています。
市場背景としては、世界的な臓器不足が深刻化していることが挙げられます。移植を待つ患者数は増加の一途を辿っており、利用可能な臓器を最大限に活用することが喫緊の課題です。臓器保存技術の進歩は、これまで利用が困難であった心停止ドナーからの臓器や、軽度の損傷がある臓器の利用を可能にし、移植機会の拡大に貢献しています。特に、機械灌流装置の市場は、その有効性が認識されるにつれて急速に成長しており、主要な医療機器メーカーやバイオテクノロジー企業がこの分野に参入しています。これらの技術革新は、移植の成功率向上、合併症の減少、ひいては医療費の削減にも繋がり、医療経済的な観点からもその価値が高く評価されています。各国政府や医療機関も、臓器移植プログラムの強化の一環として、先進的な臓器保存技術の導入を積極的に推進しています。
将来展望としては、臓器保存期間のさらなる延長が最大の目標です。現在の数時間から数十時間の保存期間を、数日、さらには数週間にまで延ばすことができれば、臓器の輸送やレシピエントの準備、手術計画の柔軟性が飛躍的に向上し、より多くの患者に移植の機会を提供できるようになります。また、保存中の臓器の品質をより正確に評価し、移植後の機能予後を予測する技術の確立も重要です。これにより、移植に適さない臓器を事前に識別し、無駄な移植を避けることができます。さらに、機械灌流システムを利用して、損傷した臓器を修復したり、遺伝子治療や幹細胞治療を施したりする「臓器再調整(organ reconditioning)」の概念も注目されています。これにより、現在では移植不適格とされる臓器も利用可能になる可能性があります。最終的には、人工知能(AI)やビッグデータ解析を活用し、個々の臓器の状態やレシピエントの特性に応じた最適な保存プロトコルを確立する個別化医療への発展も期待されています。これらの技術革新は、臓器移植医療の未来を大きく変革し、より多くの命を救うことに貢献するでしょう。