PDXモデル市場規模・シェア分析:成長動向と予測 (2025年〜2030年)
患者由来異種移植モデル市場レポートは、モデルタイプ(マウスモデルなど)、腫瘍タイプ(消化器腫瘍など)、生着技術(異所性移植、同所性移植)、用途(創薬・前臨床試験など)、エンドユーザー(製薬・バイオテクノロジー企業など)、および地域別に分類されます。市場予測は、金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
患者由来異種移植(PDX)モデル市場は、2025年から2030年までの成長トレンドと予測に関する詳細な分析レポートです。この市場は、モデルタイプ(マウスモデルなど)、腫瘍タイプ(消化器腫瘍など)、移植技術(異所性移植および同所性移植)、アプリケーション(創薬および前臨床試験など)、エンドユーザー(製薬・バイオテクノロジー企業など)、および地域によってセグメント化されており、市場予測は米ドル建てで提供されています。
市場概要
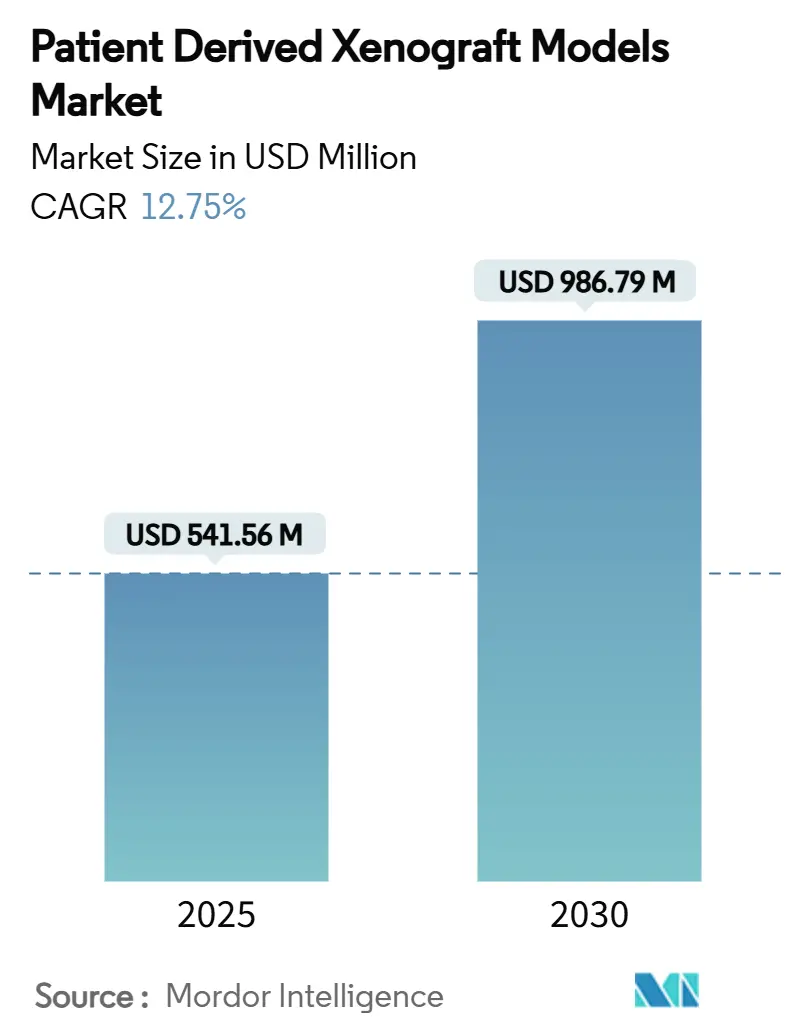
調査期間は2019年から2030年です。2025年の市場規模は5億4,156万米ドルと評価されており、2030年には9億8,679万米ドルに達すると予測されています。この期間における年平均成長率(CAGR)は12.75%と見込まれています。最も急速に成長する市場はアジア太平洋地域であり、最大の市場は北米です。市場の集中度は中程度とされています。
Mordor Intelligenceによる市場分析
PDXモデル市場の成長は、世界的な癌患者の増加、治験申請におけるPDXデータの認識を促す規制の近代化、そしてヒト化マウス、ゼブラフィッシュ、AI統合イメージングプラットフォームの着実な改善に起因しています。特に、6億5,000万米ドルのピアレビュー癌研究プログラムなど、連邦政府による腫瘍学研究への資金提供は、PDXモデル市場の拡大を強力に推進しています。
PDXモデルは、癌研究において重要なツールとして認識されており、個別化医療の進展に不可欠な役割を果たしています。これらのモデルは、患者の腫瘍組織を免疫不全マウスに移植することで作成され、元の腫瘍の生物学的特性、遺伝的特徴、および薬物反応性を維持します。これにより、研究者は様々な抗癌剤の有効性を評価し、特定の患者集団に対する最適な治療法を特定することが可能になります。
市場の主要なプレーヤーは、技術革新と戦略的提携を通じて競争力を高めています。例えば、新しいPDXモデルの作成技術の開発、ハイスループットスクリーニングプラットフォームの統合、およびAIや機械学習を活用したデータ解析ツールの導入が進められています。これらの進歩は、PDXモデルの精度と効率を向上させ、創薬プロセスにおけるその価値をさらに高めています。
しかし、PDXモデルの利用にはいくつかの課題も存在します。モデルの作成には時間とコストがかかり、成功率も常に高いわけではありません。また、マウスモデルとヒトの生理学的違いが、結果の臨床的関連性に影響を与える可能性も指摘されています。これらの課題に対処するため、研究者や企業は、より効率的で信頼性の高いPDXモデルの開発、および代替モデルシステムとの組み合わせによる補完的なアプローチを模索しています。
地域別に見ると、北米は癌研究への多額の投資、主要な製薬・バイオテクノロジー企業の存在、および高度な医療インフラにより、最大の市場シェアを占めています。一方、アジア太平洋地域は、癌患者数の増加、政府による研究開発への支援強化、および医療費の増加により、最も急速な成長が見込まれています。特に中国やインドなどの国々では、癌研究の需要が高まっており、PDXモデル市場の拡大に大きく貢献すると予測されています。
市場の成長をさらに促進する要因としては、個別化医療への関心の高まり、新規抗癌剤の開発競争の激化、およびバイオマーカー発見の進展が挙げられます。PDXモデルは、これらの分野において、薬剤の有効性予測、耐性メカニズムの解明、および新しい治療標的の特定に不可欠な情報を提供します。
結論として、PDXモデル市場は、癌研究と創薬におけるその独自の価値により、今後も堅調な成長を続けると予想されます。技術革新、戦略的パートナーシップ、および規制環境の進化が、この市場の将来を形作る主要なドライバーとなるでしょう。
このレポートは、患者由来異種移植(PDX)モデルの世界市場に関する詳細な分析を提供しています。PDXモデルとは、患者から採取された腫瘍組織を、免疫不全のマウスやラットなどの宿主動物に直接移植することで作製されるモデルであり、がん研究における新規治療薬の評価や個別化医療の推進に不可欠なツールとして注目されています。特に、ヒト化マウスやラットへの移植を通じて、がん細胞株に対する新規化合物の迅速な試験を可能にします。
市場規模は、2025年には5億4,156万米ドルに達し、2030年には9億8,679万米ドルに成長すると予測されており、予測期間中の年平均成長率(CAGR)は12.75%と高い伸びを示す見込みです。
市場の成長を牽引する主要な要因としては、世界的ながん罹患率の上昇と早期発見技術の進歩が挙げられます。また、製薬・バイオテクノロジー企業が研究開発(R&D)活動を契約研究機関(CROs)にアウトソーシングする傾向が強まっていること、新薬臨床試験開始届(IND)申請においてPDXデータが規制当局から好意的に受け入れられていることも、市場拡大に寄与しています。さらに、官民によるがん研究資金の増加、CRISPR技術を用いて遺伝子編集されたヒト化PDXモデルの登場、AIを活用した画像診断やデジタルバイオマーカー分析の統合といった技術革新も、市場の成長を後押ししています。
一方で、市場の成長を阻害する要因も存在します。3Dオルガノイドなどの代替モデルと比較して、PDXモデルは高コストであり、研究期間が長期にわたる点が課題です。また、厳格な動物福祉規制と倫理的精査、血液腫瘍や免疫細胞が豊富な腫瘍における生着成功率の低さも、普及の障壁となっています。さらに、インシリコモデルや臓器チップモデルといった競合技術の台頭も、市場に影響を与えています。
本レポートでは、市場を多角的にセグメント化し、詳細な分析を行っています。
モデルタイプ別では、ヌードマウス、NOD/SCIDマウス、NSGマウス、ヒト化マウスなどのマウスモデル、ラットモデル、ゼブラフィッシュモデル、鳥類CAMモデルが含まれます。特にゼブラフィッシュ異種移植モデルは、低コストと自動化されたハイスループットスクリーニングの利点から、CAGR 14.25%で最も速い成長が予測されています。
腫瘍タイプ別では、消化器腫瘍、婦人科腫瘍、呼吸器(胸部)腫瘍、中枢神経系腫瘍、血液悪性腫瘍、皮膚腫瘍(メラノーマ)、その他の固形腫瘍が対象となります。
生着技術別では、異所性(皮下)移植と同所性移植に分類されます。
アプリケーション別では、創薬・前臨床試験、バイオマーカー同定・コンパニオン診断、個別化腫瘍学(アバター試験)、トランスレーショナル・コークリニカル試験が分析対象です。
エンドユーザー別では、製薬・バイオテクノロジー企業、CRO、学術・研究機関、その他が含まれます。
地域別では、北米(米国、カナダ、メキシコ)、ヨーロッパ(ドイツ、英国、フランス、イタリア、スペインなど)、アジア太平洋(中国、日本、インド、韓国、オーストラリアなど)、中東・アフリカ(GCC、南アフリカなど)、南米(ブラジル、アルゼンチンなど)に分類されます。特にアジア太平洋地域は、費用対効果の高いCRO能力と拡大する製薬パイプラインを背景に、CAGR 13.27%で最高の成長率を記録すると予測されています。
規制環境の変化もPDX市場に影響を与えています。FDAおよびNIHの政策により、モノクローナル抗体の動物実験義務が段階的に廃止され、ヒト関連データが奨励されることで、新薬申請におけるPDXデータの重要性が高まっています。PDXモデルは、3Dオルガノイドなどの代替モデルと比較して高コストであるにもかかわらず、生体全体薬理学および転移挙動を保持しており、in vitroシステムでは対応できない用量反応および安全性研究に不可欠であるため、引き続き研究開発のプラットフォームとして選択されています。
競争環境については、市場集中度、市場シェア分析、および主要企業の詳細なプロファイルが提供されます。プロファイルには、Champions Oncology、Charles River Laboratories、Crown Bioscience、WuXi AppTec、Oncodesign、Hera BioLabs、EPO Berlin-Buch GmbH、Pharmatest Services Ltd、Urolead、Xentech、The Jackson Laboratory、Explora BioLabs、Inotiv Inc.、Models Genetix、GEMPharmatech、Envigo、Novotech、SOPHiA GENETICS、Shanghai LIDE Biotech、Reaction Biology Corp.などが含まれ、各社のグローバルおよび市場レベルの概要、主要セグメント、財務情報(入手可能な場合)、戦略情報、市場ランク/シェア、製品・サービス、最近の動向が網羅されています。
最後に、レポートは市場の機会と将来の展望として、未開拓分野と満たされていないニーズの評価も行い、今後の市場発展の方向性を示唆しています。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
- 4.2 市場の推進要因
- 4.2.1 がんの発生率の上昇と早期発見
- 4.2.2 CROへの製薬/バイオテクノロジーR&Dアウトソーシングの急増
- 4.2.3 IND申請におけるPDXデータの好意的な規制承認
- 4.2.4 官民のがん研究資金プールの増加
- 4.2.5 CRISPR編集されたヒト化PDXモデルの出現
- 4.2.6 AI対応イメージングとデジタルバイオマーカー分析の統合
- 4.3 市場の阻害要因
- 4.3.1 3Dオルガノイド代替品と比較した高コストと長い期間
- 4.3.2 厳格な動物福祉規制と倫理的精査
- 4.3.3 血液腫瘍および免疫細胞が豊富な腫瘍における生着成功率の低さ
- 4.3.4 インシリコおよび臓器チップモデルの競争的採用
- 4.4 ポーターの5つの力
- 4.4.1 新規参入の脅威
- 4.4.2 買い手の交渉力
- 4.4.3 供給者の交渉力
- 4.4.4 代替品の脅威
- 4.4.5 競争の激しさ
5. 市場規模と成長予測(金額、米ドル)
- 5.1 モデルタイプ別
- 5.1.1 マウスモデル
- 5.1.1.1 ヌード(無胸腺)
- 5.1.1.2 NOD/SCID
- 5.1.1.3 NSG
- 5.1.1.4 ヒト化マウス
- 5.1.2 ラットモデル
- 5.1.3 ゼブラフィッシュモデル
- 5.1.4 鳥類CAMモデル
- 5.2 腫瘍タイプ別
- 5.2.1 消化器腫瘍
- 5.2.2 婦人科腫瘍
- 5.2.3 呼吸器(胸部)腫瘍
- 5.2.4 中枢神経系腫瘍
- 5.2.5 血液悪性腫瘍
- 5.2.6 皮膚科(メラノーマ)腫瘍
- 5.2.7 その他の固形腫瘍
- 5.3 生着技術別
- 5.3.1 異所性(皮下)移植
- 5.3.2 同所性移植
- 5.4 用途別
- 5.4.1 創薬 & 前臨床試験
- 5.4.2 バイオマーカー同定 & コンパニオン診断
- 5.4.3 個別化腫瘍学(アバタートライアル)
- 5.4.4 トランスレーショナル & コークリニカル試験
- 5.5 エンドユーザー別
- 5.5.1 製薬 & バイオテクノロジー企業
- 5.5.2 受託研究機関(CRO)
- 5.5.3 学術 & 研究機関
- 5.5.4 その他
- 5.6 地域
- 5.6.1 北米
- 5.6.1.1 米国
- 5.6.1.2 カナダ
- 5.6.1.3 メキシコ
- 5.6.2 欧州
- 5.6.2.1 ドイツ
- 5.6.2.2 英国
- 5.6.2.3 フランス
- 5.6.2.4 イタリア
- 5.6.2.5 スペイン
- 5.6.2.6 その他の欧州
- 5.6.3 アジア太平洋
- 5.6.3.1 中国
- 5.6.3.2 日本
- 5.6.3.3 インド
- 5.6.3.4 韓国
- 5.6.3.5 オーストラリア
- 5.6.3.6 その他のアジア太平洋
- 5.6.4 中東およびアフリカ
- 5.6.4.1 GCC
- 5.6.4.2 南アフリカ
- 5.6.4.3 その他の中東およびアフリカ
- 5.6.5 南米
- 5.6.5.1 ブラジル
- 5.6.5.2 アルゼンチン
- 5.6.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
- 6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、コアセグメント、利用可能な財務情報、戦略情報、主要企業の市場ランク/シェア、製品&サービス、および最近の動向を含む)
- 6.3.1 チャンピオンズ・オンコロジー
- 6.3.2 チャールズ・リバー・ラボラトリーズ
- 6.3.3 クラウン・バイオサイエンス
- 6.3.4 ウーシー・アプテック
- 6.3.5 オンコデザイン
- 6.3.6 ヘラ・バイオラボ
- 6.3.7 EPO ベルリン・ブーフ GmbH
- 6.3.8 ファーマテスト・サービス株式会社
- 6.3.9 ウロリード
- 6.3.10 ゼンテック
- 6.3.11 ジャクソン研究所
- 6.3.12 エクスプローラ・バイオラボ
- 6.3.13 イノティブ・インク
- 6.3.14 モデルズ・ジェネティクス
- 6.3.15 GEMファーマテック
- 6.3.16 エンビゴ
- 6.3.17 ノボテック
- 6.3.18 ソフィア・ジェネティクス
- 6.3.19 上海LIDEバイオテック
- 6.3.20 リアクション・バイオロジー・コーポレーション
7. 市場機会と将来展望
*** 本調査レポートに関するお問い合わせ ***

PDXモデルは、がん研究および創薬開発において極めて重要な役割を果たす前臨床モデルの一つでございます。PDXとは「Patient-Derived Xenograft」の略であり、患者様から採取されたがん組織を、免疫不全マウスに直接移植して作製される異種移植モデルを指します。このモデルの最大の特長は、患者様のがん組織が持つ遺伝的特性、組織学的特徴、そして微小環境を可能な限り維持した状態で、生体内でがんの挙動を再現できる点にございます。従来のがん細胞株を用いた異種移植モデルと比較して、PDXモデルはがんの不均一性や薬剤応答性をより忠実に反映するため、臨床に近い予測性を持つと広く認識されております。これにより、新規抗がん剤の有効性評価、薬剤耐性メカニズムの解明、個別化医療の推進など、多岐にわたる研究分野で活用が進められております。
PDXモデルにはいくつかの種類と作製方法がございます。まず、移植部位によって「皮下移植モデル」と「同所性移植モデル」に大別されます。皮下移植モデルは、マウスの皮下にがん組織を移植するもので、作製が比較的容易であり、腫瘍の増殖を視覚的に観察しやすいという利点がございます。一方、同所性移植モデルは、がんの原発部位(例えば、肺がんの場合は肺、大腸がんの場合は大腸)にがん組織を移植するもので、がんの微小環境や転移能をより忠実に再現できるため、生理学的により関連性の高いモデルとされております。また、移植されるがん組織の種類も、原発巣由来のものから転移巣由来のものまで様々であり、がんの進行度に応じたモデル作製が可能でございます。さらに、PDXモデルはマウス内で継代(パス)されることがありますが、継代回数が少ないほど、元の患者様のがんの特性を保持していると考えられております。最近では、がん組織だけでなく、患者様の免疫細胞を同時に移植することで、免疫チェックポイント阻害剤などの免疫療法薬の効果を評価できる「ヒト化免疫系PDXモデル」の開発も進められております。
PDXモデルの用途は非常に広範にわたります。最も主要な用途は、新規抗がん剤の「前臨床有効性評価」でございます。開発中の薬剤が、特定のPDXモデルに対してどの程度の効果を示すかを評価することで、臨床試験に進むべき薬剤候補の選定や、最適な投与量・投与スケジュールの検討に役立てられます。また、薬剤応答性に関連する「バイオマーカーの探索」にも利用されます。特定の遺伝子変異やタンパク質の発現パターンを持つPDXモデルが、特定の薬剤に感受性を示すかどうかを解析することで、患者層別化のためのバイオマーカー候補を特定することが可能となります。さらに、「薬剤耐性メカニズムの解明」においても重要なツールでございます。薬剤投与後に耐性を獲得したPDXモデルを解析することで、耐性に関わる遺伝子変異やシグナル経路の変化を特定し、新たな治療戦略の開発に繋げることができます。個別化医療の分野では、患者様一人ひとりのがん組織からPDXモデルを作製し、複数の抗がん剤や併用療法を事前にスクリーニングすることで、その患者様にとって最適な治療法を選択する「アバターモデル」としての活用も期待されております。
PDXモデルの研究・開発には、様々な関連技術が不可欠でございます。まず、PDXモデルの基盤となるのは、免疫不全マウスでございます。特に、T細胞、B細胞、NK細胞などの免疫細胞が欠損しているNOD/SCIDマウスやNSGマウス(NOD/SCID/IL2Rγnullマウス)が広く用いられております。これらのマウスは、ヒトのがん組織を拒絶することなく生着・増殖させる能力が高いため、PDXモデル作製に必須でございます。次に、PDXモデルの特性評価には「ゲノム解析技術」が欠かせません。次世代シーケンサー(NGS)を用いた全エクソームシーケンシング(WES)やRNAシーケンシング(RNA-seq)により、患者様のがん組織とPDXモデルの遺伝子変異、遺伝子発現パターンを比較し、モデルが元の腫瘍の特性を維持していることを確認します。また、プロテオミクスやメタボロミクスといった「オミクス解析」も、より詳細な分子レベルでの特性評価に貢献します。さらに、腫瘍の増殖や転移を非侵襲的にモニタリングするために、PET、MRI、バイオイメージングなどの「生体イメージング技術」が活用されます。近年では、PDXモデルと並行して、患者様のがん組織から作製される「オルガノイド」や「スフェロイド」といった3次元培養モデルも注目されており、これらはハイスループットスクリーニングに適しているため、PDXモデルと組み合わせることで、より効率的な薬剤探索が可能となります。
PDXモデルの市場背景は、がん治療薬開発における高いアンメットニーズと、既存の前臨床モデルの限界を背景に、急速に拡大しております。製薬企業やバイオテクノロジー企業は、臨床試験での高い失敗率を改善するため、より予測性の高い前臨床モデルを求めており、PDXモデルはその有力な選択肢として認識されております。このため、PDXモデルの作製、維持、および薬剤評価サービスを提供する「CRO(医薬品開発業務受託機関)」が多数存在し、市場を牽引しております。主要なプレイヤーとしては、Charles River Laboratories、Crown Bioscience、WuXi AppTec、Champions Oncologyなどが挙げられます。これらの企業は、多様ながん種に対応する大規模なPDXライブラリを構築し、顧客のニーズに応じたサービスを提供しております。一方で、PDXモデルの作製には、時間とコストがかかること、また、動物愛護の観点からの倫理的配慮が必要であること、さらに、モデルの標準化や品質管理の課題も存在します。しかし、その高い臨床予測性から、今後も市場規模は拡大し続けると予測されております。
PDXモデルの将来展望は、技術革新と研究の深化により、さらなる進化が期待されております。最も注目されるのは、「ヒト化免疫系PDXモデル」のさらなる発展でございます。既存のPDXモデルは免疫不全マウスを使用するため、免疫細胞とがん細胞の相互作用を十分に評価できませんでしたが、ヒトの免疫システムを再構築したマウスを用いることで、免疫チェックポイント阻害剤やCAR-T細胞療法といった免疫療法の効果をより正確に評価できるようになります。これにより、免疫療法薬の開発が大きく加速すると考えられます。また、人工知能(AI)や機械学習との融合も進むでしょう。PDXモデルから得られる膨大なゲノムデータ、薬剤応答データ、病理画像データなどをAIで解析することで、新たなバイオマーカーの発見、薬剤応答性の予測精度向上、さらには最適な治療戦略の提案が可能になるかもしれません。さらに、オルガノイドなどのin vitroモデルとの連携も強化されると予想されます。オルガノイドで初期のハイスループットスクリーニングを行い、有望な候補をPDXモデルで検証するという、より効率的かつ段階的な薬剤開発パイプラインが確立される可能性があります。希少がんや小児がんなど、これまでモデル作製が困難であったがん種への適用拡大も期待されており、個別化医療の実現に向けた重要な基盤技術として、その価値は一層高まっていくことでしょう。倫理的な側面やコスト効率の改善も継続的な課題として取り組まれ、よりアクセスしやすく、標準化されたモデルとしての普及が進むことが期待されます。