レッドバイオテクノロジー市場規模・シェア分析 – 成長動向と予測 (2026年~2031年)
レッドバイオテクノロジー市場レポートは、製品(ワクチン[mRNAワクチン、ウイルスベクターワクチンなど]、治療薬[モノクローナル抗体、組換えタンパク質など]、診断・研究ツール[シーケンシング試薬・キットなど])、エンドユーザー(バイオ医薬品企業など)、および地域(北米、欧州など)別に分類されます。市場予測は、金額(米ドル)で示されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
レッドバイオテクノロジー市場の概要
本レポートは、レッドバイオテクノロジー市場の規模、見通し、および業界レポートを2026年から2031年までの期間で提供するものです。市場は、製品(ワクチン、治療薬、診断・研究ツール)、エンドユーザー(バイオ医薬品企業など)、および地域(北米、欧州など)によってセグメント化されており、市場予測は金額(米ドル)で示されています。
市場概要
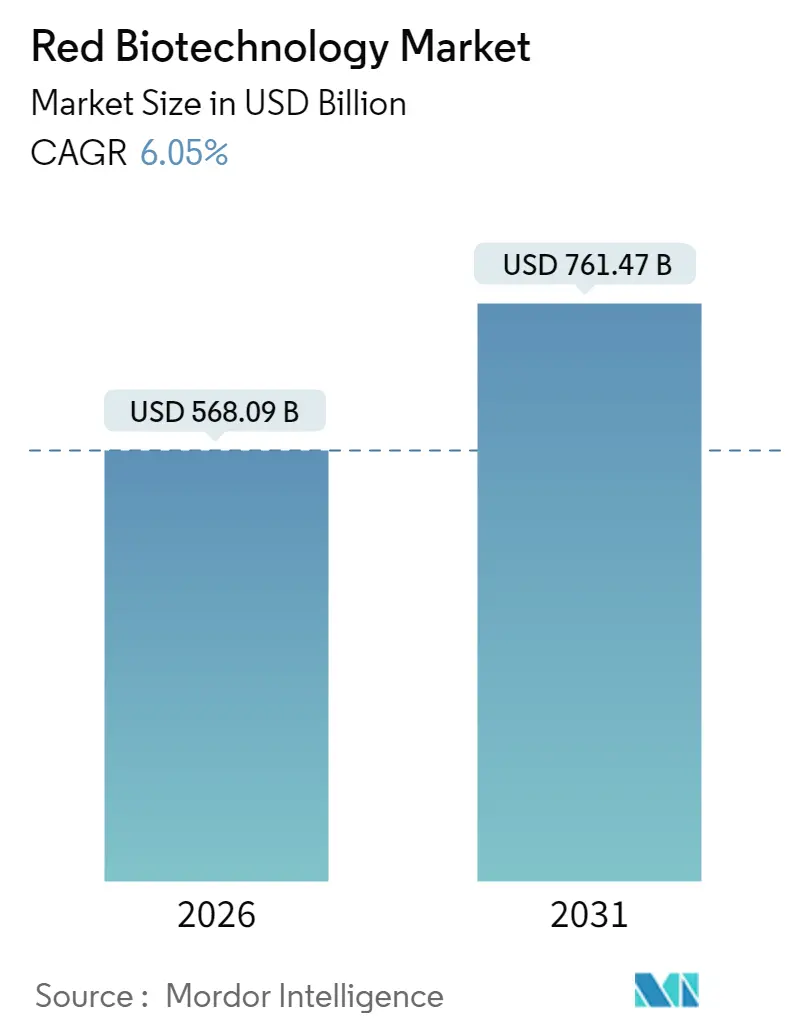
レッドバイオテクノロジー市場は、2025年に5,356.8億米ドル、2026年には5,680.9億米ドルと評価され、2031年までに7,614.7億米ドルに達すると予測されており、予測期間(2026年~2031年)における年平均成長率(CAGR)は6.05%です。アジア太平洋地域が最も急速に成長する市場であり、北米が最大の市場となっています。市場の集中度は中程度です。
この成長は、パンデミック対応のワクチン生産から、細胞・遺伝子治療、次世代モノクローナル抗体、精密診断を含む多様なパイプラインへの移行に支えられています。2024年にFDAが24件の生物学的製剤ライセンスを承認したことに見られるように、迅速な規制審査が勢いを後押ししています。また、2027年までに795億米ドルが割り当てられた公衆衛生緊急医療対策企業(PHEMCE)による政府支出は、開発と製造の両方における国内能力を強化しています。業界側では、メルク社がノースカロライナ州に10億米ドルを投じて建設するワクチン施設のような大規模な設備投資が、パンデミック対応と日常的な商業生産の両方に対応できる強靭な能力を追加しています。これらの要因が相まって、高複雑性バイオ医薬品のスケールアップに予測可能な環境を作り出し、革新的な資産の臨床導入期間を短縮するベンチャー投資や官民パートナーシップを促進しています。
主要なレポートのポイント
* 製品カテゴリー別:治療薬セグメントが2025年にレッドバイオテクノロジー市場シェアの54.12%を占め、2031年までに6.63%のCAGRで拡大すると予測されています。
* エンドユーザー別:バイオ医薬品企業が2025年に市場規模の44.25%を占めましたが、学術・研究機関が2031年までに7.05%と最も高いCAGRを記録すると予測されています。
* 地域別:北米が2025年に市場規模の38.72%を占め、アジア太平洋地域が同期間に6.94%のCAGRで最も急速に成長しています。
グローバルレッドバイオテクノロジー市場のトレンドと洞察
市場の推進要因
* 慢性疾患および希少疾患の発生率と有病率の増加(CAGRへの影響:+1.2%):2024年には8つの新規細胞・遺伝子治療がFDAの審査を通過し、未充足のニーズ領域が科学的ブレークスルーを商業的資産へと転換させていることを示しています。腫瘍学は承認の34%を占め、引き続き優位を保っています。日本の急速な高齢化人口管理の課題を反映し、次世代モノクローナル抗体や遺伝子治療への政策的優先順位付けが行われています。希少疾患パイプラインは、2024年の遺伝子治療承認の88%がオーファンドラッグ指定を受けたように、オーファンドラッグインセンティブの恩恵を受けています。FDAの希少疾患イノベーションハブとSTARTパイロットプログラムは、開発期間を短縮し、かつて商業的に魅力的でなかったニッチな疾患を企業がターゲットにするよう奨励しています。
* 医療資金の拡大と官民パートナーシップ(CAGRへの影響:+0.9%):2023年から2027年のPHEMCE割り当てでは、対策の研究開発と国内製造のために795億米ドルが確保され、以前の計画サイクルから155億米ドルの増加となりました。BARDAの20億米ドルのBioMaPコンソーシアムは、抗体からmRNAワクチンへと数ヶ月で転換できる柔軟な施設に共同投資することで、この支援を拡大しています。カナダのモントリオールにあるバイオロジクス製造センターは、ウイルスベクターおよびタンパク質サブユニットワクチンの製造能力を強化しています。
このレポートは、レッドバイオテクノロジー市場に関する包括的な分析を提供しています。レッドバイオテクノロジーは、生きた細胞、遺伝子操作された生物、またはその派生物を利用してヒトの疾患を治療、検出、予防する治療用バイオ医薬品、予防ワクチン、細胞・遺伝子ベース医薬品、分子診断薬から生み出される世界的な総収益と定義されています。工業用酵素、農業バイオ技術投入物、患者ケアに使用されない生体材料は調査範囲から除外されています。
調査方法
本調査は、厳格な一次調査と二次調査に基づいて実施されています。一次調査では、バイオ医薬品企業の製造責任者、契約開発組織(CDO)の調達担当者、CAR-T治験の腫瘍学者、支払者アドバイザーなど、主要な業界関係者へのインタビューを通じて、平均販売価格、規制承認後の普及曲線、地域ごとの償還上限などの重要なデータを検証しました。二次調査では、米国食品医薬品局(FDA)の生物製剤ライセンス申請データベース、欧州医薬品庁(EMA)の承認アーカイブ、世界保健機関(WHO)のワクチン調達ダッシュボードといった標準的な情報源に加え、国連貿易統計、臨床試験登録、査読付きジャーナル、企業報告書、有料プラットフォーム(D&B Hoovers、Dow Jones Factivaなど)を活用し、広範なデータ収集と相互検証を行いました。
市場規模の算出と予測は、バイオ医薬品の売上、ワクチン出荷量、遺伝子検査量から需要プールを再構築するトップダウンアプローチを採用し、生産能力や平均販売価格(ASP)との比較を通じて妥当性を確認しています。研究開発費、承認適応症数、バイオリアクター稼働率、特許切れ、有病率対治療患者比率、国民予防接種率などの多変量回帰分析により、2030年までの市場価値を予測しています。データは毎年更新され、重要な市場イベントが発生した場合には中間更新も行われます。
市場の状況
市場は複数の要因によって推進されています。慢性疾患および希少疾患の発生率と有病率の増加、医療資金の拡大と官民パートナーシップの進展、個別化医療の採用とコンパニオン診断薬の普及が挙げられます。また、mRNAプラットフォームの波及効果による新規バイオ医薬品の迅速な開発、AI駆動による初期段階のバイオ医薬品設計のリスク低減、政府主導のパンデミック対策プログラムによるグローバルなワクチン製造能力の拡大も市場成長を後押ししています。
一方で、市場にはいくつかの抑制要因も存在します。高いバイオ製造コストとコールドチェーンコスト、複雑で変化の激しいグローバルなバイオ医薬品規制、重要な原材料のサプライチェーンの脆弱性、次世代遺伝子治療における免疫原性リスクなどが挙げられます。
このレポートでは、サプライチェーン分析、規制状況、技術的展望、そしてポーターのファイブフォース分析(サプライヤーの交渉力、買い手の交渉力、新規参入の脅威、代替品の脅威、競争の激しさ)を通じて、市場の包括的な理解を提供しています。
市場規模と成長予測
市場規模と成長予測は、製品、エンドユーザー、地域別に詳細に分析されています。
製品別では、ワクチン(mRNAワクチン、ウイルスベクターワクチン、組換えタンパク質ワクチンなど)、治療薬(モノクローナル抗体、組換えタンパク質、遺伝子治療、細胞治療、RNA治療薬)、診断・研究ツール(シーケンシング試薬・キット、コンパニオン診断アッセイ、ポイントオブケア分子検査)に分類されています。
エンドユーザー別では、バイオ医薬品企業、契約製造組織(CMO)、契約研究組織(CRO)、学術・研究機関、病院・専門クリニックが主要なセグメントとして挙げられています。
地域別では、北米(米国、カナダ、メキシコ)、欧州(ドイツ、英国、フランスなど)、アジア太平洋(中国、インド、日本など)、中東・アフリカ、南米といった主要地域とその主要国が分析対象となっています。
競合状況
競合状況のセクションでは、市場集中度、競合ベンチマーキング、市場シェア分析が提供されています。Amgen Inc.、AstraZeneca PLC、BioNTech SE、Bristol Myers Squibb、F. Hoffmann-La Roche Ltd、Johnson & Johnson、Lonza Group AG、Moderna Inc.、Novartis AG、Pfizer Inc.、Sanofi、Takeda Pharmaceutical、Thermo Fisher Scientificなど、主要な21社の企業プロファイルが含まれており、各社の概要、主要セグメント、財務情報、戦略的情報、市場ランク/シェア、製品・サービス、最近の動向が詳述されています。
市場機会と将来展望
レポートは、未開拓領域と満たされていないニーズの評価を通じて、市場の機会と将来展望を提示しています。主要な質問への回答から、以下の重要な洞察が得られます。
* 治療モダリティの動向: 細胞・遺伝子治療は、FDAの希少疾患イノベーションハブなどのプログラムにより迅速な審査を受け、ニッチで影響力の大きい治療法として承認が加速しています。
* AIの役割: ディープラーニングモデルは、タンパク質のフォールディングや免疫原性ホットスポットを短時間で予測し、研究者が迅速に設計を反復し、初期段階の失敗リスクを低減するのに貢献しています。
* CMOとの提携の利点: 契約製造組織(CMO)は、モジュール式で使い捨ての施設を提供することで、多額の設備投資なしに生産規模を拡大することを可能にし、迅速な商業化とパンデミック時の柔軟な増産能力を実現しています。
* グローバル規制の影響: 2025年以降のEUと米国の規制の相違は、企業に申請順序の検討、地域特有のブリッジング試験の実施、科学的助言費用の増加を予算化するよう促しています。
* 個別化医療と診断ワークフロー: コンパニオン診断薬は、ポイントオブケアに近づき、迅速なゲノムアッセイを統合することで、臨床医が初診時に標的治療を選択できるよう支援しています。
* コールドチェーンコスト削減技術: トランス増幅mRNAワクチンや次世代安定化賦形剤は、標準的な冷蔵での製品保存期間を延長し、超低温貯蔵ネットワークへの依存度を低減することで、コールドチェーンの物流コスト削減に貢献しています。
このレポートは、レッドバイオテクノロジー市場における意思決定者が、明確な変数と再現可能な手順に基づいて、バランスの取れたベースラインを把握できるよう、信頼性の高い情報を提供しています。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
- 4.2 市場の推進要因
- 4.2.1 慢性疾患および希少疾患の発生率と有病率の増加
- 4.2.2 医療資金の拡大と官民パートナーシップ
- 4.2.3 個別化医療の採用とコンパニオン診断薬の普及
- 4.2.4 mRNAプラットフォームの波及による新規バイオ医薬品の迅速化
- 4.2.5 AIを活用した初期段階のバイオ医薬品設計のリスク低減
- 4.2.6 政府主導のパンデミック対策プログラムによる世界的なワクチン製造能力の拡大
- 4.3 市場の阻害要因
- 4.3.1 高いバイオ製造およびコールドチェーンコスト
- 4.3.2 複雑で変化する世界のバイオ医薬品規制
- 4.3.3 重要な原材料のサプライチェーンの脆弱性
- 4.3.4 次世代遺伝子治療における免疫原性リスク
- 4.4 サプライチェーン分析
- 4.5 規制環境
- 4.6 技術的展望
- 4.7 ポーターの5つの力分析
- 4.7.1 供給者の交渉力
- 4.7.2 買い手/消費者の交渉力
- 4.7.3 新規参入の脅威
- 4.7.4 代替品の脅威
- 4.7.5 競争の激しさ
5. 市場規模と成長予測(金額)
- 5.1 製品別
- 5.1.1 ワクチン
- 5.1.1.1 mRNAワクチン
- 5.1.1.2 ウイルスベクターワクチン
- 5.1.1.3 組換えタンパク質ワクチン
- 5.1.1.4 結合型&サブユニットワクチン
- 5.1.1.5 生弱毒化&不活化ワクチン
- 5.1.2 治療薬
- 5.1.2.1 モノクローナル抗体
- 5.1.2.2 組換えタンパク質
- 5.1.2.3 遺伝子治療
- 5.1.2.4 細胞治療
- 5.1.2.5 RNA治療薬
- 5.1.3 診断薬&研究ツール
- 5.1.3.1 シーケンシング試薬&キット
- 5.1.3.2 コンパニオン診断アッセイ
- 5.1.3.3 ポイントオブケア分子検査
- 5.2 エンドユーザー別
- 5.2.1 バイオ医薬品企業
- 5.2.2 医薬品受託製造機関(CMO)
- 5.2.3 医薬品受託研究機関(CRO)
- 5.2.4 学術機関&研究機関
- 5.2.5 病院&専門クリニック
- 5.3 地域別
- 5.3.1 北米
- 5.3.1.1 米国
- 5.3.1.2 カナダ
- 5.3.1.3 メキシコ
- 5.3.2 欧州
- 5.3.2.1 ドイツ
- 5.3.2.2 英国
- 5.3.2.3 フランス
- 5.3.2.4 イタリア
- 5.3.2.5 スペイン
- 5.3.2.6 その他の欧州
- 5.3.3 アジア太平洋
- 5.3.3.1 中国
- 5.3.3.2 インド
- 5.3.3.3 日本
- 5.3.3.4 オーストラリア
- 5.3.3.5 韓国
- 5.3.3.6 その他のアジア太平洋
- 5.3.4 中東およびアフリカ
- 5.3.4.1 GCC
- 5.3.4.2 南アフリカ
- 5.3.4.3 その他の中東およびアフリカ
- 5.3.5 南米
- 5.3.5.1 ブラジル
- 5.3.5.2 アルゼンチン
- 5.3.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 競合ベンチマーク
- 6.3 市場シェア分析
- 6.4 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要セグメント、利用可能な財務情報、戦略情報、主要企業の市場ランク/シェア、製品&サービス、および最近の動向を含む)
- 6.4.1 Amgen Inc.
- 6.4.2 AstraZeneca PLC
- 6.4.3 Biogen Inc.
- 6.4.4 BioNTech SE
- 6.4.5 Bristol Myers Squibb
- 6.4.6 CSL Limited
- 6.4.7 F. Hoffmann-La Roche Ltd
- 6.4.8 Gilead Sciences Inc.
- 6.4.9 Illumina Inc.
- 6.4.10 Johnson & Johnson (Janssen)
- 6.4.11 Lonza Group AG
- 6.4.12 Merck & Co., Inc.
- 6.4.13 Moderna Inc.
- 6.4.14 Novartis AG
- 6.4.15 Pfizer Inc.
- 6.4.16 Regeneron Pharmaceuticals
- 6.4.17 Sanofi
- 6.4.18 Sarepta Therapeutics
- 6.4.19 Takeda Pharmaceutical
- 6.4.20 Thermo Fisher Scientific
- 6.4.21 Vertex Pharmaceuticals
7. 市場機会&将来展望
*** 本調査レポートに関するお問い合わせ ***

レッドバイオテクノロジーは、医療・医薬品分野におけるバイオテクノロジーの応用を指します。人間の健康増進、病気の予防、診断、治療を目的とし、生命科学の知見と技術を駆使して革新的な医薬品や医療技術を生み出す学際的な分野です。
主な種類としては、まず創薬・医薬品開発が挙げられます。遺伝子組換え技術を用いた組換えタンパク質医薬品、特定の標的を狙うモノクローナル抗体医薬品、そして近年注目を集める遺伝子治療薬や細胞治療薬などが含まれます。これらは、従来の治療法では困難であった疾患に画期的な治療法を提供します。次に、診断薬・診断技術の開発も重要な柱です。PCR法、ELISA法、DNAマイクロアレイ、次世代シーケンシング(NGS)などの技術は、感染症の早期診断、がんのスクリーニング、遺伝性疾患の特定、個別化医療におけるバイオマーカー検出にも不可欠です。再生医療もレッドバイオテクノロジーの主要な領域であり、iPS細胞やES細胞、間葉系幹細胞などの幹細胞を用いた組織や臓器の修復・再生を目指します。また、遺伝子治療は、疾患の原因となる遺伝子の異常を直接修正したり、治療効果を持つ遺伝子を導入したりすることで、根本的な治療を目指します。さらに、感染症に対するワクチン開発、特にmRNAワクチンなどの新しいアプローチも含まれます。
これらの技術は多岐にわたる疾患の治療に応用されています。例えば、がん治療においては、免疫チェックポイント阻害剤やCAR-T細胞療法といった免疫療法が、従来の治療法で効果が限定的だった患者に新たな希望をもたらします。遺伝性疾患に対しては、遺伝子治療が脊髄性筋萎縮症や血友病などの治療に実用化されつつあります。感染症対策では、新型コロナウイルス感染症に対するmRNAワクチンの迅速な開発と普及が、レッドバイオテクノロジーの力を世界に示しました。自己免疫疾患や神経変性疾患、希少疾患に対しても、生物学的製剤や幹細胞治療、遺伝子治療の研究開発が進められており、未だ治療法が確立されていない多くの疾患の解決策として期待されます。予防医療の観点からは、遺伝子情報に基づく疾患リスクの評価や、早期診断技術の向上により、病気の発症予防や早期介入を可能にしつつあります。
レッドバイオテクノロジーを支える関連技術も日々進化しています。遺伝子組換え技術は、治療用タンパク質の生産やモデル生物の作製に不可欠な基盤技術です。細胞培養技術は、細胞治療やワクチン製造、抗体医薬品の生産において中心的な役割を担います。ゲノム編集技術、特にCRISPR-Cas9システムは、遺伝子の特定部位を正確に改変することを可能にし、遺伝子治療や疾患モデル研究に革命をもたらしました。次世代シーケンシングは、ゲノム全体の情報を高速かつ低コストで解析することを可能にし、診断や個別化医療の発展を加速させています。また、膨大な生命情報を解析するためのバイオインフォマティクス、特定の抗体を設計・改良する抗体工学、薬剤送達システムに応用されるナノテクノロジー、そして近年では創薬プロセスや診断アルゴリズムの最適化に貢献するAI(人工知能)や機械学習も、レッドバイオテクノロジーの発展に不可欠な要素です。
市場背景としては、世界的な高齢化の進展に伴う医療ニーズの増大が挙げられます。慢性疾患や生活習慣病の増加、そして未だ治療法が確立されていない難病の存在が、革新的な医薬品や治療法の開発を強く求めています。また、ゲノム科学や分子生物学の急速な進歩が、新たな治療標的の発見や技術革新を後押ししています。各国政府も、再生医療や希少疾患治療薬の開発に対する規制緩和や研究開発支援を積極的に行っており、これが市場成長を促進する要因です。さらに、新型コロナウイルス感染症のパンデミックは、感染症対策としてのワクチンや治療薬開発の重要性を再認識させ、この分野への投資と関心を一層高めました。個別化医療へのシフトも顕著であり、患者一人ひとりの遺伝子情報や病態に合わせた精密な医療の実現が、市場を牽引しています。
将来展望としては、個別化医療のさらなる深化が期待されます。ゲノム情報だけでなく、プロテオーム、メタボロームなどのオミクス情報を統合的に解析し、より精密な診断と治療選択を可能にするでしょう。遺伝子治療や細胞治療は、適用疾患が拡大し、より多くの患者に利用されるようになることが見込まれますが、そのコスト削減とアクセス性の向上が課題です。AIと機械学習は、創薬のリードタイム短縮、臨床試験の効率化、疾患予測、個別化された治療計画の立案において、ますます重要な役割を果たすでしょう。予防医療の分野では、遺伝子スクリーニングやバイオマーカーの活用により、疾患の発症前段階での介入が一般化する可能性があります。一方で、ゲノム編集技術の倫理的側面、遺伝子情報のプライバシー保護、高額な先進医療への公平なアクセスといった社会的な課題も、今後さらに議論されるべき重要なテーマです。レッドバイオテクノロジーは、人類の健康と福祉に貢献する可能性を秘めている一方で、これらの課題に対する慎重な検討と社会的な合意形成が不可欠です。