制限酵素市場:市場規模・シェア分析 – 成長動向と予測 (2025年~2030年)
制限酵素市場レポートは、業界をタイプ別(タイプI、タイプII、タイプIII、その他のタイプ)、用途別(遺伝子工学、DNAマッピング、遺伝子シーケンシング、その他の用途)、エンドユーザー別(製薬・バイオテクノロジー企業、学術研究機関、その他のエンドユーザー)、および地域別(北米、ヨーロッパ、アジア太平洋、その他の地域)に分類しています。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
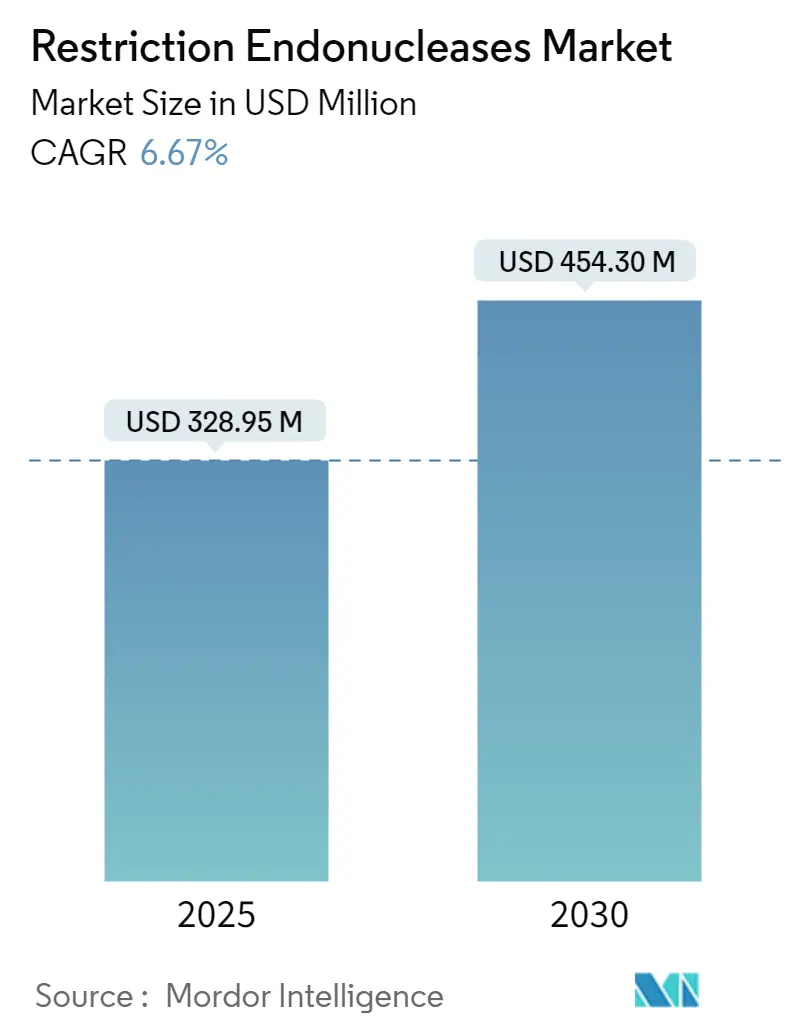
制限酵素市場は、2025年に3億2895万米ドルと推定され、2030年には4億5430万米ドルに達すると予測されており、予測期間(2025年~2030年)中の年平均成長率(CAGR)は6.67%です。この市場は、様々な用途での制限酵素の使用増加と、バイオテクノロジー企業および製薬企業による研究開発費の増加が主な推進要因となっています。
市場の概要と推進要因
制限酵素は、遺伝子工学や遺伝子配列決定といった研究や治療目的の様々なアプリケーションで広く利用されており、その需要が高まっています。例えば、2023年9月にロシア科学アカデミーシベリア支部化学生物学・基礎医学研究所が発表した研究では、現代の分子生物学において制限酵素が極めて重要なツールであり、DNA断片を得るための手順として日常的に用いられていることが強調されています。
さらに、ゲノミクス分野における研究とイノベーションに対するバイオテクノロジー企業、製薬企業、および政府機関からの資金提供と投資の増加も市場成長を促進しています。米国国立衛生研究所(NIH)の国立ヒトゲノム研究所(NHGRI)の2022年報告書によると、2022会計年度の米国大統領予算要求は6億3300万米ドルであり、2021会計年度の制定水準と比較して1700万米ドルの増加となりました。この増加は、ゲノミクスにおけるすべてのプログラム分野および基礎、疫学、臨床研究に分配されています。NHGRIによるゲノミクス研究への多額の投資は、研究中に大量の制限酵素が利用されることを意味し、予測期間中の市場成長を促進すると予想されます。
また、2022年9月にはWhiteLab GenomicsがAIを活用したゲノム療法プラットフォームのために1000万米ドルを調達しました。この投資は、遺伝子療法の創出に革命をもたらすことを目的としており、クライアントが標的ベクターやペイロードを迅速に開発し、ゲノムベースの療法をより速いペースで市場に投入できるよう支援しています。このような資金提供と投資は、制限酵素を用いた遺伝子工学、DNAマッピング、遺伝子配列決定の分野における拡大と革新の機会を創出すると推定され、市場成長をさらに推進しています。
これらの要因により、制限酵素市場は分析期間中に成長を遂げると予測されます。しかし、制限酵素の生産コストが高いことが、予測期間中の市場成長を妨げる可能性があります。
主要な市場トレンドと洞察
1. 遺伝子工学が大きな市場シェアを占める見込み
遺伝子工学は、いくつかの方法と分子生物学技術を用いてゲノムのDNA配列を変更する実践です。制限酵素、DNAシーケンシング、DNAクローニングなどの分子生物学ツールは、科学者が細胞や動物の染色体DNAを変更する実験に迅速に移行するのに役立ちます。がん、嚢胞性線維症、血友病、エイズなどの疾患に対する様々な遺伝子治療を開発するためのバイオテクノロジー企業や製薬企業による研究開発への投資増加が、このセグメントの成長を推進しています。
2022年6月に発表されたEngineering Biology Leadership Councilの報告書によると、英国政府はエンジニアリングバイオロジー(EB)の変革的製品の基礎研究と早期実用化を強力に支援しています。同報告書は、今後5年から10年以内にEBが化学・材料(産業バイオテクノロジー)、食品・農業、健康関連開発の各分野に革命をもたらす可能性を秘めていると述べています。2030年から2040年までに、EBは年間2兆から4兆米ドルの直接的な世界経済効果をもたらすと予測されています。このような政府からの支援増加は、予測期間中のセグメント成長を促進すると予想されます。
さらに、遺伝子工学分野における政府機関による投資と資金提供の増加も市場成長を促進すると予想されます。例えば、2023年12月にはTomeが、マサチューセッツ工科大学(MIT)からライセンス供与されたプログラマブルゲノム統合(PGI)技術の開発と商業化を支援するために、Andreessen Horowitz Bio + Health、ARCH Venture Partners、GV、Longwood Fund、Polaris Partners、Bruker Corporation、FUJIFILM Corporation、Alexandria Venture Investmentsなどの投資家からシリーズAおよびBで2億1300万米ドルを調達しました。このような資金提供と、遺伝性疾患の治療法開発のために制限酵素を利用する遺伝子工学における研究イニシアチブの増加は、予測期間中のセグメント成長を促進すると推定されます。
2. 北米が大きな市場シェアを占める見込み
北米は、主要企業の存在、高額な投資、地域のバイオテクノロジーおよび製薬分野における研究開発プログラムの増加などの要因により、制限酵素市場で大きなシェアを占めると予想されます。さらに、政府の有益なイニシアチブや研究パートナーシップの増加も市場成長を促進する要因です。
制限酵素は、市場成長に貢献する遺伝学研究などの科学研究にとって有用なツールです。例えば、NIHの「様々な研究、病状、疾患カテゴリー(RCDC)への資金推定、2022年更新」によると、米国の遺伝学プロジェクトへの研究費は、2020年に105億4400万米ドル、2021年に110億1000万米ドル、2022年には114億8000万米ドルと推定されています。この地域における遺伝学研究プロジェクトへの支出増加は、遺伝性疾患治療のための制限酵素の利用を促進すると予想されます。
カナダでは、バイオテクノロジー研究への政府投資が増加しています。2022年3月、イノベーション・科学・産業大臣は、カナダのライフサイエンス分野における企業のイノベーションとトレーニング活動を推進するために、adware BioInnovationsに9200万米ドルを投資しました。この投資は、商業的に有望な健康研究を革新的な新しい治療法に転換し、カナダのバイオテクノロジー企業の成長を促進するのに役立ちます。このような政府による多額の投資は、制限酵素の機会をさらに創出し、市場成長を促進すると予想されます。
また、2022年3月にはColossalが遺伝子工学と絶滅種再生技術を進めるために6000万米ドルのシリーズA資金を確保しました。この資金は、人間のヘルスケアと種の保存における遺伝学の応用を強化するために利用されます。このような発展は、予測期間中のこの地域の市場成長を増大させると推定されます。
競争環境
制限酵素市場は中程度の競争があり、いくつかの主要企業で構成されています。市場を現在支配している企業には、Agilent Technologies、Thermo Fisher Scientific、Illumina Inc.、New England Biolabs、Merck KGaA、Promega Corporation、Takara Bio Inc.、QIAGEN NV、GenScript、TransGen Biotech Co., Ltd.などが挙げられます。
最近の業界動向
* 2022年8月:診断・研究スタートアップのMedGenomeが、ライフサイエンスに特化したNovo Holdings主導で5000万米ドルを調達しました。同社はゲノムシーケンシングプラットフォームを診断および創薬に利用しており、これには制限酵素が使用されます。
* 2022年3月:Roche CustomBiotechが制限酵素Xba Iを発売しました。これはmRNA治療薬およびワクチンの製造におけるin-vitro mRNA合成ステップの上流で使用されます。
このレポートは、制限酵素市場に関する詳細な分析を提供しています。制限酵素とは、特定のヌクレオチド配列またはその近くでDNA分子を切断し、ゲル電気泳動によって分離可能な個別のDNA断片を生成する酵素であり、生命科学研究やバイオテクノロジー産業において不可欠なツールとして利用されています。
市場規模に関して、世界の制限酵素市場は2024年に3億701万米ドルと推定されています。2025年には3億2895万米ドルに達すると予測されており、さらに2025年から2030年にかけて年平均成長率(CAGR)6.67%で成長し、2030年には4億5430万米ドルに達すると見込まれています。
市場の成長を牽引する主な要因としては、様々なアプリケーションにおける制限酵素の使用増加が挙げられます。具体的には、遺伝子工学、DNAマッピング、遺伝子シーケンシングといった分野での利用が拡大しており、これらの技術の進展が市場を活性化させています。また、バイオテクノロジー企業や製薬企業による研究開発(R&D)への支出が増加していることも、市場拡大に大きく寄与しています。新しい治療法の開発や診断技術の改良に向けた研究活動が活発化する中で、制限酵素の需要が高まっています。
一方で、市場の成長を抑制する要因も存在します。制限酵素の生産コストが高いことが、特に小規模な研究機関や企業にとって課題となっており、これが市場の普及を妨げる一因となっています。
本レポートでは、市場を多角的にセグメント化して分析しています。
タイプ別では、タイプI、タイプII、タイプIII、およびその他のタイプに分類されています。
アプリケーション別では、遺伝子工学、DNAマッピング、遺伝子シーケンシング、およびその他のアプリケーションに焦点を当てています。
エンドユーザー別では、製薬・バイオテクノロジー企業、学術研究機関、およびその他のエンドユーザーに区分されています。
地域別分析では、北米、欧州、アジア太平洋、およびその他の地域にわたる市場動向が詳細に調査されています。2025年には北米が最大の市場シェアを占めると予測されており、米国、カナダ、メキシコが主要な国として挙げられます。一方、アジア太平洋地域は、予測期間(2025年~2030年)において最も高いCAGRで成長すると見込まれており、中国、日本、インド、オーストラリア、韓国などがこの地域の成長を牽引すると考えられています。欧州市場もドイツ、英国、フランス、イタリア、スペインなどを中心に重要な役割を担っています。
競合状況のセクションでは、市場で活動する主要企業が特定され、そのプロファイルが提供されています。主要な競合企業には、Agilent Technologies、Thermo Fisher Scientific、Illumina Inc.、New England Biolabs、Merck KGaA、Promega Corporation、Takara Bio Inc.、QIAGEN NV、GenScript、TransGen Biotech Co., Ltd.などが含まれます。これらの企業については、事業概要、財務状況、製品と戦略、および最近の動向が分析されています。
さらに、本レポートには、ポーターのファイブフォース分析が含まれており、新規参入の脅威、買い手/消費者の交渉力、サプライヤーの交渉力、代替製品の脅威、および競争の激しさといった側面から市場の競争環境が評価されています。また、市場機会と将来のトレンドについても言及されており、今後の市場の方向性に関する洞察が提供されています。

1. はじめに
- 1.1 調査の前提条件と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場の動向
- 4.1 市場概要
-
4.2 市場の推進要因
- 4.2.1 さまざまな用途における制限酵素の使用の増加
- 4.2.2 バイオテクノロジーおよび製薬会社による研究開発費の増加
-
4.3 市場の阻害要因
- 4.3.1 制限酵素生産の高コスト
-
4.4 ポーターの5つの力分析
- 4.4.1 新規参入者の脅威
- 4.4.2 買い手/消費者の交渉力
- 4.4.3 供給者の交渉力
- 4.4.4 代替品の脅威
- 4.4.5 競争の激しさ
5. 市場セグメンテーション (金額別市場規模 – 米ドル)
-
5.1 タイプ別
- 5.1.1 タイプI
- 5.1.2 タイプII
- 5.1.3 タイプIII
- 5.1.4 その他のタイプ
-
5.2 用途別
- 5.2.1 遺伝子工学
- 5.2.2 DNAマッピング
- 5.2.3 遺伝子シーケンシング
- 5.2.4 その他の用途
-
5.3 エンドユーザー別
- 5.3.1 製薬・バイオテクノロジー企業
- 5.3.2 学術研究機関
- 5.3.3 その他のエンドユーザー
-
5.4 地域別
- 5.4.1 北米
- 5.4.1.1 米国
- 5.4.1.2 カナダ
- 5.4.1.3 メキシコ
- 5.4.2 ヨーロッパ
- 5.4.2.1 ドイツ
- 5.4.2.2 イギリス
- 5.4.2.3 フランス
- 5.4.2.4 イタリア
- 5.4.2.5 スペイン
- 5.4.2.6 その他のヨーロッパ
- 5.4.3 アジア太平洋
- 5.4.3.1 中国
- 5.4.3.2 日本
- 5.4.3.3 インド
- 5.4.3.4 オーストラリア
- 5.4.3.5 韓国
- 5.4.3.6 その他のアジア太平洋
- 5.4.4 その他の地域
6. 競争環境
-
6.1 企業プロフィール
- 6.1.1 アジレント・テクノロジー
- 6.1.2 サーモフィッシャーサイエンティフィック
- 6.1.3 イルミナ
- 6.1.4 ニューイングランド・バイオラボ
- 6.1.5 メルクKGaA
- 6.1.6 プロメガ・コーポレーション
- 6.1.7 タカラバイオ
- 6.1.8 キアゲンNV
- 6.1.9 ジェンスクリプト
- 6.1.10 トランスジェン・バイオテック
- *リストは網羅的ではありません
7. 市場機会と将来のトレンド
*** 本調査レポートに関するお問い合わせ ***

制限酵素とは、特定のDNA配列を認識し、その配列内またはその近傍を切断する酵素の総称です。これらは主に細菌がバクテリオファージなどの外来DNAから自身を守るための防御機構として機能しており、細菌自身のDNAはメチル化によって保護されています。制限酵素が認識するDNA配列は「認識配列」と呼ばれ、多くの場合、回文構造(パリンドローム)を持っています。この酵素によるDNAの切断は、分子生物学における遺伝子操作の基盤をなす極めて重要な技術です。
制限酵素にはいくつかの種類がありますが、分子生物学研究で最も広く利用されているのはタイプII制限酵素です。タイプII酵素は、認識配列内で正確にDNAを切断し、その活性にATPを必要としないため、操作が容易です。切断様式には大きく分けて二種類あります。一つは、DNAの二本鎖を同じ位置で切断し、平らな末端(平滑末端、blunt end)を生成するタイプです。もう一つは、二本鎖をずらして切断し、一本鎖の突出部を持つ末端(付着末端、sticky endまたはcohesive end)を生成するタイプです。付着末端は相補的な配列を持つ他のDNA断片と水素結合を形成しやすいため、DNAリガーゼによる結合(ライゲーション)が効率的に行えるという利点があります。代表的な制限酵素としては、EcoRI、HindIII、BamHIなどが挙げられ、それぞれ異なる認識配列と切断様式を持っています。
制限酵素の用途は多岐にわたります。最も基本的な用途は、遺伝子クローニングです。目的の遺伝子を含むDNA断片と、その遺伝子を導入するためのベクター(プラスミドなど)を同じ制限酵素で切断することで、相補的な付着末端を生成し、DNAリガーゼを用いて結合させ、組換えDNAを作製します。これにより、特定の遺伝子を大量に増幅したり、発現させたりすることが可能になります。また、DNAマッピングにも利用され、DNA分子上の制限酵素サイトの位置を特定することで、遺伝子の相対的な位置関係を明らかにすることができます。さらに、制限酵素断片長多型(RFLP)解析は、個体間のDNA配列の違いを制限酵素による切断パターンの違いとして検出し、遺伝病の診断、親子鑑定、犯罪捜査における個人識別などに用いられてきました。遺伝子工学全般において、制限酵素はDNAを「ハサミ」のように切断し、新しい組み合わせのDNA分子を構築するための不可欠なツールとなっています。
関連技術としては、まずDNAリガーゼが挙げられます。制限酵素で切断されたDNA断片を結合させる役割を担い、遺伝子クローニングには制限酵素とDNAリガーゼの組み合わせが必須です。また、制限酵素で切断したDNA断片のサイズを分離・確認するために、アガロースゲル電気泳動が広く用いられます。目的のDNA断片を増幅するポリメラーゼ連鎖反応(PCR)も、制限酵素と組み合わせて利用されることが多く、PCRで増幅した断片に制限酵素サイトを付加してクローニングに用いる手法が一般的です。さらに、遺伝子を細胞に導入するためのベクター(プラスミド、ウイルスベクターなど)も、制限酵素サイトを複数持つように設計されており、効率的な遺伝子導入を可能にしています。近年注目されているゲノム編集技術であるCRISPR-Cas9システムにおいても、ガイドRNAを組み込んだプラスミドの構築や、編集後のDNAの検証に制限酵素が利用されることがあります。
市場背景としては、制限酵素は分子生物学研究の黎明期から現在に至るまで、バイオテクノロジー産業において極めて重要な試薬であり続けています。世界中の多くのバイオテクノロジー企業が、数百種類に及ぶ制限酵素を研究機関や製薬企業、診断薬メーカーなどに供給しています。主要なサプライヤーとしては、New England Biolabs (NEB)、Takara Bio、Thermo Fisher Scientific、Promegaなどが挙げられます。これらの企業は、高純度で安定した活性を持つ制限酵素を提供するために、厳格な品質管理を行っています。制限酵素の市場は、遺伝子工学、ゲノム科学、診断薬開発、バイオ医薬品生産といった分野の成長とともに拡大しており、特に研究開発費の増加や新規バイオテクノロジー企業の台頭が市場を牽引しています。
将来展望としては、制限酵素の応用範囲はさらに広がると考えられます。新たな認識配列を持つ制限酵素の発見や、既存の酵素を改変して特異性や活性を向上させたエンジニアリング酵素の開発が進められています。これにより、より複雑なDNA構造の操作や、特定のゲノム領域のみを標的とする精密な切断が可能になるかもしれません。合成生物学の分野では、複数の遺伝子を組み合わせて人工的な生命システムを構築する際に、標準化された制限酵素サイトを利用したモジュール式の遺伝子構築が不可欠です。また、診断分野では、特定の病原体DNAやがん関連遺伝子の変異を検出するための高感度な制限酵素アッセイの開発が期待されます。ゲノム編集技術の進化に伴い、制限酵素は直接的なゲノム編集ツールとしての役割は減少しつつありますが、ゲノム編集ベクターの構築や、編集効率の評価、オフターゲット効果の検証など、周辺技術としての重要性は今後も維持されるでしょう。将来的には、より簡便で高精度な遺伝子操作を可能にするための、新しい制限酵素関連技術の開発が期待されています。