ワクチンアジュバント市場 規模・シェア分析、成長トレンドおよび予測 (2025年~2030年)
ワクチンアジュバント市場は、製品タイプ(鉱物塩ベースアジュバント、サポニンおよびトリテルペノイド、エマルションベースなど)、使用タイプ(活性免疫賦活剤、キャリアなど)、疾患タイプ(感染症、がんなど)、用途(研究用途、商業用途)、および地域(北米、欧州など)によってセグメント化されています。市場と予測は、金額(米ドル)で提供されます。

※本ページの内容は、英文レポートの概要および目次を日本語に自動翻訳したものです。最終レポートの内容と異なる場合があります。英文レポートの詳細および購入方法につきましては、お問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
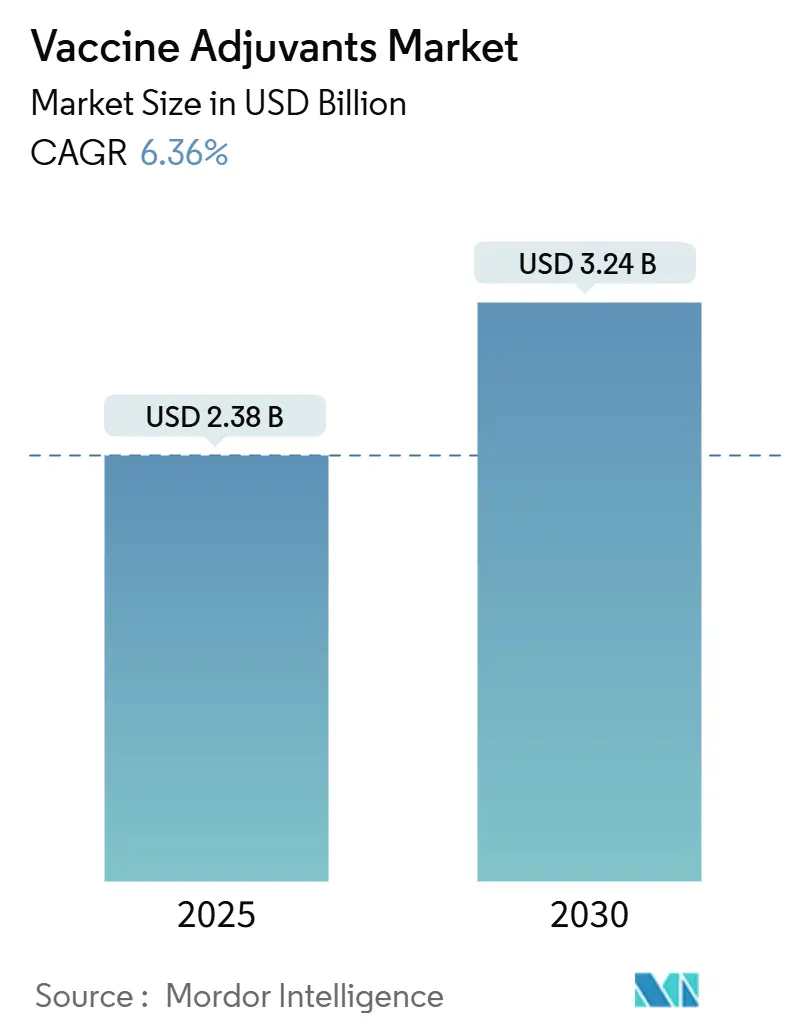
ワクチンアジュバント市場は、2019年から2030年を調査期間としています。2025年には23.8億米ドル、2030年には32.4億米ドルに達すると予測されており、2025年から2030年までの年平均成長率(CAGR)は6.36%です。最も急速に成長する市場はアジア太平洋地域であり、最大の市場は北米です。市場の集中度は中程度とされています。主要企業には、Adjuvatis、Merck KGaA、GlaxoSmithKline plc、Novavax Inc.、Croda International plcなどが挙げられます。
この市場の持続的な拡大は、製薬業界が次世代の免疫プラットフォームへと移行していること、免疫応答を増幅し、新しい抗原形式を可能にし、熱安定性のある製剤をサポートするための高度なアジュバント技術の必要性が高まっていることを反映しています。政府によるパンデミック対策へのコミットメントは、安定した購入量を確保し、AIを活用した設計は製剤開発サイクルを短縮し、コールドチェーンへの依存を減らすことで流通コストを削減し、世界的なアクセスを拡大しています。mRNA、自己増幅型RNA、ウイルス様粒子(VLP)ワクチンへの研究が活発化していることも需要を押し上げています。これらのプラットフォームは、精製または合成抗原の低い固有の免疫原性を補うために強力なアジュバントに依存しているためです。サポニンおよびトリテルペノイドの供給確保や、STINGアゴニストのような新規経路に対する規制の明確化は引き続き注視すべき点ですが、バイオテクノロジー革新への継続的な資本流入は、ワクチンアジュバント市場の長期的な魅力に対する信頼を示しています。
主要なレポートのポイント
* 製品タイプ別: 2024年にはサポニンおよびトリテルペノイド系が26.78%の収益シェアを占め、ウイルス様粒子(VLP)は2030年までに7.12%のCAGRで成長すると予測されています。
* 使用タイプ別: 2024年には活性免疫刺激剤がワクチンアジュバント市場シェアの47.89%を占め、ビークルアジュバントは2030年までに7.04%のCAGRで最も高い成長率を記録すると予測されています。
* 疾患タイプ別: 2024年には感染症ワクチンがワクチンアジュバント市場規模の72.45%を占めましたが、腫瘍学用途は7.06%のCAGRで拡大すると見込まれています。
* 用途別: 2024年には商業用ワクチンがワクチンアジュバント市場規模の68.31%を占め、研究用途は2030年までに7.34%のCAGRで進展しています。
* 地域別: 2024年には北米が41.12%のシェアを占め、アジア太平洋地域は2030年までに7.45%のCAGRで加速すると予測されています。
市場の成長要因
ワクチンアジュバント市場の成長を牽引する主な要因は以下の通りです。
* 政府による予防接種推奨の拡大: 各国政府が青少年、成人、高齢者向けのワクチン接種スケジュールを拡大しており、アジュバント含有製品の対象層が着実に増加しています。公衆衛生当局は、入院率の低下によるコスト削減効果も強調しており、アジュバントが豊富な製品への予算配分を強化しています。
* 新たな人獣共通感染症に対する満たされていないワクチンニーズ: 気候変動による生息地の変化、都市と野生生物の接触増加、グローバル貿易は、病原体のスピルオーバーイベントを促進し、迅速な免疫原性を得るために強力なアジュバントに依存する速効性ワクチンの需要を高めています。WHOは、パンデミック対策におけるアジュバントの役割を認識し、その開発と利用を奨励しています。
本レポートは、ワクチンアジュバントの世界市場に関する詳細な分析を提供しています。アジュバントとは、ワクチンの抗原に対する適応免疫応答を相乗的に促進し、誘導する薬理学的または免疫学的薬剤であり、感染症に対する長期的な防御と安全性を確保するためにワクチンに添加されます。市場は、製品タイプ、使用タイプ、疾患タイプ、用途、および地域別にセグメント化されており、世界の主要17カ国の市場規模とトレンドを網羅しています。
ワクチンアジュバントの世界市場は、2025年に23.8億米ドルの価値があり、2030年までに32.4億米ドルに達すると予測されています。
市場の成長を牽引する主な要因としては、政府による予防接種推奨の拡大、新たな人獣共通感染症に対する満たされていないワクチンニーズの増加が挙げられます。また、組換え抗原や合成抗原の採用拡大、新規アジュバントに対するmRNAプラットフォームの需要加速、微生物由来TLRアゴニストのパイプライン拡大も重要な推進力です。さらに、AI設計のナノアルミニウム製剤によるコールドチェーン不要な流通の実現も、市場拡大に貢献しています。
一方で、市場の成長を抑制する要因も存在します。局所的および全身性の毒性に関する懸念、高い発見・前臨床スクリーニングコストが挙げられます。また、スクアレンやQS-21のサプライチェーンにおけるスケールアップの課題、新規STINGアゴニストに関する規制の不確実性も、市場にとっての課題となっています。
製品タイプ別では、サポニンおよびトリテルペノイド系アジュバントが2024年に26.78%のシェアを占め、帯状疱疹やマラリアワクチンでの広範な使用により市場をリードしています。最も急速に成長しているセグメントはウイルス様粒子(VLP)アジュバントであり、スケーラブルなナノ構造プラットフォームにより2030年までに年平均成長率(CAGR)7.12%を記録すると予測されています。その他、鉱物塩アジュバント、エマルジョンベース、リポソームおよびビロソーム、炭水化物および多糖類、細菌由来TLRアゴニストなどが主要な製品タイプとして挙げられます。
地域別では、アジア太平洋地域が最も急速な成長を遂げると予測されており、中国、インド、東南アジアにおける予防接種プログラムの拡大と現地製造の進展により、2030年までに年平均成長率7.45%で成長すると見込まれています。
mRNAワクチンにおいてアジュバントは極めて重要です。mRNA構造体は、エンドソームからの脱出とバランスの取れた自然免疫活性化を確実にするための送達粒子を必要とします。最適化されたアジュバントは、炎症を緩和しながら抗原発現を促進する役割を果たします。
ワクチンアジュバント市場は中程度の集中度を示しており、上位5社が収益の60%強を占めています。これにより、新規参入企業が市場に影響を与える余地も残されています。主要な企業には、GlaxoSmithKline plc、Seppic (Air Liquide)、Dynavax Technologies Corp.、Croda International plc (Croda Pharma)、CSL Limited (BioCSL, Seqirus)、Merck KGaA (Sigma-Aldrich)、Novavax Inc.、Thermo Fisher Scientific Inc.などが挙げられます。
ワクチンアジュバント市場は、政府の支援、新たな疾患への対応、技術革新に支えられ、今後も堅調な成長が期待されます。しかし、安全性、コスト、規制の課題への対応が、持続的な発展には不可欠です。

1. はじめに
- 1.1 調査の前提と市場の定義
- 1.2 調査範囲
2. 調査方法
3. エグゼクティブサマリー
4. 市場概況
- 4.1 市場概要
-
4.2 市場の推進要因
- 4.2.1 政府の予防接種推奨の拡大
- 4.2.2 新興人獣共通感染症に対する満たされていないワクチンニーズ
- 4.2.3 組換え抗原および合成抗原の採用増加
- 4.2.4 新規アジュバントに対するmRNAプラットフォームの需要加速
- 4.2.5 微生物由来TLRアゴニストパイプラインの拡大
- 4.2.6 AI設計のナノアルミニウム製剤によるコールドチェーン不要の流通
-
4.3 市場の阻害要因
- 4.3.1 局所および全身毒性の懸念
- 4.3.2 高い発見および前臨床スクリーニングコスト
- 4.3.3 スクアレンおよびQS-21サプライチェーンのスケールアップの課題
- 4.3.4 新規STINGアゴニストに関する規制の不確実性
- 4.4 規制環境
-
4.5 ポーターの5つの力分析
- 4.5.1 新規参入者の脅威
- 4.5.2 買い手の交渉力
- 4.5.3 供給者の交渉力
- 4.5.4 代替品の脅威
- 4.5.5 競争の激しさ
5. 市場規模と成長予測(金額、米ドル)
-
5.1 製品タイプ別
- 5.1.1 鉱物塩アジュバント
- 5.1.2 サポニンおよびトリテルペノイド
- 5.1.3 エマルションベース
- 5.1.4 リポソームおよびビロソーム
- 5.1.5 炭水化物&多糖類
- 5.1.6 細菌由来TLRアゴニスト
- 5.1.7 ウイルス様粒子
- 5.1.8 その他の製品タイプ
-
5.2 使用タイプ別
- 5.2.1 活性免疫賦活剤
- 5.2.2 キャリア
- 5.2.3 ビヒクルアジュバント
-
5.3 疾患タイプ別
- 5.3.1 感染症
- 5.3.2 がん
- 5.3.3 その他
-
5.4 用途別
- 5.4.1 研究用途
- 5.4.2 商業用途
-
5.5 地域別
- 5.5.1 北米
- 5.5.1.1 米国
- 5.5.1.2 カナダ
- 5.5.1.3 メキシコ
- 5.5.2 ヨーロッパ
- 5.5.2.1 ドイツ
- 5.5.2.2 イギリス
- 5.5.2.3 フランス
- 5.5.2.4 イタリア
- 5.5.2.5 スペイン
- 5.5.2.6 その他のヨーロッパ
- 5.5.3 アジア太平洋
- 5.5.3.1 中国
- 5.5.3.2 日本
- 5.5.3.3 インド
- 5.5.3.4 オーストラリア
- 5.5.3.5 韓国
- 5.5.3.6 その他のアジア太平洋
- 5.5.4 中東およびアフリカ
- 5.5.4.1 GCC
- 5.5.4.2 南アフリカ
- 5.5.4.3 その他の中東およびアフリカ
- 5.5.5 南米
- 5.5.5.1 ブラジル
- 5.5.5.2 アルゼンチン
- 5.5.5.3 その他の南米
6. 競合情勢
- 6.1 市場集中度
- 6.2 市場シェア分析
-
6.3 企業プロファイル(グローバルレベルの概要、市場レベルの概要、主要セグメント、利用可能な財務情報、戦略情報、主要企業の市場ランク/シェア、製品&サービス、および最近の動向を含む)
- 6.3.1 グラクソ・スミスクライン plc
- 6.3.2 セピック (エア・リキード)
- 6.3.3 ダイナバックス・テクノロジーズ社
- 6.3.4 クローダ・インターナショナル plc (クローダ・ファーマ)
- 6.3.5 CSLリミテッド (BioCSL, セキルス)
- 6.3.6 メルク KGaA (シグマ・アルドリッチ)
- 6.3.7 ノババックス社
- 6.3.8 サーモフィッシャーサイエンティフィック社
- 6.3.9 アジェナス社
- 6.3.10 アジュバティス SAS
- 6.3.11 インビボジェン
- 6.3.12 SPIファーマ (ABF plc)
- 6.3.13 ヴァーテラス
- 6.3.14 パシフィック・ジーンテック社
- 6.3.15 OZバイオサイエンス
- 6.3.16 アジュバンス・テクノロジーズ社
- 6.3.17 ヴァルネバ SE
- 6.3.18 ババリアン・ノルディック A/S
- 6.3.19 ファイザー社
- 6.3.20 アストラゼネカ plc
- 6.3.21 アバンティ・ポーラー・リピッズ (クローダ)
7. 市場機会&将来展望
*** 本調査レポートに関するお問い合わせ ***

ワクチンアジュバントとは、ワクチンに含まれる抗原の免疫原性を増強し、より強力で持続的な免疫応答を誘導するために添加される物質の総称です。抗原単独では十分な免疫反応が得られない場合や、より少ない抗原量で効果的な免疫を確立したい場合に不可欠な成分として、現代のワクチン開発において極めて重要な役割を担っています。その主な作用機序としては、抗原提示細胞の活性化、サイトカインの産生誘導、抗原の局所滞留時間の延長などが挙げられ、これらを通じて自然免疫系を刺激し、その後の獲得免疫応答へと繋げていきます。アジュバントは、ワクチンの有効性を高める一方で、安全性も同時に確保されなければならないため、その開発と評価には厳格な基準が設けられています。
アジュバントには様々な種類が存在し、それぞれ異なる作用機序と免疫応答の誘導パターンを持っています。最も古くから広く使用されているのは、水酸化アルミニウムやリン酸アルミニウムなどの「アルミニウム塩(ミョウバン)」です。これらは抗原を吸着・沈殿させることで、局所での抗原提示を促進し、主に液性免疫(抗体産生)を誘導する効果があります。次に、「エマルジョン系アジュバント」として、油中水型や水中油型の製剤があり、MF59やAS03などが代表的です。これらは抗原の放出を遅延させるとともに、局所的な炎症反応を引き起こすことで免疫応答を増強します。さらに、病原体由来の成分を模倣した「TLR(Toll-like Receptor)アゴニスト」も重要なカテゴリーです。例えば、細菌由来のLPS誘導体であるMPL(Monophosphoryl lipid A)や、植物由来のサポニンであるQS-21、合成CpGオリゴヌクレオチドなどがこれに該当します。これらは自然免疫系の特定の受容体を直接刺激し、サイトカイン産生や抗原提示細胞の成熟を促すことで、特に細胞性免疫(T細胞応答)の誘導に優れています。近年では、複数のアジュバントを組み合わせることで、それぞれの利点を活かし、より広範で強力な免疫応答を狙う「複合アジュバント」の開発も進んでおり、AS04(アルミニウム塩とMPLの複合体)やAS01(QS-21とMPLをリポソームに封入したもの)などが実用化されています。
アジュバントの用途は多岐にわたります。まず、組換えタンパク質ワクチンや合成ペプチドワクチンなど、免疫原性が比較的低い抗原を用いた新規ワクチンにおいて、十分な免疫応答を引き出すために不可欠です。B型肝炎ワクチン、HPVワクチン、インフルエンザワクチン、肺炎球菌ワクチン、帯状疱疹ワクチンなど、多くの既存ワクチンにアジュバントが使用されています。また、アジュバントは免疫応答の質と量を向上させる役割も担います。具体的には、抗体価の増強やその持続期間の延長、さらにはウイルス感染症やがんに対する防御に重要な細胞性免疫(キラーT細胞応答)の誘導、そしてTh1/Th2免疫応答のバランス調整などが挙げられます。パンデミック時など、抗原の供給が限られる状況においては、アジュバントによって少ない抗原量で効果的な免疫を誘導できる「抗原量節約効果(Dose Sparing)」も重要な利点となります。HIV、マラリア、結核、がんなど、これまで有効なワクチンがなかった難治性疾患に対する新規ワクチン開発においても、アジュバントは成功の鍵を握る要素として期待されています。
関連技術としては、アジュバントと抗原を効率的に免疫細胞に届けるための「デリバリーシステム」が挙げられます。リポソーム、ナノ粒子、ウイルス様粒子(VLP)などがその代表例であり、これらは抗原とアジュバントの安定性を高め、標的細胞への送達を最適化することで、ワクチンの効果をさらに向上させます。また、アジュバントの効果を正確に評価するためには、サイトカインプロファイル、T細胞応答、B細胞応答などを詳細に解析する「免疫モニタリング技術」が不可欠です。近年では、バイオインフォマティクスや人工知能(AI)を活用し、新規アジュバントのスクリーニングや作用機序の予測を行う研究も進められており、アジュバント開発の効率化に貢献しています。遺伝子組換え技術を用いて、アジュバント活性を持つタンパク質を生産するアプローチも研究されています。
ワクチンアジュバントの市場は、新規ワクチンの開発増加や既存ワクチンの改良ニーズの高まりを背景に、世界的に拡大傾向にあります。グラクソ・スミスクライン(GSK)、サノフィ、ファイザー、メルクなどの大手製薬企業が主要なプレイヤーであり、彼らは長年の研究開発を通じて多様なアジュバントを実用化してきました。一方で、中小のバイオベンチャー企業も、特定の免疫応答を誘導する新規アジュバントや、より安全性の高いアジュバントの開発に注力しています。アジュバントを含むワクチンの開発には、各国規制当局(FDA、EMA、PMDAなど)による厳格な安全性と有効性の評価が求められ、承認プロセスは非常に複雑です。COVID-19パンデミックにおいては、mRNAワクチンがアジュバントを必要としない一方で、サブユニットワクチンではアジュバントの重要性が改めて認識され、パンデミック対応ワクチンの迅速な開発においてその役割が注目されました。
将来展望として、ワクチンアジュバントの研究開発は、より強力で安全性の高い新規アジュバントの探索に注力されるでしょう。特に、特定の免疫応答(例えば、粘膜免疫や細胞性免疫)を効率的に誘導できるアジュバントや、作用機序がより明確に解明されたアジュバントの開発が期待されています。また、患者個々の免疫状態や疾患の種類に応じた「個別化医療」への応用も視野に入れられており、最適なアジュバントの選択が重要となる可能性があります。複数の抗原に対応できる多価ワクチンや複合ワクチンへの応用も進むでしょう。安全性と忍容性の向上も引き続き重要な課題であり、副作用の軽減や局所反応の抑制を目指した研究が続けられます。AIや機械学習の活用は、アジュバントの設計や最適化を加速させ、開発コストの削減にも寄与すると考えられます。最終的には、これらの進歩が、途上国における感染症対策ワクチンを含むグローバルヘルスへの貢献に繋がることが期待されています。